Апоптоз что это такое
Апоптоз, или запрограммированная гибель клеток, является естественным процессом в организме. Он включает в себя контролируемую последовательность событий, в которых клетка сигнализируют о самоуничтожении. Апоптоз помогает контролировать естественный процесс деления клеток посредством митоза.
Почему клетки проходят апоптоз?
Существует несколько случаев, когда клеткам необходимо самоуничтожение. Например, естественный процесс менструации включает в себя распад и удаление ткани из матки. Также клетки могут подвергнутся повреждению или некоторым типам инфекции. Один из способов убрать эти клетки, не причинив вреда здоровым клеткам, является апоптоз.
Что происходит во время апоптоза?
Апоптоз — сложный процесс, который включает в себя множество событий. Во время апоптоза клетка вызывает процесс изнутри, что позволяет ей совершить самоубийство. Если клетка испытывает некоторый тип значительного стресса, такой как повреждение ДНК, то высвобождаются сигналы, которые активируют митохондрии для высвобождения белков индуцирующих апоптоз.
В результате клетка подвергается уменьшению размера, поскольку ее клеточные компоненты и органеллы разрушаются и конденсируются. На поверхности клеточной мембраны появляются пузырьки, повышающие ее проницаемость. Затем клетка разделяется на более мелкие фрагменты, называемые апоптозными телами. Эти фрагменты заключены в мембраны, чтобы не повредить соседние клетки.
Затем фагоцитарные клетки, такие как макрофаги, поглощают и разрушают апоптотические тела, не вызывая воспалительную реакцию. Апоптоз также может запускаться снаружи химическими веществами, которые связываются с конкретными рецепторами на поверхности клетки. Это путь, используемый некоторыми лейкоцитами для активации апоптоза в инфицированных клетках.
Апоптоз и рак
Некоторые виды рака сохраняются в результате неспособности клетки пройти апоптоз. Опухолевые вирусы меняют клетки путем интеграции их генетического материала с ДНК клетки-хозяина. Эти вирусы инициируют производство белков, останавливающими процесс апоптоза. Пример этого можно увидеть с вирусами папилломы, которые связывают с раком шейки матки. Раковые клетки, которые не развиваются из вирусной инфекции, могут также продуцировать вещества, ингибирующие апоптоз и способствуют неконтролируемому росту. Радиационная и химическая терапия используется для индукции апоптоза при некоторых видах рака.
Понравилась статья? Поделись с друзьями:
Источник: NatWorld.info
Что такое апоптоз
Апоптоз – это контролируемый физиологический процесс самоуничтожения клетки, характеризующийся поэтапным разрушением и фрагментацией ее содержимого с формированием мембранных пузырьков (апоптозных телец), впоследствии поглощаемых фагоцитами. Этот генетически заложенный механизм активируется под воздействием определенных внутренних или внешних факторов.
При таком варианте гибели клеточное содержимое не выходит за пределы мембраны и не вызывает воспаление. Нарушения в регуляции апоптоза приводят к серьезным патологиям, таким как неконтролируемые клеточные деления или дегенерация тканей.
Апоптоз представляет собой лишь одну из нескольких форм запрограммированной гибели клетки (ЗГК), поэтому отождествлять эти понятия ошибочно. К известным видам клеточного самоуничтожения относят также митотическую катастрофу, аутофагию и программированный некроз. Другие механизмы ЗГК пока не изучены.
Причины апоптоза клеток
Причиной запуска механизма запрограммированной клеточной гибели могут быть как естественные физиологические процессы, так и патологические изменения, вызванные внутренними дефектами или воздействием внешних неблагоприятных факторов.
В норме апоптоз уравновешивает процесс деления клеток, регулируя их количество и способствуя обновлению тканей. В таком случае причиной ЗГК служат определенные сигналы, входящие в систему контроля гомеостаза. С помощью апоптоза уничтожаются одноразовые или выполнившие свою функцию клетки. Так, повышенное содержание лейкоцитов, нейтрофилов и других элементов клеточного иммунитета по окончании борьбы с инфекцией устраняется именно за счет апоптоза.
Запрограммированная гибель является частью физиологического цикла репродуктивных систем. Апоптоз задействован в процессе оогенеза, а также способствует гибели яйцеклетки при отсутствии оплодотворения.
Классическим примером участия апоптоза клеток в жизненном цикле вегетативных систем является осенний листопад. Сам термин происходит от греческого слова apoptosis, что буквально переводится как «опадание».
Апоптоз играет важнейшую роль в эмбриогенезе и онтогенезе, когда в организме сменяются ткани и атрофируются определенные органы. Примером могут служить исчезновение перепонок между пальцами конечностей некоторых млекопитающих или отмирание хвоста при метаморфозе лягушки.
Апоптоз может быть спровоцирован накоплением дефектных изменений в клетке, возникших в результате мутаций, старения или ошибок митоза. Причиной запуска ЗГК могут быть неблагоприятная среда (недостаток питательных компонентов, дефицит кислорода) и патологические внешние воздействия, опосредованные вирусами, бактериями, токсинами и т. д. При этом если повреждающий эффект слишком интенсивен, то клетка не успевает осуществить механизм апоптоза и погибает в результате развития патологического процесса – некроза.
Морфологические и структурно-биохимические изменения клетки во время апоптоза
Процесс апоптоза характеризуется определенным набором морфологических изменений, которые с помощью микроскопии можно наблюдать в препарате ткани in vitro.
К основным признакам, характерным для апоптоза клеток, относят:
- перестраивание цитоскелета;
- уплотнение клеточного содержимого;
- конденсацию хроматина;
- фрагментацию ядра;
- уменьшение объема клетки;
- сморщивание контура мембраны;
- образование пузырьков на клеточной поверхности,
- деструкцию органоидов.
У животных эти процессы завершаются образованием апоптоцитов, которые могут быть поглощены как макрофагами, так и соседними клетками ткани. У растений формирования апоптозных телец не происходит, а после деградации протопласта сохраняется остов в виде клеточной стенки.
Помимо морфологических изменений, апоптоз сопровождается рядом перестроек на молекулярном уровне. Происходит повышение липазной и нуклеазной активностей, которые влекут за собой фрагментацию хроматина и многих белков. Резко увеличивается содержание сАМФ, изменяется структура клеточной мембраны. В растительных клетках наблюдается образование гигантских вакуолей.
Чем апоптоз отличается от некроза
Главное различие между апоптозом и некрозом заключается в причине клеточной деградации. В первом случае источником разрушения служат молекулярные инструменты самой клетки, которые работают под строгим контролем и требуют затрат энергии АТФ. При некрозе происходит пассивное прекращение жизнедеятельности из-за внешнего повреждающего воздействия.
Апоптоз – это естественный физиологический процесс, сконструированный таким образом, чтобы не вредить окружающим клеткам. Некроз – это неконтролируемое патологическое явление, возникающее в результате критических повреждений. Поэтому неудивительно, что механизм, морфология и последствия апоптоза и некроза во многом противоположны. Однако имеются и общие черты.
| Характеристика процесса | Апоптоз | Некроз |
| объем клетки | уменьшается | увеличивается |
| целостность мембраны | сохраняется | нарушается |
| воспалительный процесс | отсутствует | развивается |
| энергия АТФ | затрачивается | не используется |
| фрагментация хроматина | имеется | присутствует |
| резкое падение концентрации АТФ | есть | есть |
| итог процесса | фагоцитоз | выброс содержимого в межклеточное пространство |
В случае повреждения клетки запускают механизм запрограммированной гибели в том числе для того, чтобы не допустить некротического развития. Однако недавние исследования показали, что существует иная непатологическая форма некроза, которую также отнесли к ЗГК.
Биологическое значение апоптоза
Несмотря на то что апоптоз приводит к клеточной гибели, его роль для поддержания нормальной жизнедеятельности всего организма очень велика. Благодаря механизму ЗГК осуществляются следующие физиологические функции:
- поддержание баланса между пролиферацией и смертью клеток;
- обновление тканей и органов;
- устранение дефектных и «старых» клеток;
- защита от развития патогенного некроза;
- смена тканей и органов при эмбрио- и онтогенезе;
- удаление ненужных элементов, выполнивших свою функцию;
- устранение клеток, нежелательных или опасных для организма (мутантных, опухолевых, зараженных вирусом);
- предотвращение развития инфекции.
Таким образом, апоптоз является одним из способов поддержания клеточно-тканевого гомеостаза.
У растений апоптоз часто запускается, чтобы блокировать распространение инфицирующих ткани паразитических агробактерий.
Этапы клеточной смерти
То, что происходит с клеткой при апоптозе, является результатом сложной цепочки молекулярных взаимодействий между различными ферментами. Реакции проходят по типу каскада, когда одни белки активируют другие, способствуя постепенному развитию сценария гибели. Этот процесс можно разделить на несколько этапов:
- Индукция.
- Активация проапоптических белков.
- Активация каспаз.
- Разрушение и перестройка клеточных органелл.
- Формирование апоптоцитов.
- Подготовка клеточных фрагментов к фагоцитозу.
Синтез всех компонентов, необходимых для запуска, реализации и контроля каждого этапа заложен генетически, почему апоптоз и называют запрограммированной гибелью клетки. Активация этого процесса находится под строгим контролем регуляторных систем, включающих в том числе и различные ингибиторы ЗГК.
Молекулярные механизмы апоптоза клетки
Развитие апоптоза обуславливается совокупным действием двух молекулярных систем: индукционной и эффекторной. Первый блок отвечает за контролируемый запуск ЗГК. В него входят так называемые рецепторы смерти, Cys-Asp-протеазы (каспазы), ряд митохондриальных компонентов и проапоптических белков. Все элементы индукционной фазы можно разделить на тригеры (участвуют в индукции) и модуляторы, обеспечивающие трансдукцию сигнала смерти.
Эффекторную систему составляют молекулярные инструменты, обеспечивающие деградацию и перестройку клеточных компонентов. Переход между первой и второй фазами осуществляется на этапе протеолитического каспазного каскада. Именно за счет компонентов эффекторного блока происходит гибель клетки при апоптозе.
Факторы апоптоза
Структурно-морфологические и биохимические изменения при апоптозе осуществляются определенным набором специализированных клеточных инструментов, среди которых наиболее важными являются каспасы, нуклеазы и мембранные модификаторы.
Каспазы – группа ферментов, разрезающих пептидные связи по остаткам аспарагина, фрагментируя белки на крупные пептиды. До начала апоптоза присутствуют в клетке в неактивном состоянии из-за ингибиторов. Главной мишенью каспаз являются ядерные белки.
Нуклеазы – ответственны за разрезание молекул ДНК. Особо важна в развитии апоптоза активная эндонуклеаза CAD, разрывающая участки хроматина в областях линкерных последовательностей. В результате образуются фрагменты длиной 120-180 нуклеотидных пар. Комплексное воздействие протеолитических каспаз и нуклеаз приводит к деформации и фрагментации ядра.
Модификаторы клеточной мембраны – нарушают асимметричность билипидного слоя, превращая его в мишень для фагоцитирующих клеток.
Ключевая роль в развитии апоптоза принадлежит каспазам, которые поэтапно активируют все последующие механизмы деградации и морфологической перестройки.
Роль каспаз в клеточной гибели
Семейство каспаз включает 14 белков. Часть из них не задействована в апоптозе, а остальные подразделяются на 2 группы: инициаторные (2, 8, 9, 10, 12) и эффекторные (3, 6 и 7), которые иначе называются каспазами второго эшелона. Все эти белки синтезируются в виде предшественников – прокаспаз, активируемых протеолитическим расщеплением, суть которого состоит в отсоединении N-концевого домена и разделении оставшейся молекулы на две части, в последствии ассоциирующиеся в димеры и тетрамеры.
Инициаторные каспазы необходимы для активации эффекторной группы, которая проявляет протеолитическую активность в отношении различных жизненно важных клеточных белков. К субстратам каспаз второго эшелона относятся:
- ферменты репарации ДНК;
- игибитор белка р-53;
- поли-(ADP-рибозо)-полимераза;
- ингибитор ДНК-азы DFF (разрушение этого белка приводит к активации эндонуклеазы CAD) и др.
Общее количество мишеней эффекторных каспаз насчитывает более 60 белков.
Ингибирование апоптоза клеток еще возможно на стадии активации инициаторных прокаспаз. Когда эффекторные каспазы вступают в действие, процесс становится необратимым.
Пути активации апоптоза
Передача сигнала для запуска апоптоза клетки может быть осуществлена двумя путями: рецепторным (или внешним) и митохондриальным. В первом случае процесс активируется через специфические рецепторы смерти, воспринимающие внешние сигналы, которыми служат белки семейства TNF (фактора некроза опухолей) или Fas-лиганды, расположенные на поверхности Т-киллеров.
В состав рецептора входит 2 функциональных домена: трансмембранный (предназначенный для связи с лигандом) и ориентированный внутрь клетки «домен смерти», индуцирующий апоптоз. Механизм рецепторного пути основывается на образовании DISC-комплекса, активирующего инициаторные каспазы 8 или 10.
Сборка начинается со взаимодействия домена смерти с внутриклеточными адапторными белками, которые, в свою очередь, связывают инициаторные прокаспазы. В составе комплекса последние превращаются в функционально-активные каспазы и запускают дальнейший апоптозный каскад.
Механизм внутреннего пути основан на активации протеолитического каскада особыми митохондриальными белками, выброс которых контролируется внутриклеточными сигналами. Выход компонентов органоидов осуществляется через образование огромных пор.
Особая роль в запуске принадлежит цитохрому с. Попадая в цитоплазму, этот компонент электротранспортной цепи связывается с белком Apaf1 (апоптотический фактор активации протеаз), что приводит к активации последнего. Затем Apaf1 связывают инициаторные прокаспазы 9, которые по механизму каскада запускают апоптоз.
Контроль внутреннего пути осуществляется особой группой белков семейства Bcl12, которые регулируют выход межмембранных компонентов митохондрий в цитоплазму. В составе семейства имеются как проапоптические, так и антиапоптические белки, баланс между которыми и определяет, будет ли запущен процесс.
К одним из мощных факторов, запускающих апоптоз по митохондриальному механизму, относятся реактивные формы кислорода. Еще одним значимым индуктором является белок р53, который активирует митохондриальный путь при наличии ДНК-повреждений.
Иногда запуск апоптоза клеток сочетает в себе сразу два пути: как внешний, так и внутренний. Последний обычно служит для усиления рецепторной активации.
Источник: fb.ru
Апоптоз — это генетически регулируемая программа клеточной гибели, которая имеет определенные морфологические критерии и биохимические маркеры. Эта программа очень важна для нормального развития многоклеточного организма, сохранения нормального числа полноценных и своевременного удаления поврежденных клеток.
Термин «апоптоз» (гр. аро — полное, ptosis — падение, утрата) предложил в 1972 году J. F. Kerr, заимствовав его у Гиппократа, назвавшего так осенний листопад.
Известно, что действие сильных повреждающих факторов вызывает некроз клетки. Гибель клетки в этом случае обусловлена избыточной внешней энергией (физической, химической или биологической), нарушающей ее внутриклеточный энергетический баланс и приводящей к потере структурной целостности.
В последние годы растет интерес к запрограммированной гибели клеток — апоптозу. Важно понимать, что фактор, вызывающий апоптоз, не обладает достаточной энергией для непосредственного повреждения клетки. Он лишь включает ее собственные механизмы самоуничтожения, т.е. апоптоз реализуется за счет внутренней энергии клетки и является таким же неотъемлемым свойством живого, как рост, пролиферация и размножение.
Возможности регуляции клеточной жизни всегда вызывали большой интерес биологов и врачей. Если процессы пролиферации являются достаточно изученными, то точка зрения на регуляцию разрушения (умирания) клеток пока еще не оформлена в окончательном виде в то же время при многих состояниях нарушения именно этой программы становятся определяющими для течения заболевания.
Апоптоз имеет четко выраженные и довольно хорошо изученные морфологические критерии: уменьшение размеров, сморщивание клетки, конденсация и фрагментация ядра, разрушение цитоскелета при сохранении целостности клеточной мембраны.
Апоптотические тельца
Когда процесс внутренней деградации завершен, клетка представляет собой совокупность фрагментов цитоплазмы, окруженных мембранами (т. н. апоптотические тельца). Изоляция внутриклеточного содержимого элементами цитолеммы является главной причиной отсутствия асептического воспаления при апоптозе. Таким образом, гибель клетки путем апоптоза (в отличие от некротической) переносится организмом относительно «безболезненно». В последующем апоптотические тельца фагоцитируются макрофагами, где макромолекулы погибшей клетки расщепляются до мономеров.
Сегодня установлено множество факторов, способных индуцировать апоптоз клетки. С другой стороны, некоторые воздействия могут повысить устойчивость к запрограммированной гибели (табл. 1).
|
I. Ингибиторы апоптоза |
|
Физиологические ингибиторы |
|
|
Гены вирусов |
|
|
Фармакологические агенты |
|
|
II. Индукторы апоптоза |
|
Физиологические активаторы |
|
|
Агенты, вызывающие повреждение |
|
|
Агенты, связанные с лечением каких-либо заболеваний |
|
|
Токсины |
|
В иммунной системе апоптоз выполняет по крайней мере две функции. Во-первых, апоптоз это эффекторный механизм иммунных реакций. Вторая функция апоптоза — регуляция иммунного ответа.
Эффекторный механизм иммунных реакций
см. Клеточная цитотоксичность
Регуляция иммунного ответа
Апоптоз иммунокомпетентных клеток является неотъемлемым компонентом иммунных реакций. Установлено, что селекция антигенспецифических Т- и В-лимфоцитов сопровождается массовой гибелью активированных, но антигеннеспецифических лимфоцитов. С другой стороны, результатом иммунного ответа является накопление избыточного количества антигенспецифических Т- и В-клеток, что ведет к нарушению генетически детерминированного баланса клеток макроорганизма. Выравнивание клеточного баланса после удаления патогена обусловлено именно запрограммированной гибелью большей части антигенспецифических лимфоцитов.
Цитоплазматический апоптоз
Как уже указывалось, апоптоз является внутренним свойством клетки, своеобразной ее реакцией на различные внешние раздражители. Поэтому неудивительно, что в любой клетке человеческого организма функционирует целая система цитоплазматического апоптоза (рис. 32), Информация о структуре компонентов этой системы содержится в геноме и передается от поколения к поколению. Указанную систему цитоплазматического апоптоза условно можно разделить на три части. Первая — это совокупность мембранных рецепторов, способных воспринимать проапоптотические сигналы из внутренней среды организма. Вторая — это комплекс цитоплазматических посредников, передающих воспринятый рецептором сигнал внутрь клетки к эффекторному звену. Третья — это эффекторное звено апоптоза, т.е. те компоненты, активация которых приводит к непосредственной гибели клетки.
Рецепторы апоптоза
Сегодня открыт целый ряд рецепторов, воспринимающих проапоптотические сигналы. Это Fas (CD95), TNF-R1 (рецептор 1-го типа к ФНО-α), DR3 (WS1-1), DR4 (TRAIL-рецептор 1), DR5 (1 RAIL-рецептор 2), DR6. Хотя указанные рецепторы приводят к одному и тому же биологическому эффекту, они относятся к разным семействам и поэтому отличаются по структуре. Так, Fas и TNF-R принадлежат к семейству рецепторов к ФF10, а молекулы DR — к антигенам гистосовместимости. Общность их биологического действия обусловлена природой молекул, связанных с цитоплазматической частью рецептора. Такие молекулы получили название доменов смерти Именно они и приводят к активации апоптоза. Наиболее изученными доменами смерти являются молекулы FADD и TRADD.
Ферменты апоптоза
Цитоплазматическими посредниками в системе апоптоза являются специальные ферменты, каспазы. Каспазы способны к последовательной активации друг друга, поэтому образуют своеобразный внутриклеточный каскад, включаемый доменами смерти. Домены смерти находятся на внутренней поверхности цитолеммы в неактивном состоянии. При активации рецептора, с которым функционально связан тот или иной домен, происходит изменение конформации обеих структур. Вследствие этого высвобождается активный центр домена, и он приобретает возможность взаимодействовать с каспазой 8 — инициатором всего каспазного каскада. Конечным компонентом этого каскада является каспаза 7. Именно этот фермент активирует латентную эндонуклеазу, оказывающую непосредственный повреждающий эффект на генетический материал клетки (разрывает ДНК в межнуклеосомных участках). Таким образом, эффекторным звеном системы апоптоза является латентная эндонуклеаза.
Митохондриальный апоптоз
Кроме цитоплазматических, в клетке содержится комплекс митохондриальных посредников апоптоза. Известно, что разрушение митохондриального аппарата приводит к неминуемой гибели клетки, поскольку последняя лишена энергетического обеспечения Для предотвращения некроза при повреждении митохондрий активируются указанные белки, обуславливающие более экономную апоптотическую гибель нежизнеспособной клетки. Таким образом, каскад апоптоза может реализовываться как по цитоплазматическому, так и по митохондриальному пути.
см. Регуляция апоптоза
Источник: wiki-med.com
Министерство Образования Российской Федерации
Удмуртский Государственный Университет
Реферат
на тему:
«Апоптоз»
Выполнила: Пермитина Л.А.
Студентка 5 курса БХФ
Ижевск, 2015
Содержание
Апоптоз
Морфологические проявления апоптоза
Сжатие клетки
Конденсация хроматина
Формирование в цитоплазме полостей и апоптотических телец
Механизм апоптоза
Регуляция апоптоза
Автономный механизм апоптоза
Снижение апоптоза
Ускорение апоптоза
Значение апоптоза в развитии организма и патологических процессах
Список литературы
Апоптоз
В организме здорового человека клеточный гомеостаз определяется балансом между гибелью и пролиферацией клеток. Апоптоз — программированная клеточная гибель, энергетически зависимый, генетически контролируемый процесс, который запускается специфическими сигналами и избавляет организм от ослабленных, ненужных или повреждённых клеток. Ежедневно, примерно около 5% клеток организма подвергаются апоптозу, а их место занимают новые клетки. В процессе апоптоза клетка исчезает бесследно в течение 15-120 минут.
Апоптоз — это биохимически специфический тип гибели клетки, который характеризуется активацией нелизосомных эндогенных эндонуклеаз, которые расщепляют ядерную ДНК на маленькие фрагменты. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками.
Это энергозависимый процесс, посредством которого удаляются нежелательные и дефектные клетки организма. Он играет большую роль в морфогенезе и является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток, пример — опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, пример — атрофия.
Морфологические проявления апоптоза
Апоптоз имеет свои отличительные морфологические признаки, как на светооптическом, так и на ультраструктурном уровне. При окраске гематоксилином и эозином апоптоз определяется в единичных клетках или небольших группах клеток. Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз — в отличие от некроза — никогда не сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление.
Апоптоз — это механизм гибели клеток, который имеет ряд биохимических и морфологических отличий от некроза.
Наиболее четко морфологические признаки выявляются при электронной микроскопии. Для клетки, подвергающейся апоптозу характерно (рис.1):

Рис.1. Последовательность ультраструктурных изменений при апоптозе (справа) и некрозе (слева): 1 — нормальная клетка; 2 — начало апоптоза; 3 — фрагментация апоптотической клетки; 4 — фагоцитоз апоптотических телец окружающими клетками; 5 — гибель внутриклеточных структур при некрозе; 6 — разрушение клеточной мембраны.
Сжатие клетки
Клетка уменьшается в размерах; цитоплазма уплотняется; органеллы, которые выглядят относительно нормальными, располагаются более компактно.
Предполагается, что нарушение формы и объема клетки происходит в результате активации в апоптотических клетках трансглютаминазы. Этот фермент вызывает прогрессивное образование перекрестных связей в цитоплазматических белках, что приводит к формированию своеобразной оболочки под клеточной мембраной, подобно ороговевающим клеткам эпителия.
Конденсация хроматина
Это наиболее характерное проявление апоптоза. Хроматин конденсируется по периферии, под мембраной ядра, при этом образуются четко очерченные плотные массы различной формы и размеров. Ядро же может разрываться на два или несколько фрагментов.
Механизм конденсации хроматина изучен достаточно хорошо. Он обусловлен расщеплением ядерной ДНК в местах, связывающих отдельные нуклеосомы, что приводит к развитию большого количества фрагментов, в которых число пар оснований делится на 180-200. При электрофорезе фрагменты дают характерную картину лестницы. Эта картина отличается от таковой при некрозе клеток, где длина фрагментов ДНК варьирует. Фрагментация ДНК в нуклеосомах происходит под действием кальций чувствительной эндонуклеазы. Эндонуклеаза в некоторых клетках находится постоянно (например, в тимоцитах), где она активируется появлением в цитоплазме свободного кальция, а в других клетках синтезируется перед началом апоптоза. Однако еще не установлено, каким образом после расщепления ДНК эндонуклеазой происходит конденсация хроматина.
Формирование в цитоплазме полостей и апоптотических телец
В апоптотической клетке первоначально формируются глубокие впячивания поверхности с образованием полостей, что приводит к фрагментации клетки и формированию окруженных мембраной апоптотических телец, состоящих из цитоплазмы и плотно расположенных органелл, с или без фрагментов ядра.
Фагоцитоз апоптотических клеток или телец
Фагоцитоз апоптотических клеток или телец осуществляется окружающими здоровыми клетками, или паренхиматозными, или макрофагами. Апоптотические тельца быстро разрушаются в лизосомах, а окружающие клетки либо мигрируют, либо делятся, чтобы заполнить освободившееся после гибели клетки пространство.
Фагоцитоз апоптотических телец макрофагами или другими клетками активируется рецепторами на этих клетках: они захватывают и поглощают апоптотические клетки. Один из таких рецепторов на макрофагах — рецептор витронектина, который является β3-интегрином и активирует фагоцитоз апоптотических нейтрофилов.
Апоптоз принимает участие в следующих физиологических и патологических процессах:
Запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез). Несмотря на то, что при эмбриогенезе апоптоз не всегда является отражением “запрограммированной смерти клетки”, это определение апоптоза широко используют различные исследователи.
Гормон-зависимой инволюции органов у взрослых, например, отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации.
Удалении некоторых клеток при пролиферации клеточной популяции.
Гибели отдельных клеток в опухолях, в основном при ее регрессии, но также и в активно растущей опухоли.
Гибели клеток иммунной системы, как В-, так и Т-лимфоцитов, после истощения запасов цитокинов, а также гибели аутореактивных Т-клеток при развитии в тимусе.
Патологической атрофии гормон-зависимых органов, например, атрофии предстательной железы после кастрации и истощении лимфоцитов в тимусе при терапии глюкокортикоидами.
Патологической атрофии паренхиматозных органов после обтурации выводных протоков, что наблюдается в поджелудочной и слюнных железах, почках.
Гибели клеток, вызванных действием цитотоксических Т-клеток, например, при отторжении трансплантата и болезни “трансплантат против хозяина”.
Повреждении клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени, как тельца Каунсильмана.
Гибели клеток при действии различных повреждающих факторов, которые способны вызвать некроз, но действующих в небольших дозах, например, при действии высокой температуры, ионизирующего излучения, противоопухолевых препаратов.
Механизм апоптоза
TNF-α и Fas-лиганд (CD178) запускают каскад биохимических реакций, финальным этапом которых является дефрагментация хромосом и гибель клетки. На поверхности клеток организма имеются специальные рецепторы для TNF-α, это TNF-RI (с молекулярной массой 55-60 кДа) и TNF-RII (с молекулярной массой 75-80 кДа), а для Fas-лиганда рецептор Fas / APO-1 (CD95).
TNF-R и Fas / APO-1(CD95) имеют гомологию в экстрацеллюлярных доменах, представленную в виде цистеин богатых доменов и гомологичную последовательность в интрацеллюлярной части рецептора.

Рис.2. Апоптоз
Связывание TNF-α и Fas-лигандов с рецепторами апоптоза активирует интрацеллюлярные «домены смерти» (DED — death effector domain) этих рецепторов: DED, DED1 и DED2 и ряд посредников, включая церамиды, ras, SAPK / JNK, протеиновые тирозинкиназы, катепсин D и протеазы ICE / CED-3 семейства, которые каскадно проводят смертельный сигнал. Цистеиновые протеазы ICE / CED-3 семейства находятся в составе интрацеллюлярной части рецептора апоптоза в неактивной форме, они относятся к интерлейкин-lβ расщепляющим ферментам (ICE). Это семейство включает ряд различных типов протеаз, многие протеазы имеют несколько обозначений. Семейство цистеин-аспартат протеаз ещё называют каспазами.
Кроме семейства каспаз, в регуляции апоптоза принимает участие семейство Bcl-2 белков, в котором Bcl-2, Bcl-XL, Ced-9, Bcl-w, и Mcl-1 белки ингибируют апоптоз, а Bcl-2 гомологи (BH) 1-3, Bax подобный белок, Bak, Bok, и состоящие только из BH3 региона, Bad подобный белок, Bid, Bik, Bim, и Hrk выполняют проапоптозную функцию.
Активация DED, DED1 и DED2 вызывает каскадную перестройку и активацию протеаз ICE / CED-3 семейства. Первым этапом является превращение не активной про-каспазы-8 в активную каспазу-8. Каспаза-8 активирует каспазу-3 и Bid. Bid взаимодействуя с Bax способствует выходу из митохондрий цитохрома C, который активизирует каспазу-9. В свою очередь активная каспаза-9 приводит к появлению активных каспаз-3, — 6, — 7. В свою очередь активные ICE начинают взаимодействовать с рядом внутриклеточных субстратов: поли-(АДФ-рибозо) полимеразой (PARP), участвующей в репарации ДНК и модификации активности некоторых ядерных белков, ламином В1, топоизомеразой I и Р-актином. Все члены семейства ICE / CED-3 протеаз содержат каталитический остаток цистеина и расщепляют субстраты после аспарагиновой кислоты. Специфическое расщепление PARP, ламина В1, топоизомеразы I и Р-актина под действием ICE-подобных протеаз на большие и малые фрагменты приводит клетку к гибели, так как большие фрагменты этих субстратов и являются активными нуклеазами, которые разрезают хромосомы на фрагменты. Например, PARP расщепляется CPP32 / Yama на два фрагмента 85 и 24 кДа, из которых апоптоз-специфическим является фрагмент 85 кДа. Активация протеаз ICE / CED-3 семейства может происходить и под действием фосфолипидов, например, церамидов, которые способны активировать CPP32 / Yama.
Свободный сфингозин образуемый из церамидов в результате его гидролиза церамидазой так же активирует ICE-подобные протеазы и ускоряет апоптоз.

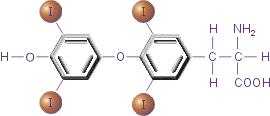
Рис.3. Тироксин
Важная роль в осуществлении апоптоза принадлежит тироксину (Т4).
Он регулирует функционирование протеиновой тирозинкиназы, важного элемента реализации сигнала смерти. При недостатке этого гормона щитовидной железы происходит подавление апоптоза.
IL-lβ блокирует апоптоз. ICE-подобные протеазы взаимодействуют с IL-lβ, а не с PARP, ламином В1, топоизомеразой I и Р-актином. В результате чего не происходит образования активных нуклеаз, и клетка избегает апоптоза.
На взаимодействие TNF-α и Fas-лигандов с TNF-R и Fas / APO-1(CD95) и проведение апоптотического сигнала оказывают влияние Bcl и Bax белки. Так белки Bcl семейства: Bcl-2, Bcl-xL и Bcl-xS блокируют выход цитохрома С из митохондрий и таким образом предотвращают превращение про-каспазы-9 в активную форму, отменяют атоптотический сигнал. В свою очередь Bax белки способствуют выходу цитохрома С из митохондрий и образованию активной каспазы-9, которая инициирует продолжение и активацию апоптотическог каскада, начавшегося с присоединения TNF-α или Fas-лигандов к TNF-R и Fas / APO-1(CD95). Быть или не быть апоптозу зависит от соотношения Bcl и Bax белков в митохондриях. Преобладание экспрессии белков Bcl семейства блокирует запуск апоптоза, а преобладание экспрессии Bax белков способствует реализации сигнала смерти.
Регуляция апоптоза
Апоптоз — это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза. Многие из этих генов сохранились в ходе эволюции — от круглых червей до насекомых и млекопитающих. Некоторые из них обнаруживаются также в геноме вирусов. Таким образом, основные биохимические процессы апоптоза в разных экспериментальных системах (исследования ведутся на круглых червях и мухах) являются идентичными, поэтому результаты исследований можно прямо переносить на другие системы (например, организм человека).
Апоптоз может регулироваться:
внешними факторами,
автономными механизмами.
Воздействие внешних факторов
Апоптоз может регулироваться действием многих внешних факторов, которые ведут к повреждению ДНК. При невосстановимом повреждении ДНК путем апоптоза происходит элиминация потенциально опасных для организма клеток. В данном процессе большую роль играет ген супрессии опухолей р53. К активации апоптоза также приводят вирусные инфекции, нарушение регуляции клеточного роста, повреждение клетки и потеря контакта с окружающими или основным веществом ткани. Апоптоз — это защита организма от персистенции поврежденных клеток, которые могут оказаться потенциально опасными для многоклеточного организма.
При стимуляции тканей каким-либо митогеном ее клетки переходят в состояние повышенной митотической активности, которая обязательно сопровождается некоторой активацией апоптоза. Судьба дочерних клеток (выживут они или подвергнутся апоптозу) зависит от соотношения активаторов и ингибиторов апоптоза:
ингибиторы включают факторы роста, клеточный матрикс, половые стероиды, некоторые вирусные белки;
активаторы включают недостаток факторов роста, потерю связи с матриксом, глюкокортикоиды, некоторые вирусы, свободные радикалы, ионизирующую радиацию.
При воздействии активаторов или отсутствии ингибиторов происходит активация эндогенных протеаз и эндонуклеаз. Это приводит к разрушению цитоскелета, фрагментации ДНК и нарушению функционирования митохондрий. Клетка сморщивается, но клеточная мембрана остается интактной, однако повреждение ее приводит к активации фагоцитоза. Погибшие клетки распадаются на небольшие, окруженные мембраной, фрагменты, которые обозначаются как апоптотические тельца. Воспалительная реакция на апоптотические клетки не возникает.
Автономный механизм апоптоза
При развитии эмбриона различают три категории автономного апоптоза: морфогенетический, гистогенетический и филогенетический.
Морфогенетический апоптоз участвует в разрушении различных тканевых зачатков. Примерами являются:
разрушение клеток в межпальцевых промежутках;
гибель клеток приводит к разрушению избыточного эпителия при слиянии небных отростков, когда формируется твердое небо.
гибель клеток в дорсальной части нервной трубки во время смыкания, что необходимо для достижения единства эпителия двух сторон нервной трубки и связанной с ними мезодермы.
Гистогенетический апоптоз наблюдается при дифференцировке тканей и органов, что наблюдается, например, при гормональнозависимой дифференцировке половых органов из тканевых зачатков. Так, у мужчин клетками Сертоли в яичках плода синтезируется гормон, который вызывает регрессию протоков Мюллера (из которых у женщин формируются маточные трубы, матка и верхняя часть влагалища) путем апоптоза.
Филогенетический апоптоз участвует в удалении рудиментарных структур у эмбриона, например, пронефроса.
При различных состояниях может наблюдаться как ускорение, так и замедление апоптоза. Несмотря на то, что апоптоз могут активировать различные факторы, характерные для определенных типов клеток, однако конечный путь апоптоза регулируется точно установленными генами и является общим, независимо от причины активации апоптоза.
Все факторы, усиливающие или ослабляющие апоптоз, могут действовать прямо на механизм гибели клетки или опосредованно, путем влияния на регуляцию транскрипции.
В некоторых случаях влияние этих факторов на апоптоз является решающим (например, при глюкокортикоид-зависимом апоптозе тимоцитов), а в других не имеет особой важности (например, при Fas — и TNF-зависимом апоптозе). В процессе регуляции принимает участие большое количество веществ. Наиболее изученными из них являются вещества из семейства bcl-2.
Bcl-2 ген впервые был описан как ген, который транслоцируется в клетках фолликулярной лимфомы и ингибирует апоптоз. При дальнейших исследованиях оказалось, что Bcl-2 является мультигеном, который обнаруживается даже у круглых червей. Гомологичные гены были также обнаружены в некоторых вирусах. Все вещества, относящиеся к данному классу делятся на активаторы и ингибиторы апоптоза.
К ингибиторам относятся: bcl-2, bcl-xL, Mcl-1, bcl-w, аденовирусный E1B 19K, Эпштейн-Барр-вирусный BHRF1.
К активаторам относятся bax, bak, Nbk / Bik1, Bad, bcl-xS.
Члены этого семейства взаимодействуют друг с другом. Одним из уровней регуляции апоптоза является взаимодействие белок-белок. Белки семейства bcl-2 формируют как гомо — так и гетеродимеры. Например, bcl-2-ингибиторы могут образовать димеры bcl-2-активаторами. Таким образом, жизнеспособность клеток зависит от соотношения активаторов и ингибиторов апоптоза. Например, bcl-2 взаимодействует с bax; при преобладании первого жизнеспособность клетки повышается, при избытке второго — уменьшается. К тому же белки семейства bcl-2 могут взаимодействовать с белками, не относящимися к этой системе. Например, bcl-2 может соединятся с R-ras, который активирует апоптоз. Другой белок, Bag-1, усиливает способность bcl-2 ингибировать апоптоз.
В настоящее время принято считать, что гены, участвующие в регуляции роста и развития опухолей (онкогены и гены-супрессоры опухолей), играют регулирующую роль в индукции апоптоза. К ним относятся:
bcl-2 онкоген, который ингибирует апоптоз, вызванный гормонами и цитокинами, что приводит к повышению жизнеспособности клетки;
Белок bax (также из семейства bcl-2) формирует димеры bax-bax, которые усиливают действие активаторов апоптоза. Отношение bcl-2 и bax определяет чувствительность клеток к апоптотическим факторам и является “молекулярным переключателем”, который определяет, будет ли происходить рост или атрофия ткани.
c-myc онкоген, чей белковый продукт может стимулировать либо апоптоз, либо рост клеток (при наличии других сигналов выживания, например, bcl-2)
Ген р53, который в норме активирует апоптоз, но при мутации или отсутствии (что обнаружено в некоторых опухолях) повышает выживаемость клеток. Установлено, что р53 необходим для апоптоза при повреждении клетки ионизирующим излучением, однако при апоптозе, вызванном глюкокортикоидами и при старении, он не требуется.
Снижение апоптоза
Продукт р53 гена следит за целостностью генома при митозе. При нарушении целостности генома клетка переключается на апоптоз. Наоборот, белок bcl-2 ингибирует апоптоз. Таким образом, недостаток р53 или избыток bcl-2 приводит к накоплению клеток: эти нарушения наблюдаются в различных опухолях. Изучение факторов регулирующих апоптоз имеет важное значение в разработке лекарственных препаратов, усиливающих гибель клеток злокачественных новообразований.
Аутоиммунные заболевания могут отражать нарушения в индукции апоптоза лимфоидных клеток, способных реагировать с собственными антигенами. Например, при системной красной волчанке наблюдается нарушение Fas-рецепторов на клеточной поверхности лимфоцитов, что ведет к активации апоптоза. Некоторые вирусы повышают свою выживаемость путем ингибирования апоптоза инфицированных клеток, например, вирус Эпштейна-Барра может воздействовать на обмен bcl-2.
Ускорение апоптоза
Ускорение апоптоза доказано при синдроме приобретенного иммунодефицита (СПИД), нейротрофических заболеваниях и некоторых заболеваниях крови, при которых наблюдается дефицит каких-либо форменных элементов. При СПИДе вирус иммунодефицита может активировать CD4 рецептор на неинфицированных Т-лимфоцитах, ускоряя, таким образом, апоптоз, что приводит к истощению клеток данного типа.
Значение апоптоза в развитии организма и патологических процесса
Апоптоз играет важную роль в развитии млекопитающих и в различных патологических процессах. Функционирование bcl-2 требуется для поддержания жизнеспособности лимфоцитов, меланоцитов, эпителия кишечника и клеток почек во время развития эмбриона. bcl-x необходим для ингибирования смерти клеток в эмбриогенезе, особенно в нервной системе. Bax необходим для апоптоза тимоцитов и поддержания жизнеспособности сперматозоидов во время их развития. р53 является геном супрессии опухолей, поэтому в эмбриогенезе особой роли не играет, но обязательно необходим для супрессии опухолевого роста. Мыши, у которых отсутствовали оба р53 гена, проявляли чрезвычайно высокую склонность к развитию злокачественных опухолей в результате полного или частичного нарушения апоптоза предопухолевых клеток. Усиленный синтез белка, кодируемого bcl-2 геном, приводит к подавлению апоптоза и, соответственно, развитию опухолей; данный феномен обнаружен в клетках В-клеточной фолликулярной лимфомы.
При лимфопролиферативных заболеваниях и похожей на системную красную волчанку болезни у мышей наблюдается нарушение функции Fas-лиганда или Fas-рецептора. Повышенный синтез Fas-лиганда может предупреждать отторжение трансплантата. Апоптоз является частью патологического процесса при инфицировании клетки аденовирусами, бакуловирусами, ВИЧ и вирусами гриппа. Ингибирование апоптоза наблюдается при персистировании инфекции, в латентном периоде, а при усиленной репликации аденовирусов, бакуловирусов, возможно герпесвирусов, вируса Эпштейн-Барра и ВИЧ наблюдается активация апоптоза, что способствует широкому распространению вируса. При нейродистрофических заболеваниях отмечается нарушение функции гена (iap-гена), сходного с ингибитором апоптоза бакуловирусов.
Список литературы
1. Белозеров Е.С., Мешкевич В.С. Клиническая иммунология-Изд-во «Альмар», 2006 г.
2. Гордеева А.В., Лабас Ю.А., Звягильская Р.А. Апоптоз одноклеточных организмов: механизмы и эволюция // Биохимия, 2009, том 69, вып. 10, с. 1301–1313 pdf html
3. Галицкий В.А. Возникновение эукариотических клеток и происхождение апоптоза // Цитология, 2008, том 47, вып. 2, с. 103–120
4. Клиническая иммунология / Под ред. Караулова А.В. М-2005 г.
5. Митин А.А. Клиническая иммунология – СПб, 2008 г.
Источник: StudFiles.net