Способность к фагоцитозу
Фагоцитоз – одно из самых блестящих открытий патофизиологии XIX века. И. И. Мечников описал фагоцитоз в 1883 г. как общебиологическое явление в жизнедеятельности одноклеточных и многоклеточных организмов, состоящее в поглощении клетками других клеток и твердых частиц. В настоящее время под фагоцитозом понимают захват клеткой путем рецепторного эндоцитоза при участии микрофиламентов объектов с диаметром более 1 мкм.
Таким образом, фагоцитоз – частный случай рецепторного эндоцитоза. Последний может проявляться и в иных формах – трансцитоза, адсорбтивного и жидкофазного пиноцитоза. Пиноцитоз не требует участия микрофиламентов, менее энергоемок и пригоден лишь для захвата меньших по размеру объектов.
Таблица 8
Иммуноглобулиноподобные молекулы клеточной адгезии
| Ig-подобный белок | Источник | Лиганды | Функции |
| ICAM-1 | Активированные эндотелий, лейкоциты, тромбоциты, эпителий тимуса. | LFA-1, CR3, риновирусы, малярийный плазмодий. | Опосредует адгезию активированных лейкоцитов, тромбоцитов и эндотелия. |
| ICAM-2 | Эндотелий. | LFA-1. | Опосредует физиологическую эмиграцию лейкоцитов. |
| ICAM-3 | Все лейкоциты в покое. | LFA-1. | Межлейкоцитарная кооперация. |
| VCAM | Активированный эндотелий и дендритические клетки. | VLA-4. | Хоуминг в пейеровых бляшках и фиксация В-лимфоцитов в герминативных центрах, транспорт лимфоцитов за гематоэнцефалический барьер. |
| CD2 | Т-лимфоциты и НК-клетки. | CD58. | Кооперация клеток при презентации антигенов, передает митогенный сигнал. |
| CD58 (LFA-3) | Большинство клеток, в том числе все клетки гемопоэтического ряда, иммунокомпетентные и антигенпредставляющие. | CD2. | Кооперация клеток при презентации антигенов, прикрепление киллеров к мишеням. |
У одноклеточных и низших многоклеточных фагоцитоз служит способом питания и защиты.
появлением в филогенезе мезодермы функции защиты переходят к ее производным. У высших животных фагоцитоз – не только способ защиты против экзогенных агрессоров, но и один из механизмов устранения собственных состарившихся клеток и апоптотических телец в ходе запрограммированной клеточной гибели на протяжении морфогенеза. Фагоцитоз обеспечивает развитие преиммунного и иммунного ответов, устраняет из кровотока иммунные комплексы, предупреждая иммунокомплексные болезни, утилизирует материал тромбов при тромболизисе и участвует в рассасывании рубцов, устранении микроэмболов и патологических продуктов обмена при тезаурисмозах. В ходе фагоцитоза его исполнителями реализуется сложный комплекс защитно-приспособительных механизмов, которые включают не только цитотоксическое или бактерицидное действие на объект фагоцитоза, но и секрецию медиаторов воспаления (экзоцитоз), активацию энергетического метаболизма фагоцита (дыхательная вспышка), процессинг антигенов и их представление лимфоцитам.
Подчеркивая важную роль фагоцитов при воспалении, Мечников говорил: «Нет воспаления без фагоцитоза». Патофизиология оценивает справедливость мечниковских слов, но это отнюдь не значит, что фагоцитоз не оказывает, наряду с саногенным, и патогенного действия.
Участники фагоцитоза – фагоциты. Мечников выделял макрофаги и микрофаги, впоследствии было установлено, что первые – это моноциты и их потомки. К последним Мечников причислил гранулоциты.
Сейчас говорят о системе мононуклеарных фагоцитов (состав которой приведен выше) и о полиморфонуклеарных фагоцитах, представленных, в основном, нейтрофилами. Способность к фагоцитозу присуща также эозинофилам и базофилам, но для них этот вид деятельности не является основным. В фагоцитозе, определенно, могут участвовать и тромбоциты, причем эта их функция сильно стимулируется a-фетопротеином. По некоторым данным, фагоцитировать способны и некоторые пролимфоциты, но зрелые лимфоидные клетки фагоцитами не являются. Эпизодически фагоцитируют даже клетки, не относящиеся к системе крови, например, нервные и эпителиальные, не являющиеся профессиональными фагоцитами.
Нейтрофил – короткоживущая клетка. В крови он находится, в среднем, 12-14 ч, а в тканях – не более 2-4 суток. При воспалениях нейтрофилы играют ту же роль, что ручные гранаты при боевых действиях: это фагоциты одноразового использования, которые обязательно гибнут при фагоцитозе, «разбрасывая» вокруг своего рода осколки – бактерицидные и цитотоксические факторы и медиаторы воспаления, в том числе и нейтрофильный хемотаксический фактор, привлекающий макрофаги, гранулоцитарный колониестимулирующий фактор, способствующий восполнению их пула и нейтрофильный пироген, вносящий некоторый вклад в стимуляцию преиммунного ответа организма.
Гибель нейтрофилов при воспалении связана не столько с кознями микробов, сколько с тем, что они не выдерживают собственного мощного окислительного удара, наносимого по флогогенным агентам системой продукции активных кислородных радикалов.
Не участвующие в воспалении нейтрофилы претерпевают апоптоз или экспрессируют антиген стареющих клеток и фагоцитируются макрофагами («экспроприация экспроприаторов»!). Остатки нейтрофилов и макрофагов, а также поврежденные клетки и микроорганизмы формируют гной. При нейтрофильном экссудате гной особенно богат миелопероксидазой, придающей ему зеленоватый цвет. Макрофаги лишены миелопероксидазы и формируют гной иного оттенка. Компоненты бактерий, например, синегнойной палочки, могут придавать гною особые, специфические цвет и другие свойства. Гной всегда проявляет гидролитическую активность и может участвовать в распространении воспаления и инфекции, что привело медицину к постулату «Ubi pus – ibi evacua».
Нейтрофилы отличаются менее широким репертуаром фагоцитируемых объектов, чем макрофаги. Последние принципиально способны фагоцитировать практически все объекты, доступные нейтрофилам (например, кокки и грибки), а также многие другие, не фагоцитируемые гранулоцитами. Так, фагоцитоз опухолевых клеток, а также клеток, зараженных вирусами и персистирующими интрацеллюлярными патогенами, является исключительно макрофагальным.
В то же время, в фагоцитозе стафилококков, стрептококков, включая пневмококки, диплококков и многих других возбудителей, условно обозначаемых как «гноеродная флора», роль нейтрофилов является решающей. Отчасти, именно поэтому скарлатина, гоноррея и менингококковая инфекция, например, сопровождаются нейтрофильным, а коклюш, паротит и мононуклеоз – моноцитарно-лимфоцитарным лейкоцитозом в крови и соответствующим составом экссудатов.
Система мононуклеарных фагоцитов представлена как профессиональными фагоцитами, так и антиген-представляющими клетками различной локализации. Это, прежде всего, монобласты и промоноциты, моноциты и макрофаги костного мозга, пролиферация и дифференцировка которых находятся под влиянием ряда последовательно действующих цитокинов (плюрипотентного ростового фактора, ИЛ-6, ИЛ-1, ИЛ-3, GM-CSM), моноциты периферической крови, проводящие в ней, в среднем, 1-2 дня и покидающие кровеносное русло через высокоэндотелиальные венулы и синусоиды. В тканях моноциты превращаются в альвеолярные макрофаги легких, плевральные, перикардиальные, суставные и перитонеальные макрофаги серозных полостей, селезеночные макрофаги, клетки Купфера в печени, макрофаги лимфоузлов, микроглию головного мозга, остеокласты костей, гистиоциты соединительной ткани, мезангиальные макрофаги клубочков почек, эпителиоидные клетки. Фагоцитирующие макрофаги особенно активны при метаболическом взрыве и экзоцитозе медиаторов воспаления. Близкие к ним, но обособленные в функциональном и антигенном отношении антиген-представляющие макрофагальные клетки – это клетки Лангерганса в коже, интердигитирующие клетки тимуса и лимфоузлов, фолликулярные дендритические клетки герминативных центров. Помимо фагоцитоза, они специализированы на взаимодействии с лимфоцитами, обладают экспрессией белков ГКГС не только первого, но и второго класса, осуществляют процессинг антигенов и их презентацию и выделяют клеточно-специфические хемоаттрактивные пептиды.
В тканях как при воспалении, так и в норме, макрофаги представляют собой долгоживущие элементы и их участие в фагоцитозе и воспалении многократно. Более того, на протяжении воспаления макрофаг, по-видимому, в пределах своей специализации может менять спектр вырабатываемых медиаторов воспаления и влиять на его ход, не только управляя процессами альтерации и экссудации, но и оперируя противовоспалительными сигналами, участвуя в контроле и исполнении пролиферации и репаративного процесса в целом. Репертуар объектов фагоцитоза у макрофагов очень широк. Уже отмечалось, что такие объекты, как клетки, пораженные микобактериями, бруцеллами, риккетсиями, сальмонеллами, токсоплазмами и листериями, иммунные комплексы, стареющие и снабженные неоантигенами собственные клетки, мишени аутоиммунных процессов, практически подлежат только макрофагальному фагоцитозу. Макрофаги не только выделяют, но и синтезируют заново медиаторы воспаления, принадлежащие ко всем химическим группам.
Это важные источники арахидоновых производных и АКР, причем они обладают значительным антиоксидантным потенциалом и, как правило, выживают при нанесении окислительного удара по микробам и другим мишеням фагоцитоза. В отличие от нейтрофилов и моноцитов крови, обладающих миелопероксидазой и генерирующих гипохлорит, зрелые тканевые макрофаги не содержат данного фермента, поэтому спектр вырабатываемых ими АКР богат перекисью водорода и гидроксильными радикалами, но не включает этот «естественный отбеливатель».
о может способствовать их выживанию при фагоцитозе. Мононуклеары способны вырабатывать биогенные амины и многие медиаторы, присущие нейтрофилам (гидролазы, лизоцим). Макрофаги синтезируют компоненты сторожевой полисистемы плазмы крови (включая факторы комплемента, факторы свертывания, предшественники кининов и активатор фибринолиза плазминоген). В отличие от нейтрофилов, они выделяют транспортные белки (трансферрин, транскобаламин, апопротеины липопротеидов), фибронектин, противовоспалительные антиоксиданты и ингибиторы протеаз (a2-макроглобулин, С-реактивный белок, a1-антитрипсин и другие положительные глобулины острой фазы плазмин). ИЛ-1, кахексин и a-интерферон также являются макрофагальными продуктами. Это делает исключительной роль макрофагального фагоцитоза как процесса, обеспечивающего с помощью этих цитокинов стартовые сигналы для преиммунного ответа – системного коррелята воспаления. Продромальный синдром, включая лихорадку, распространенное повышение адгезивных свойств эндотелия, гипоферремию, ускорение СОЭ и типовой сдвиг белковых фракций в плазме крови, обеспечивается, в основном, макрофагальными цитокинами. Истощение при хронических воспалениях и опухолевых процессах опосредуется действием кахексина, значительная часть которого производится тоже активированными макрофагами.
Лейкоцитоз при воспалениях стимулируется не только нейтрофилами, но и макрофагальными колониестимулирующими факторами. Макрофаги и, в еще большей степени, близкие к ним антигенпредставляющие клетки, выделяют хемоаттрактанты и ингибиторы миграции для лимфоцитов и гранулоцитов, участвующих в рекрутировании клеток в состав экссудатов и гранулём. Мононуклеарные фагоциты – мощный источник стимуляторов пролиферации и биосинтетической деятельности фибробластов (фактор роста, фактор ангиогенеза). Они могут и тормозить размножение клеток (опухолевых, некоторых бактериальных, например, туберкулезных и листериозных; а также лимфоидных). Доказано, что макрофаги, в отличие от гранулоцитов, сами могут пролиферировать в очагах воспаления, хотя их тканевой пул пополняется, по большей части, иммиграцией. Таким образом, роль макрофагов, по сравнению с другими фагоцитами, становится особенно важной при хроническом воспалении.
Наследственные и приобретенные нарушения в работе фагоцитов тяжело отражаются на ходе воспаления и снижают его защитную эффективность.
Источник: helpiks.org
Моноциты
Моноциты – одно их первых названий, которые всплывают  в памяти при упоминании о фагоцитозе. Эти осуществляющие фагоцитоз лейкоциты непрерывно перемещаются в крови, «сканируя» окружающее пространство на предмет наличия в нем вредоносных объектов. Найдя «обидчика», они захватывают и уничтожают его. После этого, избавившись от продуктов расщепления бактерии, микропаразита или вируса, они продолжают свою работу в аналогичном направлении.
в памяти при упоминании о фагоцитозе. Эти осуществляющие фагоцитоз лейкоциты непрерывно перемещаются в крови, «сканируя» окружающее пространство на предмет наличия в нем вредоносных объектов. Найдя «обидчика», они захватывают и уничтожают его. После этого, избавившись от продуктов расщепления бактерии, микропаразита или вируса, они продолжают свою работу в аналогичном направлении.
При фагоцитозе моноцит справляется с вредными объектами всего за 9 минут. Иногда он поглощает и расщепляет клетки и субстраты, превышающие его по размерам в несколько раз.
Нейтрофилы
Фагоцитоз нейтрофилов осуществляется похожим образом, с той лишь разницей, что они работают по принципу «Светя другим, сгораю сам». Это значит, что, захватив патоген и уничтожив его, нейтрофил погибает.
Макрофаги
Макрофаги – это осуществляющие фагоцитоз лейкоциты, образовавшиеся из моноцитов крови. Они располагаются в тканях: как непосредственно под кожей и слизистыми, так и в глубине органов. Существуют особые разновидности макрофагов, которые находятся в конкретных органах.
Например, в печени «живут» клетки Купфера, задача которых состоит в разрушении старых компонентов крови. В легких располагаются альвеолярные макрофаги. Эти клетки, способные к фагоцитозу, захватывают вредные частицы, проникшие в легкие с вдыхаемым воздухом, и переваривают их, разрушая своими ферментами: протеазами, лизоцимом, гидролазами, нуклеазами и т.д.
Обычные тканевые макрофаги обычно погибают после встречи с патогенами, то есть в этом случае происходит то же, что и при фагоцитозе нейтрофилов.
 Дендритные клетки
Дендритные клетки
Эти клетки – угловатые, ветвистые – совершенно не похожи на макрофаги. Тем не менее, они являются их родственниками, так как тоже образуются из моноцитов крови. К фагоцитозу способны только молодые дендритные клетки, остальные в основном «работают» с лимфоидной тканью, обучая лимфоциты правильно реагировать на некоторые антигены.
Тучные клетки
Помимо того, что тучные клетки запускают реакцию воспаления, эти лейкоциты способны к фагоцитозу. Особенность их работы состоит в том, что они уничтожают только грамотрицательные бактерии. Причины такой «разборчивости» не совсем понятны, видимо, у тучных клеток есть к этим бактериям особое сродство.
Они могут уничтожить сальмонеллу, кишечную палочку, спирохету, многих возбудителей ЗППП, но совершенно равнодушно воспримут возбудителя сибирской язвы, стрептококка и стафилококка. Борьбой с ними займутся другие лейкоциты.
Перечисленные выше клетки – это профессиональные фагоциты, об «опасных» свойствах которых известно всем. А теперь несколько слов о тех клетках, для которых фагоцитоз – не самая типичная функция.
Тромбоциты
Тромбоциты, или кровяные пластинки, занимаются главным образом тем, что отвечают за свертываемость крови, прекращают кровотечения, формируют тромбы. Но, помимо этого, у них обнаружены и фагоцитарные свойства. Тромбоциты могут образовывать ложноножки и уничтожать некоторые вредные компоненты, попавшие в организм.
Клетки эндотелия
Оказывается, клеточная выстилка сосудов тоже представляет  опасность для бактерий и прочих «захватчиков», проникших в организм. В крови с чужеродными объектами борются моноциты и нейтрофилы, в тканях их поджидают макрофаги и другие фагоциты, и даже в стенках сосудов, находясь между кровью и тканями, «враги» не могут «чувствовать себя в безопасности». Воистину, возможности защиты организма чрезвычайно велики. При увеличении содержания в крови и тканях гистамина, что происходит при воспалении, фагоцитирующая способность клеток эндотелия, почти незаметная до этого, возрастает в несколько раз!
опасность для бактерий и прочих «захватчиков», проникших в организм. В крови с чужеродными объектами борются моноциты и нейтрофилы, в тканях их поджидают макрофаги и другие фагоциты, и даже в стенках сосудов, находясь между кровью и тканями, «враги» не могут «чувствовать себя в безопасности». Воистину, возможности защиты организма чрезвычайно велики. При увеличении содержания в крови и тканях гистамина, что происходит при воспалении, фагоцитирующая способность клеток эндотелия, почти незаметная до этого, возрастает в несколько раз!
Гистиоциты
Под этим собирательным названием объединяют все клетки тканей: соединительной ткани, кожи, подкожной клетчатки, паренхимы органов и так далее. Раньше этого никто не мог предположить, но оказывается, при определенных условиях многие гистиоциты способны менять свои «жизненные приоритеты» и тоже приобретать способность к фагоцитозу! Повреждения, воспаление и другие патологические процессы пробуждают в них эту способность, которая в норме отсутствует.
Источник: www.transferfaktory.ru
Что же такое фагоцитоз?
В биологии есть термин «эндоцитоз». Процесс поглощения клеткой частицы, молекулы, другой клетки или бактерии. Если поглощается большая и твердая частица, то эндоцитоз и называют фагоцитозом.
Макрофаг vs микроб. Кто такой макрофаг?
Мир в котором мы живем — довольно грязное место. Так как и все в природе стремится к хаосу, так и в нашей жизни все стремится замусориться. Нужно постоянно следить за тем, чтобы в нашем доме всегда все было чисто и вещи лежали на своем месте.
Подобная ситуация происходит и в нашем теле. Постоянно присходит рождение и гибель новых клеток, каждый день и час в нашем организме в одной из клеток происходит генетический сбой — она становится раковой. В кишечнике проживают бактерии, постоянно проникающие в печень по воротной вене. Вирусы, бактерии, простейшие, старающиеся превратить наше тело в питательную среду…
Наша иммунная система работает постоянно, постоянно поддерживая порядок. Неотъемлемая часть этой системы — макрофаг.
Это амебоподобный организм (как слизеподобный добряк в «Охотниках за приведениями»). Задача макрофага — очистить организм от микроскопического мусора и бактерий. Родина макрофагов — костный мозг, предшественник — белая кровяная клетка — моноцит.
Живут макрофаги около полутора месяцев, в течение этого времени они патрулируют организм (в анализе крови смотрим сегментоядерные нейтрофилы, попадая в ткани, они становятся макрофагами).
Макрофаг — это большая лейкоцитарная клетка, которая является важной частью нашей иммунной системы. Слово «макрофаг» буквально означает «большой пожиратель».
Это амебоподобный организм, и его задача — очистить наш организм от микроскопических мусора и захватчиков. Макрофаг обладает способностью находить и «съедать» частицы, такие как бактерии, вирусы, грибы и паразиты.
Еще один увлекательный аспект макрофага — знать, какие клетки уничтожать, а какие оставить в покое. Здоровые клетки организма имеют рецепторы, которые дают сигнал «не ешь меня». Лимфоциты хелперы (помощники) вырабатывают антитела, которые фиксируются на возбудителе. Это уже другой сигнал для макрофага: «сьешь меня».
Этапы фагоцитоза
Рассмотрим этот процесс на примере лейкоцитов (нейтрофилы — самые многочисленные из них), как клеток иммунной системы, поглощающих вредоносную бактерию. Ну, во-первых, лейкоцит должен четко понимать, что перед ним чужеродный организм. Процесс распознавания довольно сложен.
Иммунная клетка определяет высвобождаемые бактерией молекулы как сигнал к действию. Затем лейкоцит должен зацепиться, прилипнуть к бактерии. Для этого на его поверхности есть специальные рецепторы, при помощи которых происходит прилипание к чужеродной клетке (это может быть не только бактерия, но и своя клетка, которая не отвечает на команды — например раковая).
После прилипания мембрана разбухает наружу и как бы обволакивает бактериальную клетку. В результате, непрошенный гость оказывается как бы в мыльном пузыре — фагосоме.
Внутрь фагосомы клетка-фагоцит выделяет ферменты, которые разружают клеточную стенку бактерии, разрушая ее.

Рассмотрим по порядку.
1. Хемотаксис. А нюх как у собаки… Как макрофаг находит чужеродный объект? Неужели нужно все клетки (как человек по комнате, ночью, на ощупь) нужно «потрогать» рецепторами?
Нет. Хемотаксис — это направленное движение относительно объекта, в зависимости от химических веществ, которые выделяет этот самый объект. Про отрицательный гемотаксис написано было еще в учебнике зоологии: бросался кристаллик соли в воду и амеба старалась уползти от такого соседства подальше. С макрофагами хемотаксис положительный. Ползет, реагируя на химические вещества, выделяемые чужеродными организмами. Привлекают также вещества — цитокины, выделяемые своими же клетками: зовут подомогу. Туберкулезная палочка, к примеру, токсинов не выделяет («не пахнет»), поэтому иммунная система выявляет их не сразу.
Первыми в очаг воспаления мигрируют нейтрофилы из крови, существенно позже поступает «большой пожиратель». По скорости хемотаксиса эти клетки идентичны, но макрофаги активируются заметно позднее.
2. Адгезия макрофагов к объекту. Или «прилипание». На поверхности как здоровых, так и патологических клеток и микробов есть определенный набор химических молекул, которые сигнализируют макрофагу: «съешь меня» или «не ешь меня».
Распознавание осуществляется специальными рецепторами. И хотя макрофаги способны фагоцитировать неживые клетки (кусочки угля, асбеста, стекла), фагоцитарный процесс активируется после команды других клеток — Т-хелперов.
Именно Т-хелперы (вид лимфоцитов) «подсвечивают» то, что нужно скушать: на «неподготовленный» объект налипают специфические белки — опсонины. На «запах» опсонинов и идет макрофаг.
3. В том месте, где произошел контакт с микробом, активируется мембрана клетки. Она как бы вминается внутрь.
4. Формирование фагосомы. Фагосома — это полость, в котором оказывается объект поглощения. Своеобразный «желудок», в котором под действием ферментов происходит расщепление чужеродного организма.
В лизисе (расщеплении) учавствует перекись водорода (прекращайте постоянно лить на рану перекись, таким образом повреждаются и здоровые клетки!), закись азота, лизоцим. Различного рода ферменты — протеазы, липазы.
Самый ударный фермент лизосом — эластаза.
5. Выброс перевариваемых остатков.
Profit! Go to step №1!
Это в идеальных условиях. В реальности все происходит намного интереснее. Сам механизм иммунного ответа макроорганизма (нас с вами) и микро- (все то живое, что можно увидеть в микроскоп) — это результат гонки вооружений, продолжающейся миллионы лет.
перемирия в этом противостоянии не планируется и договора по ограничению оружия никто подписывать не станет. Кто кого перехитрит.
Задача микроба: внедриться, размножиться и распространиться. А эволюция постаралась, чтобы было чем эти планы реализовывать. Поэтому как со стороны микро- и макроорганизма накопился богатый арсенал приспособлнений.
Есть возбудители (такие как микобактерия туберкулеза или гонококк), для которых быть проглоченным макрофагом — это неотъемлемый этап развития.
А где лучше всего спрятаться от имунной системы? Конечно внутри представителя этой имунной системы!
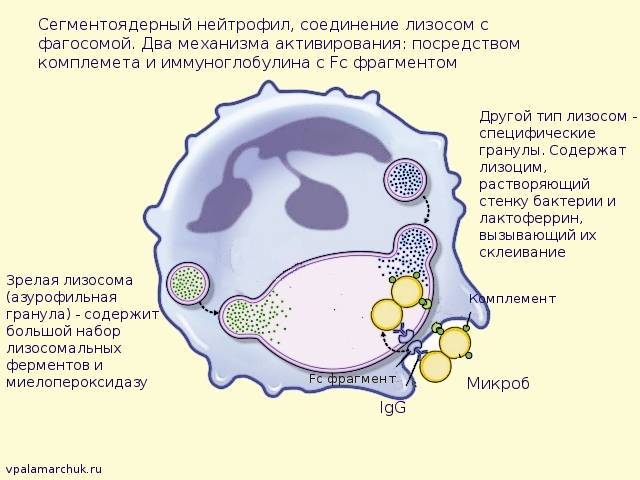
Когда не все так просто: незавершенный фагоцитоз
Есть микроорганизмы, для которых нападение на них макрофагов не является какой-то проблемой. Даже напротив — это для них важный этап в развитии. Как уже говорилось, макрофаг поглощает микроб, формируя фагосому. А вот тут и происходит сбой. Ферменты, учавствующие в расщеплении всего, что поглотил макрофаг, концентрируются в другом «мыльном пузыре» — лизосоме.

В норме лизосома сливается с фагосомой. В фагосоме создается кислая среда, снижается pH. В кислой среде начинают действовать ферменты, расщепляющие бактерию.
А вот листерия, к примеру выделяет вещества, препятствующие присоединению липосомы (содежащей ферменты) с фагосомой. Блокада фагосомно-лизосомального слияния также характерна для вируса гриппа и токсоплазм. Не может макрофаг «переварить» и возбудителя гонококковой инфекции. Гонококк (стафилококки, кстати, тоже) довольно устойчив к лизосомальным ферментам. А риккетсии разрушают фагосому и могут свободно плавать с цитоплазме фагоцита.
Как же можно справиться с тем, что не получается переварить и уничтожить?
Прежде чем продолжить рассказ, стоит поговорить о том, как сам механизм фагоцитоза изучался. Точнее от том, благодаря кому. Диктиостеллиум.
Именно этому микроорганизму принадлежит самая главная роль в исследовании фагоцитоза. Клеточный слизевик. Хотел написать, что это одноклеточный организм, но это не совсем так… Но и не многоклеточный тоже.
Этот амебоподобный организм был описан в 1935 году. В связи с тем, что очень легко выращивается в лаборатории, стал самым изучаемым микроорганизмом. Механизм фагоцитоза очень древний, у слизевика и у наших с вами макрофагов он очень схож. Обитает во влажном листовом опаде, питается слизевик бактериями. Еще уникальная особенность — у диктиостелиума три «пола», причем для полового размножения достаточно двух их трех в любых сочетаниях.Большую часть жизни диктиостелиум живет в форме одиночных амеб, питаясь бактериями листовой подстилки.
А вот теперь самое интересное. Помните фильм про трансформеров, когда несколько роботов собиралось в одного огромного?
Так вот эти амебы при нехватке пищи образуют клеточные агрегаты, причем размеры такого клеточного образования для микромира огромны — до 1 см. Этот макроорганизм способен ползать и впоследствии формирует «плодовое тело».
Слизевики перед тем как сформировать многоклеточный организм (псевдоплазмодий), поглощают бактерии, но не переваривают их. Более того, на новом месте дают этим бактериям размножится. Такие вот одноклеточные садовники.
Макрофаги нашего организма тоже способны к созданию такого многоклеточного образования. Этого «монстра» называют клеткой Пирогова-Лангханса. Ранее эти многоядерные клетки выявлялись как имунный ответ на внедрение туберкулезной палочки.
Когда пациенту с длительно продолжающимся кашлем рекомендуют сдать анализ мокроты, то в заключении пишется «КУМ не обнаружены». КУМ — это кислотоустойчивые микобактерии. Туберкулезную палочку клетки нашей иммунной системы полноценно фагоцитировать не могут.
Когда происходит контакт макроорганизма с микобактерией туберкулеза, то первыми в борьбу вступают нейтрофилы. И погибают все. Микобактерия оказывается им не по зубам. Затем в бой идет «старший брат» — макрофаг. Макрофаг поглощает бактерии одну за другой, но полноценно переварить их не может. Бактерия устойчива к кислой среде фагосомы, влияет она и на фагосомно-лизосомальное слияние.
Бороться иммунной системе с возбудителем туберкулеза предельно сложно (почему клиника во многом зависит от количества бактерий, попавших в организм). Чтобы ограничить распространение инфекции, «наевшиеся» микобактериями макрофаги начинают объединяться в большую многоклеточную структуру — клетку Пирогова-Лангханса. Поначалу такую микроскопическую находку приписывали воспалению при туберкулезе, но затем выявились и другие заболевания (например, актиномикоз).
Вот про такой воспалительный процесс и говорят: специфический. Ну а что же организму делать с туберкулезной палочкой, которая, ну никак, умирать не хочет? Вокруг зоны специфического воспаления формируется своеобразный саркофаг. Сначала состоит из волокнистого белка — фибрина, затем кальцифицируется. Очаг Гона в легких — нередкая находка на флюорографии. Полностью выздороветь от туберкулеза нельзя. Человек остается навсегда инфицированным (но клинически абсолютно здоровым).
БЦЖ — прививка от туберкулеза. Содержит убитые бактерии, чтобы познакомить иммунные клетки с антигенами возбудителя. Гарантированно защитить прививка не может (понятно, почему), но эффективность иммунного ответа повышается. Повторюсь, все зависит от количества бактерий и состояния организма.
Некоторые последние исследования фагоцитоза.
Как сон влияет на фагоцитарную активность
Одна бессонная ночь — это конечно нехорошо, но в большинстве случаев не вызывает каких-либо последствий.
Другое дело — бесчисленные бессонные ночи. В одном из исследований, опубликованных в журнале «Neuroscience» был оценен биологический эффект лишения сна лабораторных мышей. Было выяснено, что мозг при длительной нехватке сна причиняет себе ущерб. Лабораторных животных разделили на четыре группы. Одна группа — «хорошо отдохнувшие», мышей второй группы периодически будили, в третьей группе животные не спали несколько дней. После чего ученые изучали активность мозга у каждой группы. У мышей, длительно лишенных сна было выявлено повышение активности фагоцитоза. Фагоциты — это клетки-уборщики, необходимые мозгу для очишения от побочных продуктов нейронной активности в течение дня.
После длительного отсутствия сна мозг включает «овердрайв», что может быть очень вредным. Не стоит паниковать, если ваш режим сна и бодрствования не в идеальной форме, но постарайтесь высыпаться.
Фагоцитоз и гипергликемия
Почему хирурги часто назначают при гнойно-воспалительных процессах анализ крови с определением уровня глюкозы?
Почему у больных с сахарным диабетом инфекционные заболевания протекают тяжелее? Один из факторов: быстрые углеводы влияют на активность макрофагов.
Людям давали стограммовые порции углеводов из глюкозы, фруктозы, сахарозы, меда. Затем брали венозную кровь через 1,2,3 и 5 часов после приема пищи. К крови добавляли суспензию, содержащую эпидермальный стафилококк (Staphylococcus epidermidis).
В дальнейшем проводилось исследование активности макрофагов. Установлено, что быстроусвояемые углеводы угнетают фагоцитарную активность макрофагов.
Так что очень важно следить за уровнем глюкозы, тем более больных с сахарным диабетом, проходящих лечение гнойно-воcпалительных процессов.
В заключение
И хотя фагоцитоз — самый древний способ защиты от чужеродных организмов, значения он не утратил. Этот механизм является ключевым в борьбе со стафилококковой инфекцией.
Паламарчук Вячеслав
Источник: vpalamarchuk.ru