Тканевые макрофаги
Макрофáги (от др.-греч. μακρός — большой, и φάγος — пожиратель (синонимы: гистиоцит-макрофаг, гистофагоцит, макрофагоцит, мегалофаг-пожиратель)), полибласты, клетки мезенхимальной природы в животном организме, способные к активному захвату и перевариванию бактерий, остатков погибших клеток и других чужеродных или токсичных для организма частиц. Термин «макрофаги» введён Мечниковым.
К макрофагам относят моноциты крови, гистиоциты соединительной ткани, эндотелиальные клетки капилляров кроветворных органов, купферовские клетки печени, клетки стенки альвеол лёгкого (лёгочные макрофаги) и стенки брюшины (перитонеальные макрофаги).
Установлено, что у млекопитающих предшественники макрофагов образуются в костном мозге. Активными фагоцитарными свойствами обладают также клетки ретикулярной ткани кроветворных органов, объединяемые с макрофагами в ретикуло-эндотелиальную (макрофагическую) систему, выполняющую в организме защитную функцию.
Морфология
Главный тип клеток системы мононуклеарных фагоцитов. Это крупные (10 — 24 мкм) долгоживущие клетки с хорошо развитым лизосомальным и мембранным аппаратом. На их поверхности имеются рецепторы к Fc-фрагменту IgGl и IgG3, C3b-фрагменту С, рецепторам В- и Т-лимфоцитов, комплементу, другим интерлейкинам и гистамину.
Тканевые макрофаги
Фактически моноцит становится макрофагом, когда покидает сосудистое русло и проникает в ткани.
В зависимости от типа ткани выделяют следующие виды макрофагов.
· Гистиоциты — макрофаги соединительной ткани; компонент ретикуло-эндотелиальной системы.
· Купферовские клетки — иначе эндотелиальные звездчатые клетки печени.
· Альвеолярные макрофаги — иначе, пылевые клетки; расположены в альвеолах.
· Эпителиоидные клетки — составляющие гранулемы.
· Остеокласты — многоядерные клетки, участвующие в резорбции костной ткани.
· Микроглия — клетки центральной нервной системы, разрушающие нейроны и поглощающие инфекционные агенты.
· Макрофаги селезенки
Идентификация макрофагов
макрофаги содержат многочисленные цитоплазматические ферменты и могут быть идентифицированы в тканях гистохимическими методами, которые обнаруживают эти ферменты. Некоторые ферменты, типа мурамидазы (лизоцима) и химотрипсина, могут обнаруживаться методом меченных антител (иммуногистохимия), при котором используются антитела против белков фермента. Такие моноклональные антитела против различных CD антигенов широко используются для идентифицикации макрофагов.
Функции макрофагов
функции макрофагов включают в себя фагоцитоз, «обработку» антигенов и взаимодействие с цитокинами.
Фагоцитоз
· Неиммунный фагоцитоз: макрофаги способны фагоцитировать чужеродные частицы, микроорганизмы и остатки поврежденных клеток непосредственно, без вызова иммунного ответа. Однако фагоцитоз микроорганизмов и их уничтожение значительно облегчаются при присутствии специфических иммуноглобулинов, комплемента и лимфокинов, которые производятся иммунологически активированными T-лимфоцитами.
· Иммунный фагоцитоз: макрофаги имеют поверхностные рецепторы для C3b и Fc-фрагмента иммуноглобулинов. Любые частицы, которые покрыты иммуноглобулином или комплементом (опсонизированы), фагоцитируются значительно легче, чем «голые» частицы.
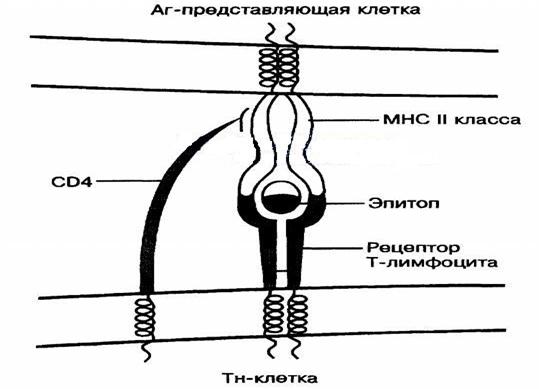
· «Обработка» антигенов: макрофаги «обрабатывают» антигены и представляют их B- и T-лимфоцитам в необходимой форме; Это клеточное взаимодействие включает одновременное распознавание лимфоцитами MHC молекул и «обработанных антигенов», находящихся на поверхности макрофагов.
· Взаимодействие с цитокинами: макрофаги взаимодействуют с цитокинами, производимыми T-лимфоцитами для защиты организма против определенных повреждающих агентов. Типичный результат такого взаимодействия — формирование гранулем. Макрофаги также производят цитокины, включая интерлейкин-l, b-интерферон и факторы роста T- и B-клеток. Различные взаимодействия лимфоцитов и макрофагов в тканях проявляются морфологически при хроническом воспаление.
Роль макрофагов не ограничивается секрецией ИЛ-1. В этих клетках синтезируется еще ряд биологически активных веществ, каждое из которых делает свой вклад в воспаление. К ним относятся: эстеразы, протеазы и антипротеазы; лизосомальные гидролазы — коллагеназа, аластаза, лизоцим, α-макроглобулин; монокины — ИЛ-1, колониестимулирующий фактор, фактор, стимулирующий рост фибробластов; антиинфекционные агенты — интерферон, трансферрин, транскобаламин; компоненты комплемента: С1, С2, СЗ, С4, С5, С6; дериваты арахидоновой кислоты: простагландин Е2, тромбоксан А2, лейкотриены.
Источник: cyberpedia.su
Функции макрофагов
Макрофаги выполняют следующие функции:
- Осуществляют фагоцитоз.
- Процессируют антиген, а затем рекомендуют (презентируют) его пептиды Т-хелперам, поддерживая осуществление иммунного ответа (рис. 6).
- Выполняют секреторную функцию, состоящую в синтезе и выделении ферментов (кислые гидролазы и нейтральные протеиназы), компонентов комплемента, ингибиторов ферментов, компонентов межклеточного матрикса, биологически активных липидов (простагландинов и лейкотриенов), эндогенных пирогенов, цитокинов (ИЛ-1β, ИЛ-6, ФНО-α и пр.).
- Оказывают цитотоксическое влияние на клетки-мишени при условии фиксации на них антитез ы соответствующей стимуляции со стороны Т-лимфоцитов (так называемые реакции антителозависимой клеточно-опосредованной цитотоксичности).
- Изменяют метаболизм при воспалении.
- Принимают участие в асептическом воспалении и разрушении инородных частиц.
- Обеспечивают процесс заживления ран.
Фагоцитоз
Основным свойством макрофага (рис. 4) является способность к фагоцитозу — селективному эндоцитозу и дальнейшей деструкции объектов, содержащих патогенсвязанные молекулярные шаблоны или присоединенные опсонины (рис. 5, 6).
Рецепторы макрофагов
см. Рецепторы врожденного иммунитета#Рецепторы фагоцитов
Для выявления таких объектов макрофаги содержат на своей поверхности рецепторы шаблонного распознавания (в частности, маннозосвязывающий рецептор и рецептор к бактериальным липополисахаридам), а также рецепторы к опсонинам (например, к C3b и Fc-фрагментам антител).
Макрофаги на своей поверхности экспрессируют рецепторы, обеспечивающие процессы адгезии (например, CDllc и CDllb), восприятие регуляторных влияний и участие в межклеточном взаимодействии. Так, есть рецепторы к различным цитокинам, гормонам, биологически активным веществам.
Презентация антигена
Пока происходит разрушение захваченного объекта, на мембране макрофага существенно возрастает количество рецепторов шаблонного распознавания и рецепторов к опсонинам, что позволяет продолжать осуществление фагоцитоза, а также повышается экспрессия молекул главного комплекса гистосовместимости II класса, вовлекаемых в процессы презентации (рекомендации) антигена иммунокомпетентным клеткам.
раллельно макрофаг производит синтез доиммунных цитокинов (в первую очередь ИЛ-1β, ИЛ-6 и фактора некроза опухоли α), привлекающих к работе другие фагоциты и активирующих иммунокомпетентные клетки, подготавливая их к предстоящему распознаванию антигена. Остатки патогена удаляются из макрофага путем экзоцитоза, а иммуногенные пептиды в комплексе с НLA II поступают на поверхность клетки для активации Т-хелперов, т.е. поддержания иммунного ответа.
Макрофаги и воспаление
Хорошо известна важная роль макрофагов в асептическом воспалении, которое развивается в очагах неинфекционного некроза (в частности, ишемического). Благодаря экспрессии рецепторов к «мусору» (scavenger receptor) эти клетки эффективно фагоцитируют и обезвреживают элементы тканевого детрита.
Также именно макрофаги захватывают и перерабатывают инородные частицы (например, пыль, частицы металла), по разным причинам попавшие в организм. Трудность фагоцитоза таких объектов состоит в том, что они абсолютно лишены молекулярных шаблонов и не фиксируют опсонины. Чтобы выйти из этой сложной ситуации, макрофаг начинает синтезировать компоненты межклеточного матрикса (фибронектин, протеогликаны и др.), которыми обволакивает частицу, т.е. искусственно создает такие ее поверхностные структуры, которые легко распознаются. Материал с сайта http://wiki-med.com
Установлено, что за счет деятельности макрофагов происходит перестройка метаболизма при воспалении. Так, ФНО-α активирует липопротеинлипазу, мобилизирующую липиды из депо, что при длительном течении воспаления приводит к похуданию. За счет синтеза доиммунных цитокинов макрофаги способны угнетать синтез целого ряда продуктов в печени (так, ФНО-α угнетает синтез гепатоцитами альбуминов) и повышать образование острофазовых белков (в первую очередь за счет ИЛ-6), относящихся преимущественно к глобулиновой фракции. Подобная перепрофилизация гепатоцитов наряду с увеличением синтеза антител (иммуноглобулинов) приводит к снижению альбумино-глобулинового коэффициента, что используется как лабораторный маркер воспалительного процесса.
Кроме классически активированных макрофагов, речь о которых шла выше, выделяют субпопуляцию альтернативно активированных макрофагов, которые обеспечивают процесс заживления ран и репарацию после воспалительной реакции. Эти клетки продуцируют большое количество ростовых факторов — тромбоцитарного, инсулинового, факторов роста, трансформирующего фактора роста β и фактора роста эндотелия сосудов. Альтернативно активированные макрофаги формируются под действием цитокинов ИЛ-13 и ИЛ-4, т.е. в условиях реализации преимущественно гуморального иммунного ответа.
Хорошо известна важная роль макрофагов в асептическом воспалении, которое развивается в очагах неинфекционного некроза (в частности, ишемического).
Макрофаги в крови
Благодаря экспрессии рецепторов к «мусору» (scavenger receptor) эти клетки эффективно фагоцитируют и обезвреживают элементы тканевого детрита.
Также именно макрофаги захватывают и перерабатывают инородные частицы (например, пыль, частицы металла), по разным причинам попавшие в организм.
Трудность фагоцитоза таких объектов состоит в том, что они абсолютно лишены молекулярных шаблонов и не фиксируют опсонины. Чтобы выйти из этой сложной ситуации, макрофаг начинает синтезировать компоненты межклеточного матрикса (фибронектин, протеогликаны и др.), которыми обволакивает частицу, т.е. искусственно создает такие ее поверхностные структуры, которые легко распознаются. Материал с сайта http://wiki-med.com
Установлено, что за счет деятельности макрофагов происходит перестройка метаболизма при воспалении.
Так, ФНО-α активирует липопротеинлипазу, мобилизирующую липиды из депо, что при длительном течении воспаления приводит к похуданию. За счет синтеза доиммунных цитокинов макрофаги способны угнетать синтез целого ряда продуктов в печени (так, ФНО-α угнетает синтез гепатоцитами альбуминов) и повышать образование острофазовых белков (в первую очередь за счет ИЛ-6), относящихся преимущественно к глобулиновой фракции.
Подобная перепрофилизация гепатоцитов наряду с увеличением синтеза антител (иммуноглобулинов) приводит к снижению альбумино-глобулинового коэффициента, что используется как лабораторный маркер воспалительного процесса.
Кроме классически активированных макрофагов, речь о которых шла выше, выделяют субпопуляцию альтернативно активированных макрофагов, которые обеспечивают процесс заживления ран и репарацию после воспалительной реакции.
Эти клетки продуцируют большое количество ростовых факторов — тромбоцитарного, инсулинового, факторов роста, трансформирующего фактора роста β и фактора роста эндотелия сосудов. Альтернативно активированные макрофаги формируются под действием цитокинов ИЛ-13 и ИЛ-4, т.е. в условиях реализации преимущественно гуморального иммунного ответа.
Рецепторы макрофагов
На поверхности макрофагов содержится большой набор рецепторов, обеспечивающих участие клеток в широком круге физиологических реакций, в том числе во врожденном и адаптивном иммунном ответе.
Прежде всего, на мембране МФ экспрессированы паттерн-распознающие рецепторы врожденного иммунитета, обеспечивающие распознавание ПАМС большинства патогенов и ОАМС — молекулярных структур, ассоциированных с опасными для жизни клеток воздействиями и ситуациями, в первую очередь стрессовых белков.
Ведущими ПРР МН/МФ являютсяТолл-подобные и NOD-рецепторы.
На поверхности этих клеток содержатся все известные экспрессирующиеся на плазматических мембранах клеток TLR: TLR1, TLR2, TLR4, TLR5, TLR6 и TLR10. В цитоплазме содержатся внутриклеточные TLR3, TLR7, TLR8, TLR9, а также NOD1 и NOD2-рецепторы.
Такой обширный репертуар ПРР позволяет МФ распознавать практически все виды патогенов (бактерии, вирусы, грибы, простейшие, паразиты), а также молекулярные структуры, характерные для патологически измененных, поврежденных и апоптозных клеток. См. ч.II гл.2 «Рецепторы врожденного иммунитета и распознаваемые ими молекулярные структуры».
Связывание бактериальных ЛПС с помощью TLR4 рецепторов МФ опосредовано мембранным белком CD14, который является маркером МФ.
CD14 взаимодействует с комплексом «бактериальный ЛПС — ЛПС-связывающий белок», что облегчает взаимодействие ЛПС с TLR4.
На поверхности моноцитов содержится аминопептидаза N (CD13), которая также относится к ПРР моноцитов, но отсутствует у МФ. Молекула CD13 обладает способностью связывать белки оболочки некоторых вирусов.
На МН/МФ экспрессировано большое количество фагоцитарных рецепторов.
Это лектиновые рецепторы (в первую очередь маннозный рецептор, дектин-1 и DC-SIGN), а также скавенджер-рецепторы, с помощью которых осуществляется прямое распознавание патогенов и других объектов фагоцитоза.
(См. ч.II гл.2 «Рецепторы врожденного иммунитета и распознаваемые ими молекулярные структуры»). Лигандами для скавенджер-рецепторов служат компоненты ряда бактерий, в том числе стафилококков, нейссерий, листерий, а также видоизмененные структуры собственных клеток, модифицированные липопротеины низкой плотности и фрагменты апоптозных клеток.
Маннозный рецептор опосредует захват МН/МФ многих видов бактерий, в том числе Mycobacteria, Leismania, Legionella, Pseudomonas aeruginosa и др.
Структура этого рецептора предопределяет его способность к высокоаффинному связыванию пептидогликана клеточной стенки бактерий. Интересно, что цитокины, активирующие МФ (IFN-γ, TNF-α), вызывают угнетение синтеза этого рецептора и снижение его экспрессии. Напротив, противоспалительные кортикостероиды повышают синтез маннозного рецептора и его экспрессию на МФ.
Стимулятором экспрессии этого рецептора является витамин Д.
На мембране макрофагов обнаружены также специальные рецепторы для связывания конечных продуктов гликозилирования (AGEs), которые прогрессивно накапливаются в тканях по мере старения организма и ускоренно накапливаются при диабете. Эти продукты гликозилирования вызывают повреждение тканей за счет перекрестного связывания белков.
Макрофаги, имеющие специальные рецепторы для AGEs, захватывают и деградируют модифицированные этими продуктами белки, предупреждая тем самым развитие деструкции тканей.
На МН/МФ экспрессированы также практически все фагоцитарные рецепторы, с помощью которых осуществляется опосредованное распознавание опсонизированных антителами и комплементом патогенов и других чужеродных частиц и клеток.
К ним в первую очередь относятся Fc-рецепторы и рецепторы для фрагментов активированного комплемента (CR1, CR3 и CR4, а также рецепторы для фрагмента C1q и анафилатоксинов С3а и С5а).
Ғс-рецепторы обеспечивают распознавание и стимулируют фагоцитоз объектов, опсонизированных антителами.
Для связывания IgG существует три различных рецептора: FcγRI, FcγRII и FcγRIII (соответственно CD64, CD32 и CD16).
FcγRI — единственный из этих рецепторов, который характеризуется высокой аффинностью для мономерного IgG и экспрессирован почти исключительно на макрофагах.
В отличие от него, низкоаффинный рецептор FcγRII экспрессирован на моноцитах и макрофагах. FcγRIII также экспрессирован на моноцитах и макрофагах, он отличается низкой аффинностью для IgG и связывает, в основном, иммунные комплексы или агрегированный IgG. Все три типа рецепторов опосредуют фагоцитоз бактерий и других клеток, опсонизированных IgG, участвуют в антителозависимой клеточной цитотоксичности естественных киллеров (АЗКЦТ) и фагоцитов в отношении клеток-мишеней, несущих на мембране комплексы антиген-антитело.
В качестве таких клеток-мишеней могут выступать клетки, инфицированные вирусами, простейшими или злокачественно трансформированные клетки самого организма. Такой вариант защиты наиболее эффективен и при некоторых паразитарных и вирусных инфекциях, при которых макрофаги не способны захватывать ни сами патогены, ни их комплексы со специфическими антителами.
Характеристика, развитие, расположение и роль макрофагов
Активация макрофагов через Fc-рецепторы ведет к лизису клеток-мишеней за счет выделения ряда медиаторов (в первую очередь TNF-α), которые вызывают гибель этих клеток. Некоторые цитокины (IFN-γ и ГМ-КСФ) способны повышать эффективность АЗКЦТ с участием моноцитов и макрофагов.
Важной группой рецепторов являются рецепторы для хемокинов и других хемоаттрактантов.
Помимо рецепторов для С3а, С5а, С5b67, вызывающих хемотаксис МН/МФ в очаг воспаления или инфекции, на поверхности этих клеток содержатся рецепторы для воспалительных хемокинов (CXCR1, CCR1, CCR2, CCR3, CCR4, CCR5, CCR8 и др.).
Воспалительные хемокины, продуцируемые эпителиальными клетками и эндотелиальными клетками сосудов, а также резидентными МФ, находящимися в очаге реакции, которые были активированы контактом с патогенами или повреждением ткани, стимулируют хемотаксис новых клеток, участвующих в защите.
Первыми в очаг воспаления поступают нейтрофилы, позднее начинается моноцитарно-макрофагальная инфильтрация, вызываемая контактом хемокиновых рецепторов этих клеток с соответствующими лигандами.
На мембранах МН/МФ экспрессируется большое количество гликопротеиновых рецепторов для цитокинов.
Связывание цитокинов с соответствующими рецепторами служит первым звеном в цепи передачи активационного сигнала к ядру клетки. Наиболее специфичен для МН/МФ рецептор для ГМ-КСФ (CD115). Наличие этого рецептора позволяет дифференцировать МН и их предшественники от клеток гранулацитарного ряда, на которых этот рецептор отсутствует.
Особенно важными для МН/МФ являются рецепторы для IFN-γ (IFNγRI и IFNγRII), так как через них происходит активация многих функций этих клеток.
Имеются также рецепторы для провоспалительных цитокинов (ИЛ-1, ИЛ-6, TNF-α, ИЛ-12, ИЛ-18, ГМ-КСФ), активирующих, в том числе аутокринно, МН/МФ, участвующие в воспалительном ответе.
Тканевые макрофаги
Несколько популяций тканевых макрофагов, потомков мононуклеарных фагоцитов, также были охарактеризованы по поверхностным маркерам и биологическим функциям. В гранулемах обычно обнаруживаются эпителиоидные клетки, которые, по-видимому, образуются из моноцитов крови, активированных в ходе иммунного ответа на чужеродный антиген, например при кожной реакции гиперчувствительности замедленного типа.
Эпителиоидные клетки обладают многими морфологическими признаками макрофагов и несут рецепторы Fc и СЗ. В целом они обладают меньшей фагоцитирующей активностью, чем макрофаги. Другой тип клеток, многоядерные гигантские клетки, образуются, по всей видимости, за счет слияния макрофагов, а не за счет деления ядер в отсутствие цитоплазматического деления.
Были идентифицированы два типа таких клеток: клетки Ланганса с относительно небольшим числом ядер на периферии цитоплазмы, и клетки типа инородного тела, у которых множество ядер распределено по всей цитоплазме.
Судьба моноцитов, проникающих в участки воспаления, может быть различной: они могут превратиться в оседлые макрофаги, трансформироваться в эпителиоидные клетки или слиться с другими макрофагами и стать многоядерными гигантскими клетками.
Когда воспаление спадает, макрофаги исчезают — каким образом, пока неясно. Их число может уменьшаться в результате либо гибели, либо их миграции из участка воспаления.
Купферовские клетки представляют собой оседлые макрофаги печени. Они граничат с кровотоком, что позволяет им постоянно контактировать с чужеродными антигенами и другими иммуностимулирующими агентами. Анатомическое расположение между венами, несущими кровь от желудочно-кишечного тракта, и собственным кровотоком печени приводит к тому, что купферовские клетки одними из первых в ряду мононуклеарных фагоцитов взаимодействуют с иммуногенами, поглощаемыми из кишечника.
Как и другие тканевые макрофаги, купферовские клетки являются долгоживущими потомками моноцитов, которые поселились в печени и дифференцировались в макрофаги.
Они живут в печени в среднем около 21 дня. Важнейшая функция купферовских клеток заключается в поглощении и деградации растворенных и нерастворимых материалов в портальной крови.
Купферовские клетки играют важнейшую роль в очистке кровотока от множества потенциально вредных биологических материалов, включая бактериальные эндотоксины, микроорганизмы, активированные факторы свертывания и растворимые иммунные комплексы. В соответствии со своей функцией купферовские клетки содержат необычайно большое количество лизосом, содержащих кислые гидролазы и способных к активному внутриклеточному перевариванию.
Ранее считалось, что способность купферовских клеток осуществлять ка- кие-либо функции помимо фагоцитарных относительно мала.
Поэтому можно было думать, что, поглощая и переваривая большие потенциально иммуногенные соединения, позволяя оставаться в кровотоке лишь небольшим с трудом поглощаемым фрагментам, купферовские клетки участвуют в создании состояния толерантности. Однако недавние исследования высокоочищенных купферовских клеток in vitro показали, что они способны функционировать как антиген-презентирующие клетки во многих известных тестах на способность активировать Т-клетки. Видимо, анатомические и физиологические особенности нормального печеночного микроокружения накладывают ограничения на активность купферовских клеток, не позволяя им участвовать в индукции иммунного ответа in vivo.
Альвеолярные макрофаги выстилают альвеолы и являются первыми им- мунологически компетентными клетками, поглощающими вдыхаемые патогены. Важно было поэтому выяснить, способны ли к функционированию в качестве вспомогательных клеток макрофаги из такого органа, как легкие, имеющие обширную эпителиальную поверхность, постоянно контактирующую с внешними антигенами. Находящиеся на поверхности альвеол макрофаги идеально расположены для того, чтобы взаимодействовать с антигеном и затем представлять его Т-лимфоцитам.
Альвеолярные макрофаги морской свинки оказались весьма активными вспомогательными клетками в тестах на пролиферацию Т-клеток, индуцированную как антигеном, так и митогеном.
Затем было показано, что антиген, введенный животному в трахею, может индуцировать первичный иммунный ответ и вызывать избирательное обогащение специфичных к нему Т-клеток в легких.
Источник: cyberlesson.ru
МАКРОФАГИ (греч, makros большой + phagos пожирающий) — клетки соединительной ткани, обладающие активной подвижностью, адгезивностью и выраженной способностью к фагоцитозу. Макрофаги открыты И. И. Мечниковым; он впервые установил их роль в защитных и других реакциях организма и предложил термин «макрофаги», подчеркивающий отличия этих клеток от клеток меньшего размера — «микрофагов» (т. е. сегментоядерных лейкоцитов, нейтрофилов), фагоцитирующих лишь мелкие чужеродные частицы, напр. микробы. Макрофаги описывали под разными названиями: клазматоциты Ранвье, рагиокринные клетки, адвентициальные клетки, блуждающие клетки в покое, пирроловые клетки, полибласты, амебоидные, металлофильные клетки, макрофагоциты, гистиоциты. Большинство этих терминов имеет лишь исторический интерес.
М., как и все клетки соединительной ткани, имеют мезенхимное происхождение, а в постнатальном онтогенезе дифференцируются из стволовой кроветворной клетки (см. Кроветворение), проходя в костном мозге последовательно стадии монобласта, промоноцита и моноцита. Последние циркулируют в крови, и, выселяясь в ткани, превращаются в М. Различают М. свободные (мигрирующие) и фиксированные в тканях. М. также подразделяют на гематогенные, образующиеся из только что выселившихся из крови моноцитов, и гистиогенные, которые ранее присутствовали в тканях. В зависимости от локализации различают М. рыхлой соединительной ткани — гистиоциты (см.), печени — звездчатые ретикулоэндотелиоциты (купферовы клетки), легкого — альвеолярные М., серозных полостей — перитонеальные и плевральные М., М. костного мозга и лимфоидных органов, глиальные макрофаги ц. н. с. (микроглии). Из М. происходят, по-видимому, и остеокласты.
М., являясь последней стадией дифференцировки одноядерных фагоцитов, не делятся митозом. Исключение, возможно, составляют М. в очагах хрон, воспаления. На основе общего происхождения из стволовой кроветворной клетки, строения и функции М. и их клетки-предшественники (моноциты и др.), согласно классификации, опубликованной в Бюллетене ВОЗ (1973), включены в систему мононуклеарных фагоцитов. В отличие от этого ретикулоэндотелиальная система (см.) объединяет клетки, имеющие различное происхождение и обладающие способностью к фагоцитозу: ретикулярные клетки, эндотелиальные клетки (в частности синусоидные капилляры кроветворных органов) и другие элементы.
Строение М. отличается разнообразием, зависящим от фагоцитарной активности, свойств поглощенного материала и пр. (рис. 1). В отличие от своих предшественников моноцитов (см. Лейкоциты) М. имеют большие размеры (20—100 мкм), содержат много плотных цитоплазматических гранул и митохондрий; в слабобазофильной (иногда оксифильной) цитоплазме нередко видны остатки фагоцитированного материала. Ядро сферической, бобовидной или неправильной формы. При наблюдении в фазовом контрастном микроскопе в М. выявляется характерная ундулирующая клеточная мембрана, совершающая волнообразные движения. При электронной микроскопии в М. виден хорошо развитый пластинчатый комплекс (см. Гольджи комплекс), обычно небольшое количество гранулярного эндоплазматического ретикулума. Отражением фагоцитарной активности являются плотные цитоплазматические гранулы — лизосомы (см.), фагосомы, мультивезикулярные остаточные тельца — так наз. миелиновые фигуры (рис. 2). Наблюдаются также микротрубочки и пучки микрофиламент.
Функц, значение М. определяется их высокой способностью к поглощению и переработке плотных частиц — фагоцитоз (см.) и растворимых веществ — Пиноцитоз (см.).
Источник: xn--90aw5c.xn--c1avg
Липидные «антенны»
Своей потенциальной «многоликостью» макрофаг обязан необычной организации генетического материала – так называемому открытому хроматину. Этот не до конца изученный вариант структуры клеточного генома обеспечивает быстрое изменение уровня экспрессии (активности) генов в ответ на различные стимулы.

Выполнение макрофагом той или иной функции зависит от характера получаемых им стимулов. Если стимул будет распознан как «чужой», то происходит активация тех генов (и соответственно функций) макрофага, которые направлены на уничтожение «пришельца». Однако макрофаг могут активировать и сигнальные молекулы самого организма, которые побуждают эту иммунную клетку участвовать в организации и регуляции обмена веществ. Так, в условиях «мирного времени», т. е. при отсутствии патогена и обусловленного им воспалительного процесса, макрофаги участвуют в регуляции экспрессии генов, отвечающих за метаболизм липидов и глюкозы, дифференцировку клеток жировой ткани.
Интеграция между взаимоисключающими «мирным» и «военным» направлениями работы макрофагов осуществляется путем изменения активности рецепторов клеточного ядра, представляющих собой особую группу регуляторных белков.
Среди этих ядерных рецепторов следует особо выделить так называемые липидные сенсоры, т. е. белки, способные взаимодействовать с липидами (например, окисленными жирными кислотами или производными холестерина) (Смирнов, 2009). Нарушение работы этих чувствительных к липидам регуляторных белков в макрофагах может быть причиной системных обменных нарушений. Например, дефицит в макрофагах одного из этих ядерных рецепторов, обозначаемых как PPAR-гамма, приводит к развитию диабета 2 типа и дисбалансу липидного и углеводного обмена во всем организме.
Клеточные метаморфозы
В разнородном сообществе макрофагов на основе базовых характеристик, определяющих их принципиальные функции, выделяют три основных клеточных субпопуляции: макрофаги М1, М2 и Мox, которые участвуют, соответственно, в процессах воспаления, восстановления поврежденных тканей, а также защите организма от окислительного стресса.
«Классический» макрофаг М1 формируется из клетки-предшественника (моноцита) под действием каскада внутриклеточных сигналов, запускающихся после распознавания инфекционного агента с помощью специальных рецепторов, расположенных на поверхности клетки.
Образование «пожирателя» М1 происходит в результате мощной активации генома, сопровождаемой активацией синтеза более чем сотни белков – так называемых факторов воспаления. К ним относятся ферменты, способствующие генерации свободных радикалов кислорода; белки, привлекающие в очаг воспаления другие клетки иммунной системы, а также белки, способные разрушать оболочку бактерий; воспалительные цитокины – вещества, обладающие свойствами активировать иммунные клетки и оказывать токсическое действие на остальное клеточное окружение. В клетке активируется фагоцитоз и макрофаг начинает активно разрушать и переваривать все, что встретится на его пути (Шварц, Свистельник, 2012). Так появляется очаг воспаления.
Однако уже на начальных этапах воспалительного процесса макрофаг М1 начинает активно секретировать и противовоспалительные субстанции – низкомолекулярные липидные молекулы. Эти сигналы «второго эшелона» начинают активировать вышеупомянутые липидные сенсоры в новых «рекрутах»-моноцитах, прибывающих в очаг воспаления. Внутри клетки запускается цепь событий, в результате которых активирующий сигнал поступает на определенные регуляторные участки ДНК, усиливая экспрессию генов, отвечающих за гармонизацию обмена веществ и одновременно подавляя активность «провоспалительных» (т. е. провоцирующих воспаление) генов (Душкин, 2012).

Так в результате альтернативной активации образуются макрофаги М2, которые завершают воспалительный процесс и способствуют тканевому восстановлению. Популяцию М2 макрофагов можно, в свою очередь, разделить на группы в зависимости от их специализации: уборщики мертвых клеток; клетки, участвующие в реакции приобретенного иммунитета, а также макрофаги, секретирующие факторы, которые способствуют замещению погибших тканей соединительной тканью.
Еще одна группа макрофагов – Мох, формируется в условиях так называемого окислительного стресса, когда в тканях возрастает опасность повреждения их свободными радикалами. Например, Мох составляют около трети всех макрофагов атеросклеротической бляшки. Эти иммунные клетки не только сами устойчивы к повреждающим факторам, но и участвуют в антиоксидантной защите организма(Gui et al., 2012).
Пенистый камикадзе
Одной из самых интригующих метаморфоз макрофага является его превращение в так называемую пенистую клетку. Такие клетки были обнаружены в атеросклеротических бляшках, а свое название получили из-за специфического внешнего вида: под микроскопом они напоминали мыльную пену. По сути, пенистая клетка – это тот же макрофаг М1, но переполненный жировыми включениями, преимущественно состоящими из водонерастворимых соединений холестерина и жирных кислот.
Была высказана гипотеза, ставшая общепринятой, что пенистые клетки образуются в стенке атеросклеротических сосудов в результате неконтролируемого поглощения макрофагами липопротеинов низкой плотности, переносящих «плохой» холестерин. Однако впоследствии было обнаружено, что накопление липидов и драматическое (в десятки раз!) возрастание скорости синтеза ряда липидов в макрофагах можно спровоцировать в эксперименте только лишь одним воспалением, без всякого участия липопротеинов низкой плотности (Душкин, 2012).
Это предположение подтвердилось клиническими наблюдениями: оказалось, что превращение макрофагов в пенистую клетку происходит при разнообразных заболеваниях воспалительной природы: в суставах – при ревматоидном артрите, в жировой ткани – при диабете, в почках – при острой и хронической недостаточности, в ткани мозга – при энцефалитах. Однако понадобилось около двадцати лет исследований, чтобы понять, как и зачем макрофаг при воспалении превращается в клетку, нафаршированную липидами.

Оказалось, что активация провоспалительных сигнальных путей в М1 макрофагах приводит к «выключению» тех самых липидных сенсоров, которые в нормальных условиях контролируют и нормализуют липидный обмен (Душкин, 2012). При их «выключении» клетка и начинает накапливать липиды. При этом образующиеся липидные включения представляют собой вовсе не пассивные жировые резервуары: входящие в их состав липиды обладают способностью усиливать воспалительные сигнальные каскады. Главная цель всех этих драматических изменений – любыми средствами активировать и усилить защитную функцию макрофага, направленную на уничтожение «чужих» (Melo, Drorak, 2012).
Однако высокое содержание холестерина и жирных кислот дорого обходится пенистой клетке – они стимулируют ее гибель путем апоптоза, запрограммированной клеточной смерти. На внешней поверхности мембраны таких «обреченных» клеток обнаруживается фосфолипид фосфатидилсерин, в норме расположенный внутри клетки: появление его снаружи является своеобразным «похоронным звоном». Это сигнал «съешь меня», который воспринимают М2 макрофаги. Поглощая апоптозные пенистые клетки, они начинают активно секретировать медиаторы заключительной, восстановительной стадии воспаления.
Фармакологическая мишень
Воспаление как типовой патологический процесс и ключевое участие в нем макрофагов является, в той или иной мере, важной составляющей в первую очередь инфекционных заболеваний, вызванных различными патологическими агентами, от простейших и бактерий до вирусов: хламидиальные инфекции, туберкулез, лейшманиоз, трипаносомоз и др. Вместе с тем макрофаги, как уже упоминалось выше, играют важную, если не ведущую, роль в развитии так называемых метаболических заболеваний: атеросклероза (главного виновника сердечно-сосудистых заболеваний), диабета, нейродегенеративных заболеваний мозга (болезнь Альцгеймера и Паркинсона, последствия инсультов и черепно-мозговых травм), ревматоидного артрита, а также онкологических заболеваний.
Разработать стратегию управления этими клетками при различных заболеваниях позволили современные знания о роли липидных сенсоров в формировании различных фенотипов макрофага.
Так, оказалось, что в процессе эволюции хламидии и туберкулезные палочки научились использовать липидные сенсоры макрофагов, чтобы стимулировать не опасную для них альтернативную (в М2) активацию макрофагов. Благодаря этому поглощенная макрофагом туберкулезная бактерия может, купаясь как сыр в масле в липидных включениях, спокойно дожидаться своего освобождения, а после гибели макрофага размножаться, используя содержимое погибших клеток в качестве пищи (Melo, Drorak, 2012).
Если в этом случае использовать синтетические активаторы липидных сенсоров, которые препятствуют образованию жировых включений и, соответственно, предотвращают «пенистую» трансформацию макрофага, то можно подавить рост и понизить жизнеспособность инфекционных патогенов. По крайней мере в экспериментах на животных уже удалось в разы снизить обсемененность легких мышей туберкулезными бациллами, используя стимулятор одного из липидных сенсоров или ингибитор синтеза жирных кислот (Lugo-Villarino et al., 2012).
 Еще один пример – такие болезни, как инфаркт миокарда, инсульт и гангрена нижних конечностей, опаснейшие осложнения атеросклероза, к которым приводит разрыв так называемых нестабильных атеросклеротических бляшек, сопровождаемый моментальным образованием тромба и закупоркой кровеносного сосуда.
Еще один пример – такие болезни, как инфаркт миокарда, инсульт и гангрена нижних конечностей, опаснейшие осложнения атеросклероза, к которым приводит разрыв так называемых нестабильных атеросклеротических бляшек, сопровождаемый моментальным образованием тромба и закупоркой кровеносного сосуда.
Формированию таких нестабильных атеросклеротических бляшек и способствует макрофаг М1/пенистая клетка, который продуцирует ферменты, растворяющие коллагеновое покрытие бляшки. В этом случае наиболее эффективная стратегия лечения – превращение нестабильной бляшки в стабильную, богатую коллагеном, для чего требуется трансформировать «агрессивный» макрофаг М1 в «умиротворенный» М2.
Экспериментальные данные свидетельствуют, что подобной модификации макрофага можно добиться, подавляя в нем продукцию провоспалительных факторов. Такими свойствами обладает ряд синтетических активаторов липидных сенсоров, а также природные вещества, например, куркумин – биофлавоноид, входящий в состав корня куркумы, хорошо известной индийской пряности.
Нужно добавить, что такая трансформация макрофагов актуальна при ожирении и диабете 2 типа (большая часть макрофагов жировой ткани имеет М1 фенотип), а также при лечении нейродегенеративных заболеваний мозга. В последнем случае в мозговых тканях происходит «классическая» активация макрофагов, что приводит к повреждению нейронов и накоплению токсичных веществ. Превращение М1-агрессоров в мирных дворников М2 и Mox, уничтожающих биологический «мусор», может в ближайшее время стать ведущей стратегией лечения этих заболеваний (Walace, 2012).
С воспалением неразрывно связано и раковое перерождение клеток: например, имеются все основания считать, что 90 % опухолей в печени человека возникает как следствие перенесенных инфекционных и токсических гепатитов. Поэтому с целью профилактики раковых заболеваний необходимо контролировать популяцию М1 макрофагов.
Однако не все так просто. Так, в уже сформированной опухоли макрофаги преимущественно приобретают признаки статуса М2, который содействует выживанию, размножению и распространению самих раковых клеток. Более того, такие макрофаги начинают подавлять противораковый иммунный ответ лимфоцитов. Поэтому для лечения уже образовавшихся опухолей разрабатывается другая стратегия, основанная на стимулировании у макрофагов признаков классической М1-активации (Solinas et al., 2009).
Примером такого подхода служит технология, разработанная в новосибирском Институте клинической иммунологии СО РАМН, при которой макрофаги, полученные из крови онкобольных, культивируют в присутствии стимулятора зимозана, который накапливается в клетках. Затем макрофаги вводят в опухоль, где зимозан освобождается и начинает стимулировать классическую активацию «опухолевых» макрофагов.

Сегодня становится все более очевидно, что соединения, вызывающие метаморфозы макрофагов, оказывают выраженное атеропротективное, антидиабетическое, нейропротективное действие, а также защищают ткани при аутоиммунных заболеваниях и ревматоидном артрите. Однако такие препараты, имеющиеся на сегодня в арсенале практикующего врача, – фибраты и производные тиазолидона, хотя и снижают смертность при этих тяжелых заболеваниях, но при этом имеют выраженные тяжелые побочные действия.
Эти обстоятельства стимулируют химиков и фармакологов к созданию безопасных и эффективных аналогов. За рубежом – в США, Китае, Швейцарии и Израиле уже проводятся дорогостоящие клинические испытания подобных соединений синтетического и природного происхождения. Несмотря на финансовые трудности, российские, в том числе и новосибирские, исследователи также вносят свой посильный вклад в решение этой проблемы.
Так, на кафедре химии Новосибирского государственного университета было получено безопасное соединение TS-13, стимулирующее образование Мox фагоцитов, которое обладает выраженным противовоспалительным эффектом и оказывает нейропротективное действие в экспериментальной модели болезни Паркинсона (Дюбченко и др., 2006; Зенков и др., 2009).
В Новосибирском институте органической химии им. Н. Н. Ворожцова СО РАН созданы безопасные антидиабетические и противоатеросклеротические препараты, действующие сразу на несколько факторов, благодаря которым «агрессивный» макрофаг М1 превращается в «мирный» М2 (Dikalov et al., 2011). Большой интерес вызывают и растительные препараты, получаемые из винограда, черники и других растений с помощью механохимической технологии, разработанной в Институте химии твердого тела и механохимии СО РАН (Dushkin, 2010).
С помощью финансовой поддержки государства можно в самое ближайшее время создать отечественные средства для фармакологических и генетических манипуляций с макрофагами, благодаря которым появится реальная возможность превращать эти иммунные клетки из агрессивных врагов в друзей, помогающих организму сохранить или вернуть здоровье.
Литература
Душкин М. И. Макрофаг/пенистая клетка как атрибут воспаления: механизмы образования и функциональная роль // Биохимия, 2012. T. 77. C. 419—432.
Смирнов А. Н. Липидная сигнализация в контексте атерогенеза // Биохимия. 2010. Т. 75. С. 899—919.
Шварц Я. Ш., Свистельник А. В.Функциональные фенотипы макрофагов и концепция М1-М2-поляризации. Ч. 1 Провоспалительный фенотип. // Биохимия. 2012. Т. 77. С. 312—329.
Источник: scfh.ru
В очагах воспаления обнаруживаются три типа клеток: эпителиоидные клетки, гигантские клетки и макрофаги.
В гранулемах обычно обнаруживаются эпителиоидные клетки, которые, по-видимому, образуются из моноцитов крови, активированных в ходе иммунного ответа на чужеродный антиген, например при кожной реакции гиперчувствительности замедленного типа. Эпителиоидные клетки обладают многими морфологическими признаками макрофагов и несут рецепторы FС и С3. В целом они обладают меньшей фагоцитирующей активностью, чем макрофаги.
Другой тип клеток, ногоядерные гигантские клетки, образуются, по всей видимости, за счет слияния макрофагов, а не за счет деления ядер. Таких клеток два типа: клетки Ланганса с относительно небольшим числом ядер по периферии цитоплазмы; Клетки типа инородного тела, у которых множество ядер распределено по всей цитоплазме.
Когда воспаление спадает макрофаги исчезает либо в результате гибели, либо мигрируют из участка воспаления. Пока в этом вопросе нет ясности.
Купферовские клетки представляют собой оседлые макрофаги печени. Они граничат с кровотоком, что позволяет им постоянно контактировать с чужеродными агентами и другими иммуностимулирующими агентами. Анатомическое расположение между венами, несущими кровь от желудочно-кишечного тракта, и собственным кровотоком печени приводит к тому, что купферовские клетки одними из первых в ряду мононуклеарных фагоцитов взаимодействуют с иммуногенами, поглощаемыми из кишечника. Как и другие тканевые макрофаги, купферовские клетки являются долгоживущими потомками моноцитов, которые поселились в печени и дифференцировались в макрофаги. Они живут в печени в среднем около 21 дня. Важнейшая функция купферовских клеток заключается в поглощении и деградации растворенных и нерастворимых материалов, приносимых в печень воротной веной. Они играют важнейшую роль в очистке кровотока от множества потенциально вредных биологических материалов, включая бактериальные эндотоксины, микроорганизмы, активированные факторы свертывания и растворимые иммунные комплексы.
В соответствии со своей функцией купферовские клетки содержат необычайно большое количество лизосом, содержащих кислые гидролазы и способных к активному внутриклеточному перевариванию.
Недавние исследования высокоочищенных купферовских клеток in vitro показали, что они способны функционировать как антигенпрезентирующие клетки во многих известных тестах на способность активировать Т-клетки.
Видимо, in vivo они не способны участвовать в индукции иммунного ответа под влиянием анатомических и физиологических особенностей нормального печеночного окружения.
Альвеолярные макрофагивыстилают альвеолы и являются первыми иммунологически компетентными клетками, поглощающими вдыхаемые патогены. Находящиеся на поверхности альвеол макрофаги идеально расположены для того, чтобы взаимодействовать с антигеном и затем представлять его Т-лимфоцитам. Альвеолярные макрофаги морской свинки оказались весьма активными вспомогательными клетками в тестах на пролиферацию Т-лимфоцитов, индуцированную как антигеном, так и митогеном. Было показано, что антиген, введенный животному в трахею, может индуцировать первичный иммунный ответ и вызывать избирательное обогащение специфических к нему Т-клеток в легких.
Макрофаг как эффекторная клетка.Механизм регуляции взаимодействия макрофагов с тимоцитами можно разделить на два аспекта. Первый: В результате взаимодействия активируются Т-клетки, вследствие чего у них появляется хелперная функция и, как результат, защитная иммунная реакция. Второй аспект участия макрофагов в иммунном ответе на инфекционные агенты и опухолевые клетки включает в себя их активацию. Для развития активного состояния макрофагов необходимо их взаимодействие со стимулированными Т-лимфоцитами или их продуктами: фактор хемотаксиса макрофагов (ФХМ), фактор тормозящий миграцию (ФТМ), фактор активирующий макрофаги (ФАМ).
В результате имеет место замкнутый цикл: АГ® МКФ® Т-клетка® МКФ® АГ.В результате антиген активно элиминируется.
 |
Таким образом, фагоцит выполняет двойную функцию: с одной стороны, он традиционно играет роль “мусорщика” убирающего антигены, а с другой стороны, перерабатывая антиген мобилизует и стимулирует лимфоциты.
В большом количестве работ было установлено, что существует положительная корреляция между активацией макрофагов и их способностью секретировать Н2О2. Инкубация макрофагов в среде, богатой лимфокинами, приводила к их активации и к выделению перекиси. Способность макрофагов секретировать реакционноспособные производные кислорода строго коррелирует со степенью их активации, определяемой по способности убивать определенные патогенные внутриклеточные микроорганизмы. Наличие такой корреляции, по-видимому, отражает прямое участие этих веществ в уничтожении микробов. Несомненно, однако, что макрофаги обладают и независимыми от кислорода важными механизмами антимикробной активности. Создается также впечатление, что некоторые одинаковые биохимические процессы используются макрофагами и для модификации их окружения и переработки фагоцитированных частиц. Так, например, окислительные механизмы участвуют не только в подавлении внутриклеточных паразитов, но также в уничтожении опухолевых клеток, а возможно, и некоторых тканей в местах воспаления.
Макрофаги секретируют множество разных продуктов.И в этом отношении могут соперничать даже с гепатоцитами. К наиболее важным продуктам секреции макрофагов относятся протеазы, активурующиеся при нейтральном значении рН, многие компоненты комплемента, кислые гидролазы и многие другие.
Цитоплазма макрофагов содержит большое количество лизосом, содержащих набор разнообразных гидролитических ферментов в отношении белков, углеводов, липидов и нуклеиновых кислотх. Пероксдазы, каталазы и NADH обеспечивают выделение высокобактериоцидного аниона О2— .Супероксиддесмутаза защищает макрофаг от собственного О2—.. Слияние фагосомы с лизосомой приводит к образованию фагодизосомы и к перевариванию (разрушению, лизису) фагоцитируемой частицы.
В случае захвата микроорганизма проявляется микробоцидное действие.
Фагоцитарная активность повышается в присутствии антител против данного чужеродного агента. Дело в том, что на мембране макрофагов имеются FС-рецепторы, которые специфически связываются с тяжелой цепью иммуноглобулинов (IgG). Присоединившиеся к макрофагу молекулы антител содействуют захвату фагоцитируемых частиц . Имеются также рецепторы к С3-компоненту комплемента. Вот почему антигенные частицы, покрытые антителами и комплементом, активно присоединяются к рецепторам макрофагов и фагоцитируются.
Таким образом, функция макрофагов не ограничивается захватом и разрушением чужеродных частиц. Макрофаги презентируют обработанный антиген Т-лимфоциту, то есть принимают участие в самом начальном акте, инициирующем иммунный ответ. На следующем этапе –этапе взаимодействия Т- и В-клеток, макрофаги опосредуют этот процесс, выступая в роли клетки, которая передает от Т-лимфоцита согнал включения В-лимфоциту. Важной функцией макрофагов является удаление избыточного количества антигенного материала, который может заблокировать иммунный ответ. Кроме того, макрофаги являются активно секретирующими клетками. Они вырабатывают ряд компонентов системы комплемента (факторы С2, С3, С4 и С5). Они вырабатывают лизоцим, интерферон, митогенный белок с молекулярной массой 15 000 дальтон, который стимулирует синтез ДНК в лимфоцитах, и цитотоксины, способные при определенных условиях убивать раковые клетки. Кроме того, макрофагами выделяются дифференцировочные факторы:
колониестимулирующий фактор – необходим стволовым кроветворнм клеткам для их дифференцировки в гранулоцитарном направлении;
фактор, содействующий созреванию Т-лимфоцитов.
И в завершение ко всему сказанному выше следует добавить, что макрофагам свойственно и супрессирующее действие, то есть они участвуют и в самоограничении иммунного ответа.
Макрофаги играют важную роль в активации лимфоцитов, хотя им не свойственна иммунологическая специфичность. Выяснилось, что нормальные макрофаги, макрофаги толерантного донора и макрофаги иммунных людей функционируют одинаково хорошо.
Результаты многочисленных исследований демонстрируют абсолютную необходимость участия макрофагов в активации антиген-специфических Т-клеток и показывают, что макрофаги должны быть первыми клетками в культуре, которые взаимодействуют с антигеном.
Тем не менее трудно исключить возможность прямой активации лимфоцитов антигеном.
Ранние эксперименты показали, что после премирования антигеном лимфоидные клетки становятся менее зависимыми от макрофагов, — вторичный иммунный ответ может развиваться и в их отсутствие. Пониженная зависимость от макрофагов появлялась лишь через 7-10 дней после иммунизации, но сохранялась при однократном введении антигена по меньшей мере в течение года. Объясняется это, возможно, тем, что активированные В-лимфоциты могут сами стимулировать иммунные Т-хелперные клетки без участия макрофагов. Возможно, наиболее эффективный, хотя несомненно не единственный, путь активации Т-хелперов при вторичном иммунном ответе заключается в прямой презентации Т-хелеперной клетке антигена, связанного с премированной антиген-специфической В-клеткой, и последующей активации дифференцировки В-клетки в непосредственной близости от Т-хелпера.
Общее заключение, которое можно сделать из приведенных выше данных сводится к тому, что функция вспомогательных клеток – это презентация антигена Т-лимфоцитам и обеспечение тем самым образования антител на тимусзависимые антигены.
Функция же вспомогательных клеток при ответе на Т-независимый антиген может заключаться в презентации антигена непосредственно В-клеткам. Способность В-клеток реагировать на активационные сигналы вспомогательных клеток может приобретаться по мере того, как В-клетки созревают и дифференцируются.
Результаты исследований по изучению процессинга антигена макрофгами дают право сделать некоторые выводы.Можно считать установленным, что при презентации антигена Т-клетке фрагмент антигена или сам нативный антиген присутствует на поверхности макрофага. Ясно также, что поглощение антигена макрофагом — это процесс температурозависимый, требующий затраты метаболической энергии, а не пассивное присоединение антигена к поверхности макрофага.
В настоящее время не ясно, представляют ли поглощение антигена и его протеолитический распад необходимый этап переработки антигена или же несущественную деталь, зависящую от природы исследуемого агента.
Источник: studopedia.ru