Клеточная стенка растений состоит из полисахаридов
В отличие от животных и многих простейших, у растений, бактерий и грибов, почти все клетки имеют стенку, лежащую кнаружи от цитоплазматической мембраны и обладающую повышенной прочностью. Основная функция данной структуры — опора и защита.
Клеточные стенки (или клеточные оболочки) строятся из веществ, синтезируемых самими клетками. Их химический состав различен у растений, грибов и прокариот. Кроме того, даже у одного растения у различных клеток состав стенок несколько различен.
Клеточная стенка растений состоит в основном из целлюлозы. Целлюлоза — это полисахарид, мономером которого является глюкоза.
Основу бактериальных клеточных стенок составляет вещество муреин (относится к пептидогликанам). У грамположительных бактерий в состав оболочки входят различные кислоты, а сама оболочка плотно прилегает к цитоплазматической мембране. У грамотрицательных бактерий оболочка более тонкая и не прилегает к мембране. Между мембраной и оболочкой образуется периплазматическое пространство. Снаружи клеточная оболочка грамотрицательных прокариот окружена внешней мембраной, составленной из липополисахарида.
У грибов основным веществом клеточных стенок является хитин, а не целлюлоза.
Состав клеточной стенки растений
У растений стенка дочерних клеток образуется уже во время деления родительской. Впоследствии она называется первичной. У многих клеток позже образуется вторичная оболочка.
Первичная клеточная оболочка состоит из микрофибрилл целлюлозы, погруженных в матрикс из других полисахаридов. Отличительной особенностью волокон целлюлозы является их прочность. Молекула целлюлозы представляет собой длинную полисахаридную цепь. Отдельные молекулы соединяются друг с другом водородными связями в пучок, который называется микрофибриллой. Такие фибриллы образуют каркас клеточной стенки.
Матрикс клеточной стенки составляют полисахариды пектины и гемицеллюлозы, а также ряд других веществ (например, белков). Пектиновые вещества представляют собой группу кислых полисахаридов, их молекулы могут быть не только линейными, но и разветвленными. Гемицеллюлозы также смешанная группа полисахаридов. Длина их линейных молекул короче, чем у целлюлозы.
Оболочки соседних клеток растений соединены между собой срединной пластинкой, состоящих из пектатов магния и кальция, для которых характерна клейкость.

В состав стенок растений входит вода (составляет более половины массы), обуславливая ряд физических и химических свойств полисахаридов.
Жесткий каркас растения во многих местах пронизан каналами (плазмодесмами), по которым цитоплазма одной клетки соединяется с цитоплазмой соседних.
Клетки мезофилла листа (а также некоторые другие) на протяжении всей своей жизни имеют только первичную стенку. У большинства же клеток на первичную оболочку с внутренней стороны отлагается вторичная стенка, составленная из дополнительных слоев целлюлозы. Обычно в это время клетка уже дифференцирована и не растет (исключение составляют, например, клетки колленхимы).
В каждом отдельном слое вторичного утолщения микрофибриллы целлюлозы располагаются под одним углом (параллельно друг другу). Однако разные слои имеют разный угол, что обеспечивает большую прочность.
Часть клеток растений одревесневают (трахеальные элементы ксилемы, склеренхима и др.). В основе этого процесса лежит интенсивная лигнификация стенок (в небольших количествах лигнин есть во всех оболочках). Лигнин не является полисахаридом, а представляет собой сложное полимерное вещество. Отложения лигнина могут иметь различную форму (сплошную, кольцевую, спиральную, сетчатую). Он скрепляет целлюлозу, не дает ей смещаться. Лигнин не только обеспечивает прочность, но и дает дополнительную защиту от неблагоприятных физических и химических факторов.
Функции клеточной стенки
Оболочки разных клеток совместно обеспечивают всему растению и его отдельным частям механическую прочность и опору. Это функция клеточной стенки аналогична одной из функций скелета животных. Однако она не единственная.
Жесткость стенок препятствует растяжению клеток и их разрыву. В результате по физическим законам в клетки может путем осмоса поступать вода. Для травянистых растений тургоцентричность клеток является единственной их опорой.
Микрофибриллы целлюлозы ограничивают рост клеток и определяют их форму. Если микрофибриллы окольцовывают клетку, то она будет расти в длину (поперек направления волокон).
Связанные клеточные стенки образуют апопласт, по которому передвигается вода и минеральные вещества. Плазмодесмы связывают содержимое разных клеток в единую систему — симпласт.
Стенки сосудов ксилемы, трахеид, ситовидных трубок выполняют транспортную функцию.
Наружные клеточные стенки эпидермальных клеток покрыты воском (кутикулой). С одной стороны, он препятствует испарению воды, с другой – проникновению вредных микроорганизмов.
У некоторых растений в определенных клетках оболочки видоизменяются и служат местом запаса питательных веществ.
Источник: biology.su
Пояснение.
Клеточная стенка растений состоит из полисахаридов. Ответ: 1
Клеточная стенка представляет собой жесткую и плотную оболочку, расположенную над цитоплазматической мембраной. Этот элемент характерен для клеток бактерий, грибов и растений.
В растительной клеточной стенке принято выделять три основных компонента: каркас, матрикс и инкрустирующие вещества.
Каркас клеточной стенки растения состоит из целлюлозы. Благодаря образованию водородных связей, молекулы целлюлозы образуют прочные микрофибриллы, которые погружены в основное вещества, или матрикс. Матрикс клеточной оболочки составляет примерно 60% общей ее массы. Он заполняет пространство между микрофибриллами, а также создает прочные связи между макромолекулами, обеспечивает эластичность и прочность этой клеточной структуры.
Основными компонентами матрикса являются гемицеллюлоза и пектин. Гемицеллюлоза представляет собой полисахарид, по структуре своей сходный с целлюлозой, но с более короткими и разветвленными цепями мономеров. Пектиновые вещества также относятся к полисахаридам, но в их состав также входят остатки метилового спирта. Благодаря образованию химических связей с ионами кальция и магния, пектин берет участие в формировании серединных пластинок — мест, где две соседние клетки соединяются между собой. Кстати, большое количество пектина содержится в плодах растений.
Инкрустирующие вещества в большинстве случаев представлены лигнином, которые составляет примерно 30% сухой массы клеточной стенки.
гнин может откладываться как в виде сплошного слоя, так и в форме отдельных элементов — спиралей, сеток или колец. Это вещество действует как цемент — оно скрепляет волокна целлюлозы между собой. Лигнин не является самостоятельным веществом, а представляет собой смесь ароматических полимеров. Благодаря лигнификации, клеточная стенка становиться более стойкой и мене водопроницаемой. Кстати, именно лигнин отвечает за одревеснение растений.
Довольно часто на внешнюю поверхность клеточной оболочки откладываются такие вещества, как кутин, суберин и воск.
Источник: bio-ege.sdamgia.ru
- ПРЕДИСЛОВИЕ РЕДАКТОРОВ ПЕРЕВОДА
- ПРЕДИСЛОВИЕ
- Благодарности
- ЧАСТЬ I. БИОМОЛЕКУЛЫ
ГЛАВА 1. БИОХИМИЯ-МОЛЕКУЛЯРНАЯ ЛОГИКА ЖИВЫХ ОРГАНИЗМОВ
- 1.1. Для живой материи характерны некоторые отличительные особенности
- 1.2. Биохимия стремится понять природу живого состояния
- 1.3. Все живые организмы содержат органические макромолекулы, построенные по общему плану
- 1.4. Обмен веществ и энергии в живых организмах
- 1.5. Ферменты, играющие роль катализаторов в живых клетках, управляют сложно организованной сетью химических реакций
- 1.6. Клетки используют энергию в химической форме
- 1.7. Процессы клеточного метаболизма находятся под постоянным контролем
- 1.8. Живые организмы способны к точному самовоспроизведению
ГЛАВА 2. КЛЕТКИ
- 2.1. Все клетки обладают некоторыми общими структурными характеристиками
- 2.2. Клетки должны иметь очень малые размеры
- 2.3. Существуют два больших класса клеток — прокариотические и эукариотические
- 2.4. Прокариоты — самые простые и самые мелкие клетки
- 2.5. Escherichia coli — самая известная из прокариотических клеток
- 2.6. Эукариотические клетки крупнее и сложнее прокариотических
- 2.7. Ядро эукариот — это очень сложная структура
- 2.8. Митохондрии — «силовые установки» эукариотических клеток, поставляющие энергию
- 2.9. Эндоплазматический ретикулум образует каналы в цитоплазме
- 2.10. Тельца Гольджи — секреторные органеллы
- 2.11. Лизосомы — контейнеры с гидролитическими ферментами
- 2.12. Пероксисомы — пузырьки, разрушающие перекись водорода
- 2.13. Микрофиламенты участвуют в сократительных процессах клеток
- 2.14. Микротрубочки также связаны с клеточными движениями
- 2.15. Микрофиламенты, микротрубочки и микротрабекулярная сеть образуют цитоскелет
- 2.16. Реснички и жгутики позволяют клеткам передвигаться
- 2.17. В цитоплазме содержатся также гранулярные тельца
- 2.18. Цитозоль — непрерывная водная фаза цитоплазмы
- 2.19. Клеточная мембрана имеет большую площадь поверхности
- 2.20. На поверхности многих животных клеток имеются также «антенны»
- 2.21. Эукариотические клетки растений имеют некоторые специфические особенности
- 2.22. Вирусы — надмолекулярные паразиты
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
ГЛАВА 3. СОСТАВ ЖИВОЙ МАТЕРИИ: БИОМОЛЕКУЛЫ
- 3.1. Химический состав живой материи отличается от химического состава земной коры
- 3.2. Большинство биомолекул содержит углерод
- 3.3. Биомолекулы имеют специфическую форму и определенные размеры
- 3.4. Функциональные группы органических биомолекул определяют их химические свойства
- 3.5. Многие биомолекулы асимметричны
- 3.6. Основные классы биомолекул в клетках представлены очень крупными молекулами
- 3.7. Макромолекулы образуются из небольших молекул, играющих роль строительных блоков
- 3.8. Молекулы, используемые в качестве строительных блоков, имеют простую структуру
- 3.9. Структурная иерархия в молекулярной организации клеток
- 3.10. Биомолекулы первыми возникли в процессе химической эволюции
- 3.11. Химическую эволюцию можно воспроизвести в лабораторных условиях
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
ГЛАВА 4. ВОДА
- 4.1. Необычные физические свойства воды обусловлены ее способностью участвовать в образовании водородных связей
- 4.2. Водородные связи широко распространены в биологических системах и играют в них важную роль
- 4.3. Вода как растворитель обладает необычными свойствами
- 4.4. Растворенные вещества изменяют свойства воды
- 4.5. Состояние равновесия обратимых реакций характеризуется константой равновесия
- 4.6. Ионизацию воды можно охарактеризовать величиной константы равновесия
- 4.7. Шкала pH: обозначения концентраций ионов Н+ и ОН-
- 4.8. Свойства кислот и оснований тесно связаны со свойствами воды
- 4.9. Слабые кислоты имеют характерные кривые титрования
- 4.10. Буферы — это смеси слабых кислот и сопряженных с ними оснований
- 4.11. Фосфат и бикарбонат — важные биологические буферные системы
- 4.12. Приспособленность живых организмов к водной среде
- 4.13. «Кислые» дожди загрязняют наши озера и реки
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 5. АМИНОКИСЛОТЫ И ПЕПТИДЫ
- 5.1. Общие структурные свойства аминокислот
- 5.2. Почти все аминокислоты содержат асимметрический атом углерода
- 5.3. Стереоизомеры обозначаются в соответствии с их абсолютной конфигурацией
- 5.4. Оптически активные аминокислоты в белках представляют собой L-стереоизомеры
- 5.5. Классификация аминокислот на основе их R-групп
- 5.6. Восемь аминокислот содержат неполярные R-группы
- 5.7.
мь аминокислот содержат незаряженные полярные R-группы
- 5.8. Две аминокислоты содержат отрицательно заряженные (кислые) R-группы
- 5.9. Три аминокислоты содержат положительно заряженные (основные) R-группы
- 5.10. В некоторых белках присутствуют нестандартные аминокислоты
- 5.11. В водных растворах аминокислоты ионизированы
- 5.12. Аминокислоты могут вести себя и как кислоты, и как основания
- 5.13. Аминокислоты имеют характерные кривые титрования
- 5.14. По кривой титрования можно предсказать, какой электрический заряд несет данная аминокислота
- 5.15. Аминокислоты различаются по своим кислотно-основным свойствам
- 5.16. Кислотно-основные свойства аминокислот служат основой для аминокислотного анализа
- 5.17. Электрофорез на бумаге позволяет разделять аминокислоты в соответствии с их электрическим зарядом
- 5.18. Ионообменная хроматография служит более эффективным способом разделения аминокислот
- 5.19. Химические реакции, характерные для аминокислот
- 5.20. Пептиды — это цепочки аминокислот
- 5.21. Разделение пептидов может быть основано на различиях в их ионизационных свойствах
- 5.22. Химические реакции, характерные для пептидов
- 5.23. Некоторые пептиды обладают высокой биологической активностью
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 6. БЕЛКИ: КОВАЛЕНТНАЯ СТРУКТУРА И БИОЛОГИЧЕСКИЕ ФУНКЦИИ
- 6.1. Белки обладают множеством различных биологических функций
- 6.2. Белки можно классифицировать также по форме их молекул
- 6.3. В ходе гидролиза брлки распадаются на аминокислоты
- 6.4. Некоторые белки имеют в своем составе не только аминокислоты, но и другие химические группы
- 6.5. Белки — это очень крупные молекулы
- 6.6. Белки можно выделить и подвергнуть очистке
- 6.7. Определение аминокислотной последовательности полипептидных цепей
- 6.8. Инсулин — это первый белок, для которого была установлена аминокислотная последовательность
- 6.9. В настоящее время известны последовательности многих других белков
- 6.10. Гомологичные белки разных видов имеют гомологичные последовательности
- 6.11. Различия между гомологичными белками можно выявить по иммунной реакции
- 6.12. Белки претерпевают структурные изменения, называемые денатурацией
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
ГЛАВА 7. ФИБРИЛЛЯРНЫЕ БЕЛКИ
- 7.1. Термины «конфигурация» и «конформация» имеют разный смысл
- 7.2. Как это ни парадоксально, нативные белки имеют только одну или всего лишь несколько конформаций
- 7.3. a-Кератины — фибриллярные белки, синтезируемые клетками эпидермиса
- 7.4. Рентгеноструктурный анализ показывает, что в кератинах имеются повторяющиеся структурные единицы
- 7.5. Рентгеноструктурные исследования пептидов свидетельствуют о жесткости и плоской конфигурации пептидных групп
- 7.6. В a-кератине полипептидные цепи имеют форму a-спирали
- 7.7. Некоторые аминокислотные остатки препятствуют образованию a-спирали
- 7.8. В a-кератинах содержится много аминокислот, способствующих образованию a-спиральной структуры
- 7.9. В нативных a-кератинах a-спиральные полипептидные цепи скручены наподобие каната
- 7.10. a-Кератины нерастворимы в воде из-за преобладания в их составе аминокислот с неполярными R-группами
- 7.11. b-Кератины имеют другую конформацию полипептидной цепи, называемую b-структурой
- 7.12. Перманентная завивка волос — пример биохимической технологии
- 7.13. Коллаген и эластин — главные фибриллярные белки соединительных тканей
- 7.14. Коллаген — самый распространенный белок у высших животных
- 7.15. Коллаген обладает как обычными, так и необычными свойствами
- 7.16. Полипептиды в коллагене представляют собой трехцепочечные спиральные структуры
- 7.17. Структура эластина придает особые свойства эластической ткани
- 7.18. Что говорят нам фибриллярные белки о структуре белков?
- 7.19. Другие типы фибриллярных или нитевидных белков встречающихся в клетках
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
ГЛАВА 8. ГЛОБУЛЯРНЫЕ БЕЛКИ: СТРУКТУРА И ФУНКЦИЯ ГЕМОГЛОБИНА
- 8.1. Полипептидные цепи глобулярных белков свернуты в плотную компактную структуру
- 8.2. Рентгеноструктурный анализ миоглобина — выдающееся достижение в исследовании белков
- 8.3. Миоглобины, выделенные из разных видов, имеют сходную конформацию
- 8.4. Глобулярные белки различных типов имеют неодинаковую структуру
- 8.5. Аминокислотная последовательность белка определяет его третичную структуру
- 8.6. Силы, стабилизирующие третичную структуру глобулярных белков
- 8.7. Свертывание полипептидных цепей происходит с очень высокой скоростью
- 8.8. Олигомерные белки имеют как третичную, так и четвертичную структуру
- 8.9. Метод рентгеноструктурного анализа позволил установить как третичную, так и четвертичную структуру гемоглобина
- 8.10. По своей третичной структуре a- и b-цепи гемоглобина очень сходны с миоглобином
- 8.11. Была установлена четвертичная структура и некоторых других олигомерных белков
- 8.12. Эритроциты — специализированные клетки, переносящие кислород
- 8.13. Для миоглобина и гемоглобина характерны разные кривые связывания кислорода
- 8.14. Кооперативное связывание кислорода делает гемоглобин более эффективным переносчиком кислорода
- 8.15. Гемоглобин служит также переносчиком С02 и ионов H+
- 8.16. Оксигенация гемоглобина вызывает изменение его пространственной конформации
- 8.17. Серповидноклеточная анемия — «молекулярная болезнь» гемоглобина
- 8.18. Гемоглобин больных серповидноклеточной анемиеи имеет измененную аминокислотную последовательность
- 8.19. Серповидная форма эритроцитов обусловлена склонностью молекул гемоглобина S к агрегации
- 8.20. «Неправильные» аминокислоты появляются в белках в результате генных мутаций
- 8.21. Можно ли найти «молекулярное лекарство» для серновидноклеточного гемоглобина?
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ГЛАВА 9. ФЕРМЕНТЫ
- 9.1. История биохимии — это в значительной мере история исследования ферментов
- 9.2. Ферменты обнаруживают все свойства белков
- 9.3. Ферменты классифицируются на основе реакций, которые они катализируют
- 9.4. Ферменты ускоряют химические реакции, снижая энергию активации
- 9.5. Концентрация субстрата оказывает огромное влияние на скорость реакций, катализируемых ферментами
- 9.6. Существует количественная связь между концентрацией субстрата и скоростью ферментативной реакции
- 9.7. Каждый фермент имеет характерную величину Км для данного субстрата
- 9.8. Многие ферменты катализируют реакции с участием двух субстратов
- 9.9. Каждый фермент имеет определенный оптимум pH
- 9.10. Количество фермента можно определить по его активности
- 9.11. Ферменты проявляют специфичность по отношению к своим субстратам
- 9.12. Ферменты можно ингибировать определенными химическими соединениями
- 9.13. Существуют обратимые ингибиторы двух типов — конкурентные и неконкурентные
- 9.14. Неконкурентное ингибирование тоже обратимо, но не может быть ослаблено или устранено повышением концентрации субстрата
- 9.15. Факторы, определяющие каталитическую эффективность ферментов
- 9.16. Рентгеноструктурный анализ выявил важные структурные особенности ферментов
- 9.17. В ферментных системах есть «дирижер», роль которого выполняет регуляторный фермент
- 9.18. Аллостерические ферменты регулируются путем нековалентного присоединения к ним молекул модуляторов
- 9.19. Аллостерические ферменты ингибируются или активируются их модуляторами
- 9.20. Поведение аллостерических ферментов не описывается уравнением Михаэлиса — Ментеи
- 9.21. Субъединицы аллостерических ферментов сообщаются между собой
- 9.22. Некоторые ферменты регулируются путем обратной ковалентной модификации
- 9.23. Многие ферменты существуют в нескольких формах
- 9.24. Нарушение каталитической активности ферментов может быть обусловлено мутациями
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
ГЛАВА 10. ВИТАМИНЫ И МИКРОЭЛЕМЕНТЫ: ИХ РОЛЬ В ФУНКЦИОНИРОВАНИИ ФЕРМЕНТОВ
- 10.1. Витамины — незаменимые органические микрокомпоненты пищи
- 10.2. Витамины являются важными компонентами коферментов и простетических групп ферментов
- 10.3. Витамины можно разделить на два класса
- 10.4. Тиамин (витамин B1) функционирует в форме тиаминпирофосфата
- 10.5. Рибофлавин (витамин В2) — компонент флавиновых нуклеотидов
- 10.6. Никотинамид — это активная группа коферментов NAD и NADP
- 10.7. Пантотеновая кислота — компонент кофермента А
- 10.8. Пиридоксин (витамин В6) играет важную роль в метаболизме аминокислот
- 10.9. Биотин является активным компонентом биоцитина — простетической группы некоторых ферментов, катализирующих реакции карбоксилирования
- 10.10. Фолиевая кислота служит предшественником кофермента тетрагидрофолиевой кислоты
- 10.11. Витамин B12 — предшественник кофермента В12
- 10.12. Биохимическая функция витамина С (аскорбиновой кислоты) не известна
- 10.13. Жирорастворимые витамины представляют собой производные изопрена
- 10.14. Витамин А, вероятно, выполняет несколько функций
- 10.15. Витамин D — предшественник гормона
- 10.16. Витамин Е защищает клеточные мембраны от кислорода
- 10.17. Витамин К-компонент карбокснлнрукнцего фермента
- 10.18. В пище животных должны содержаться многочисленные неорганические вещества
- 10.19. Для действия многих ферментов требуется железо
- 10.20. В некоторых окислительных ферментах содержится также медь
- 10.21. Для действия многих ферментов необходим цинк
- 10.22. Некоторым ферментам требуются ионы марганца
- 10.23. В состав витамина В12 входит кобальт
- 10.24. Селен является и незаменимым микроэлементом, и ядом
- 10.25. Для некоторых ферментов требуются другие микроэлементы
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и залами
ГЛАВА 11. УГЛЕВОДЫ: СТРОЕНИЕ И БИОЛОГИЧЕСКИЕ ФУНКЦИИ
- 11.1. Углеводы делятся на три класса в зависимости от числа остатков сахаров
- 11.2. Существует два семейства моносахаридов: альдозы и кетозы
- 11.3. Моносахариды обычно содержат несколько асимметрических центров
- 11.4. Типичные моносахариды имеют циклическую структуру
- 11.5. Простые моносахариды могут служить восстановителями
- 11.6. Дисахариды содержат две моносахаридные единицы
- 11.7. Полисахариды содержат большое число моносахаридных остатков
- 11.8. Некоторые полисахариды представляют собой форму запасания «клеточного топлива»
- 11.9. Целлюлоза — наиболее распространенный структурный полисахарид
- 11.10. Клеточные стенки содержат в больших количествах структурные и защитные полисахариды
- 11.11. Гликопротеины — гибридные молекулы
- 11.12. На поверхности клеток животных присутствуют гликопротеины
- 11.13. Гликозаминогликаны и протеогликаны — важные компоненты соединительной ткани
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
ГЛАВА 12. ЛИПИДЫ И МЕМБРАНЫ
- 12.1. Жирные кислоты — структурные компоненты большинства липидов
- 12.2. Триацилглицеролы — это глицероловые эфиры жирных кислот
- 12.3. Триацилглицеролы — форма запасания липидов
- 12.4. Воска — эфиры жирных кислот и длинноцепочечных спиртов
- 12.5. Фосфолипиды — основные липидные компоненты мембран
- 12.6. Сфинголипиды — также важные компоненты мембран
- 12.7. Стероиды — неомыляемые липиды, обладающие специфическими функциями
- 12.8. Липопротеины сочетают свойства липидов и белков
- 12.9. Полярные липиды образуют мицеллы, монослои и бислои
- 12.10. Полярные липиды и белки — основные компоненты мембран
- 12.11. Мембраны имеют жидкостно-мозаичную структуру
- 12.12. Мембраны асимметричны, т.е. имеют неравноценные стороны
- 12.13. Мембраны эритроцитов исследованы очень подробно
- 12.14. Лектины — специфические белки, способные связываться с определенными клетками и вызывать их агглютинацию
- 12.15. Мембраны имеют очень сложные функции
- Краткое содержание главы
- ЛИТЕРАТУРА
- Вопросы и задачи
- ПРИЛОЖЕНИЕ ОТВЕТЫ
Источник: scask.ru
Структура клеточной стенки растений
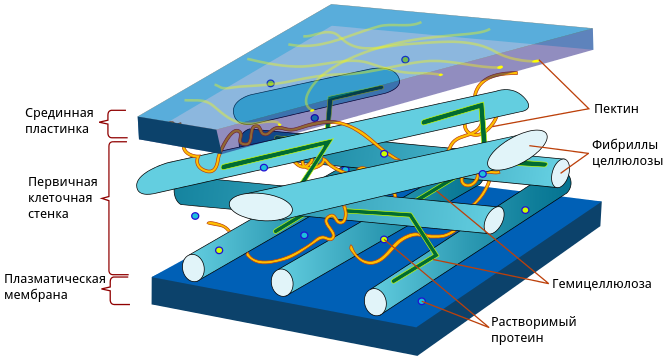
Клеточная стенка растений многослойная и включает три секции: внешний слой или средняя пластинка, первичная и вторичная клеточные стенки. Хотя все растительные клетки имеют среднюю пластинку и первичную клеточную стенку, не у всех есть вторичная клеточная стенка.
Средняя пластинка — внешней слой клеточной стенки, который содержит полисахариды, называемые пектинами. Пектины помогают в адгезии клеток, связывая стенки соседних клеток друг с другом.
Первичная клеточная стенка — слой, образованный между средней пластинкой и плазматической мембраной в растущих клетках растений. Он состоит в основном из целлюлозных микрофибрилл, содержащихся в гелеобразной матрице из гемицеллюлозных волокон и пектиновых полисахаридов. Первичная клеточная стенка обеспечивает прочность и гибкость, необходимые для роста клеток.
Вторичная клеточная стенка — слой, образованный между первичной стенкой клетки и плазматической мембраной в некоторых растительных клетках. Когда первичная клеточная стенка перестает делиться и расти, она может сгущаться, образуя вторичную клеточную стенку. Этот прочный слой укрепляет и поддерживает клетку. Кроме целлюлозы и гемицеллюлозы, некоторые вторичные клеточные стенки включают лигнин, который усиливает их и обеспечивает водопроводимость клеток сосудистой ткани растений.
Функции клеточной стенки
Основные функции клеточной стенки заключаются в том, чтобы сформировать каркас для клетки и предотвратить ее расширение. Целлюлозное волокно, структурные белки и другие полисахариды придают клеткам форму и обеспечивают поддержку. К дополнительным функциям клеточной стенки относятся:
- Поддержка — обеспечение механической прочности и структуры, а также контроль направления роста клеток.
- Выдерживает тургорное давление — сила воздействия содержимого клетки (протопласта) на ее стенки. Это давление помогает растению оставаться жестким и прямостоящим, но может также вызвать разрушение клетки.
- Регулировка роста — посылает сигналы клеткам для входа в клеточный цикл, чтобы делится и расти.
- Регулировка диффузии — пористая структура клеточной стенки позволяет некоторым необходимым веществам, включая белки, попадать внутрь клетки, препятствуя проникновению других.
- Связь — клетки взаимодействуют между собой через плазмодесмы (поры или каналы между стенками растительных клеток, которые позволяют молекулам и сигналам связи проходить между отдельными клетками растения).
- Защита — осуществляет защиту клеток от вирусов и остальных опасных веществ или микроорганизмов, а также помогает предотвратить потерю воды.
- Хранение — хранит углеводы, которые используются для роста растений, особенно в семенах.
Источник: natworld.info
Источник: chem21.info