Пигменты хлоропластов
ХЛОРОПЛАСТЫ (от греч. chloros — зелёный и plastos — вылепленный), внутриклеточные органоиды (пластиды) растений, в к-рых осуществляется фотосинтез; благодаря хлорофиллу окрашены в зелёный цвет. Встречаются в клетках разл. тканей надземных органов растений, особенно обильны и хорошо развиты в листьях и зелёных плодах. Дл. 5— 10 мкм, шир. 2—4 мкм. В клетках высших растений X. (чаще их 15—50) имеют линзовидно-округлую или эллипсоидную форму. X. отделены от цитоплазмы двойной мембраной, обладающей избирательной проницаемостью; внутренняя её часть, врастая в матрикс, образует систему осн. структурных единиц X. в виде уплощённых мешков — тилакоидов, в к-рых локализованы пигменты: основные — хлорофиллы и вспомогательные — каротиноиды. Группы дисковидных тилакоидов, связанных друг с другом таким образом, что их полости оказываются непрерывными, образуют (наподобие стопки монет) граны. Кол-во гран в X. высших растений может достигать 40—60 (иногда до 150). X. содержат рибосомы, ДНК, ферменты и, кроме фотосинтеза, осуществляют синтез АТФ из АДФ (фосфорилирование), синтез и гидролиз липидов, ассимиляционного крахмала и белков, откладываемых в строме.
X. синтезируются также ферменты, осуществляющие световую реакцию и белки мембран тилакоидов. Собственный генетич. аппарат и специфич. белоксинтезирующая система обусловливают относит, автономию X. от др. клеточных структур. Каждый X. развивается, как полагают, из пропластиды, к-рая способна реплицироваться путём деления (именно так увеличивается их число в клетке); зрелые X. иногда также способны к репликации. При старении листьев и стеблей, созревании плодов X. вследствие разрушения хлорофилла утрачивают зелёную окраску.
См 15 билет
Фотохимический этап фотосинтеза включает ряд последовательно протекающих процессов, локализованных в тилакоидных мембранах. Пигменты, специфически связанные с белками фотосинтетических мембран, и другие компоненты, необходимые для протекания реакций поглощения света и электронного транспорта, образуют надмолекулярные комплексы — фотосистему I (ФС I) и фотосистему II (ФС II). В составе каждой фотосистемы различают: реакционный центр, в котором происходят очень быстрые реакции первичного разделения зарядов; комплекс компонентов, по которым передается электрон от реакционного центра, и последний окисляется.
Физиологическая роль азота. Признаки его недостатка.
Основная функция и способность азота – образовывать пептидные связи и формировать все разнообразие белков, а также участвовать в составе множества биологически активных гетероциклов. Азот необходим всем живым организмам для синтеза азотсодержащих строительных блоков — аминокислот, из которых образуются белки и нуклеиновые кислоты. Растения добывают азот из почвы в виде растворимых нитратов и соединений аммиака.
Физиологическая роль азота в организме ассоциируется, прежде всего, с белками и аминокислотами, их метаболизмом, участием в жизненно-важных процессах и влиянием на эти процессы. Аминокислоты являются исходными соединениями при биосинтезе гормонов, витаминов, медиаторов, пигментов, пуриновых и пиримидиновых оснований и т.д.
Основные проявления дефицита азота:
многочисленные расстройства, отражающие нарушения обмена белков, аминокислот, азотсодержащих соединений и связанных с азотом биоэлементов.
Источник: studopedia.ru
Строение и функции хлоропластов
Хлоропласты — зеленые пластиды, содержащие зеленый пигмент — хлорофилл.
Основная функция хлоропласт — фотосинтез.
В хлоропластах есть свои рибосомы, ДНК, РНК, включения жира, зерна крахмала. Снаружи хлоропласта покрыты двумя белково-липидными мембранами, а в их полужидкую строму (основное вещество) погружены мелкие тельца — граны и мембранные каналы.
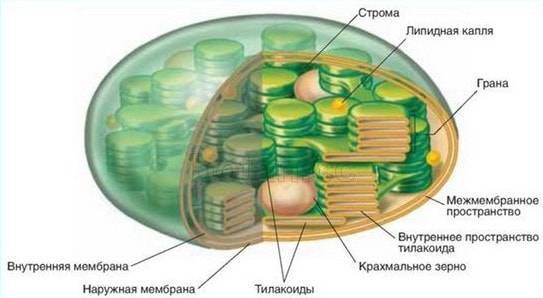
Граны (размером около 1мкм) — пакеты круглых плоских мешочков (тилакоидов), сложенных подобно столбику монет. Располагаются они перпендикулярно поверхности хлоропласта. Тилакоиды соседних гран соединены между собой мембранными каналами, образуя единую систему. Число гран в хлоропластах различно. Например, в клетках шпината каждый хлоропласт содержит 40-60 гран.
Хлоропласты внутри клетки могут двигаться пассивно, увлекаемые током цитоплазмы, либо активно перемещаться с места на место.
- Если свет очень интенсивен, они поворачиваются ребром к ярким лучам солнца и выстраиваются вдоль стенок, параллельных свету.
- При слабом освещении, хлоропласты перемещаются на стенки клетки, обращенные к свету, и поворачиваются к нему своей большой поверхностью.
- При средней освещенности они занимают среднее положение.
Этим достигаются наиболее благоприятные для процесса фотосинтеза условия освещения.
Хлорофилл
В гранах пластид растительной клетки содержится хлорофилл, упакованный с белковыми и фосфолипидными молекулами так, чтобы обеспечить способность улавливать световую энергию.
Молекула хлорофилла очень сходна с молекулой гемоглобина и отличается главным образом тем, что расположенный в центре молекулы гемоглобина атом железа заменен в хлорофилле на атом магния.
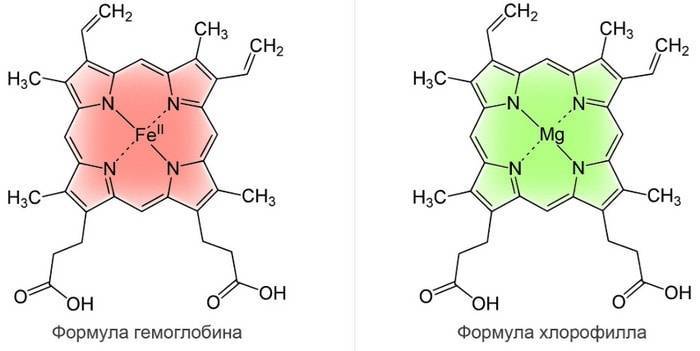
В природе встречается четыре типа хлорофилла: a, b, c, d.
Хлорофиллы a и b содержат высшие растения и зеленые водоросли, диатомовые водоросли содержат a и c, красные — a и d.
Лучше других изучены хлорофиллы a и b (их впервые разделил русский ученый М.С.Цвет в начале XXв.). Кроме них существуют четыре вида бактериохлорофиллов — зеленых пигментов пурпурных и зеленых бактерий: a, b, c, d.
Большинство фотосинтезирующих бактерий содержат бактериохлорофилл a, некоторые — бактериохлорофилл b, зеленые бактерии — c и d.
Хлорофилл обладает способностью очень эффективно поглощать солнечную энергию и передавать ее другим молекулам, что является его главной функцией. Благодаря этой способности хлорофилл — единственная структура на Земле, которая обеспечивает процесс фотосинтеза.
Главная функция хлорофилла в растениях — поглощение энергии света и передача ее другим клеткам.
Пластидам, так же, как и митохондриям, свойственна до некоторой степени автономность внутри клетки. Они размножаются путем деления.
Наряду с фотосинтезом, в пластидах происходит процесс биосинтеза белка. Благодаря содержанию ДНК пластиды играют определенную роль в передаче признаков по наследству (цитоплазматическая наследственность).
Строение и функции хромопластов
Хромопласты относятся к одному из трех видов пластид высших растений. Это небольших размеров, внутриклеточные органеллы.
Хромопласты имеют различный окрас: желтый, красный, коричневый. Они придают характерный цвет созревшим плодам, цветкам, осенней листве. Это необходимо для привлечения насекомых-опылителей и животных, которые питаются плодами и разносят семена на дальние расстояния.

Структура хромопласта похожа на другие пластиды. Их двух оболочек внутренняя развита слабо, иногда вовсе отсутствует. В ограниченном пространстве расположена белковая строма, ДНК и пигментные вещества (каротиноиды).
Каротиноиды – это жирорастворимые пигменты, которые накапливаются в виде кристаллов.
Форма хромопластов очень разнообразна: овальная, многоугольная, игольчатая, серповидная.
Роль хромопластов в жизни растительной клетки до конца не выяснена. Исследователи предполагают, что пигментные вещества играют важную роль в окислительно-восстановительных процессах, необходимы для размножения и физиологичного развития клетки.
Строение и функции лейкопластов
Лейкопласты — это органоиды клетки, в которых накапливаются питательные вещества. Органеллы имеют две оболочки: гладкую наружную и внутреннюю с несколькими выступами.
Лейкопласты на свету превращаются в хлоропласты (к примеру зеленые клубни картофеля), в обычном состоянии они бесцветны.
Форма лейкопластов шаровидная, правильная. Они находятся в запасающей ткани растений, которая заполняет мягкие части: сердцевину стебля, корня, луковиц, листьев.

Функции лейкопластов зависят от их вида (в зависимости от накапливаемого питательного вещества).
Разновидности лейкопластов:
- Амилопласты накапливают крахмал, встречаются во всех растениях, так как углеводы основной продукт питания растительной клетки. Некоторые лейкопласты полностью наполнены крахмалом, их называют крахмальными зернами.
- Элайопласты продуцируют и запасают жиры.
- Протеинопласты содержат белковые вещества.
Лейкопласты также служат ферментной субстанцией. Под действием ферментов быстрее протекают химические реакции. А в неблагоприятный жизненный период, когда процессы фотосинтеза не осуществляются, они расщепляют полисахариды до простых углеводов, которые необходимы растениям для выживания.
В лейкопластах не может происходить фотосинтез, потому что они не содержат гран и пигментов.
Луковицы растений, в которых содержится много лейкопластов, могут переносить длительные периоды засухи, низкую температуру, жару. Это связано с большими запасами воды и питательных веществ в органеллах.
Предшественниками всех пластид является пропластиды, небольшие органоиды. Допускают, что лейко — и хлоропласты способны трансформироваться в другие виды. В конечном итоге после выполнения своих функций хлоропласты и лейкопласты становятся хромопластами — это последняя стадия развития пластид.
Важно знать! Одновременно в клетке растения может находиться только один вид пластид.
Источник: animals-world.ru
 |
|
| Астрономия Биология География Дом и сад Другие языки Другое Информатика История Культура Литература Логика Математика Медицина Металлургия Механика Образование Охрана труда Педагогика Политика Право Психология Религия Риторика Социология Спорт Строительство Технология Туризм Физика Философия Финансы Химия Черчение Экология Экономика Электроника |
К. играют роль вспомогательных светособирающих пигментов в той части солнечного спектра, где слабо поглощает хлорофилл. Это особенно важно для водных экосистем, куда проникают кванты синего и зеленого света и наблюдается дефицит квантов красного света, необходимых для возбуждения хлорофилла. Обязательным условием для передачи энергии от возбужденных светом каротиноидов на хлорофилл является частичное перекрывание электронных облаков молекул пигментов. Это достигается близким расположением Х и К в светособирающем комплексе. К. также выполняют ф-циифотопротекторов — защищают Х от фотоокисления на слишком ярком свету и подавляют процесс накопления возбужденного синглетного кислорода, препятствуя окислительному стрессу. Энергия возбуждения триплетного Х и синглетного кислорода резонансным путем передается на каротиноиды, а затем рассеивается в виде тепла. Ф-ции вспомогательных пигментов в антенных комплексах фотосистем I и II выполняют виолоксантин, лютеин и неоксантин. В процессе рассеивания энергии возбужденного светом Х принимает участие зеаксантин. Переключение ф-ций К с аккумулирования энергии света на ее рассеивание может происходить в виолоксантиновом (ксантофилловом) цикле: на сильном свету виолоксантин превращается вначале в антероксантин, а затем в зеаксантин (под д-ем фермента виолоксантиндеэпоксидазы; его активность увеличивается при высокой освещенности и снижении рН). Обратное превращение зеаксантина в виолоксантин происходит на слабом свету или в темноте с помощью фермента заексантинэпоксидазы. Т.о., в этом цикле В аккумулирует энергию света, а З рассеивает ее.
Фотофизические и фотохимические реакции фотосинтеза. Характеристика фотосистемы I и фотосистемы II. Эффект Эмерсона. Электрон-транспортная цепь хлоропласта. Образование кислорода при фотосинтезе. Световая фаза фотосинтеза состоит из трех этапов и включает в себя фотофизические и фотохимические процессы. Первый этап: фотофизический. Энергия света поглощается, переходит в энергию электронного возбуждения пигментов и передаётся в реакционный центр фотосистем. Эти фотофизические процессы протекают в светособирающих антенных комплексах. Второй этап: фотохимический. Энергия возбуждения пигментов используется для разделения зарядов в реакционном центре фотосистем. Это центральный момент фотосинтеза, потому что именно в этом процессе происходит преобразование физической формы энергии в химическую. Большая часть фотосинтетических пигментов тилакоидных мембран находится в форме пигмент-белковых комплексов, образуя фотосинтетические единицы (ФСЕ). Они включают антенный комплекс, функционально сопряженный с реакционным центром. Идея о существовании в хлоропластах двух фотосистем была высказана Р. Эмерсоном. Он изучал зависимость эффективности фотосинтеза от длины волны света. Объектом служила хлорелла, у неё он анализировал влияние света на квантовый выход фотосинтеза (к-во О2, выделившихся при фотосинтезе, в расчете на 1 квант поглощённой энергии). Эмерсон установил, что наиболее эффективен для фотосинтеза у хлореллы красный свет (650-680 нм) и синий свет (400-600 нм). Но если увеличивать длину волны, то квантовый выход фотосинтеза резко падает. Если же хлореллу освещать и коротковолновым и длинноволновым красным светом одновременно, то суммарный эффект будет выше, чем при действии каждого вида лучей в отдельности. Это явление носит название эффекта Эмерсона. Эти опыты показали, что для световых процессов фотосинтеза необходимо взаимодействие двух фотосистем. Фотосистема II высших растений и зеленых водорослей состоит из реакционного центра, который включает первичный донор электронов – димер хлорофилла а с максимумом поглощения 680 нм; два первичных акцептора электронов феофетина а; вторичные акцепторы – молекулы пластохинона. Ядро реакционного центра составляют два мембранных белка (D1 и D2.), они служат основой для связывания простетических групп реакционного центра, выполняющих функции переносчиков электронов. Другие белки формируют внутренний светособирающий комплекс, участвуют в выделении кислорода при фотоокислении воды или выполняют другие функции. В кислород-выделяющий комплекс входят Mn-содержащий кластер и кофакторы кальций и хлор. Остаток аминокислоты тирозина белка D1 выступает посредником между кислород-выделяющим комплексом и хлорофиллом. Фотосистема I высших растений и водорослейпредставляет собой интегральный пигмент-белковый комплекс, состоящий из 13 пептидов. В структуре комплекса выделяют центральную часть из двух крупных белков (А и В) и два периферийных домена — со стороны стромы (белки C, D и E) и стороны люмена (белки F и N). К комплексу белков фотосистемы I примыкают белки внешней антенны ССК I. Белки А, В и С включают первичный донор электронов — димер хлорофиллов а с максимумом поглощения 700 нм; по одному дополнительному хлорофиллу а; по одной молекуле первичного 700 П акцептора — мономера хлорофилла а ; по одной молекуле вторичного акцептора — витамина K1 , филлохинона; терминальные акцепторы — белки, содержащие железосерные ( Fe4S4 ) кластеры. От терминальных акцепторов электроны поступают на водорастворимый железосерный (Fe2S2) белок ферредоксин, а затем на растворимый флавопротеин —ферредоксин-НАДФ-редуктазу (ФНП). Двойной набор дополнительных хлорофиллов, первичных акцепторов и филлохинонов формируют две практически симметричные ветви транспорта электронов от П700 к FX . Комплекс цитохромовb6 /f состоит из цитохрома b6 (цит b6 ), цитохрома f (цит f), железосерного белка Риске (Fe2S2)R и субъединицы IV . Цитохром b6 и субъединица IV являются наиболее гидрофобными элементами комплекса. Основная часть молекулы цитохрома f расположена в полости тилакоида, в то время как ее С-концевой участок находится на его поверхности. Простетическая группа цитохрома f представлена гемом с-типа. Простетическую группу цитохрома b6 составляют два гема b-типа, ковалентно связанные с остатками гистидина. Эти два гема называют низкопотенциальным (L) и высокопотенциальным (H). От комплекса цитохромов b6 /f электроны передаются на пластоцианин (Пц) — водорастворимый белок, содержащий два атома меди, который восстанавливает окисленную форму хлорофилла П700 . Комплекс цитохромов b6 /f функционирует в тилакоидной мембране в виде димера. Реакционными центрами фотосистем называют хлорофилл-белковые комплексы, способные к первичному фотохимическому разделению зарядов. При этом хлорофилл П680 служит первичным донором электрона в реакционном центре фотосистемы II, а хлорофилл П700 — в реакционном центре фотосистемы I. Обычно время жизни возбужденных электронов ароматических соединений составляет около 5 *10-9 с. За такое время энергия возбужденного состояния молекулы либо переходит в тепло, либо испускается в виде кванта флуоресценции. Для того чтобы эта энергия могла использоваться для разделения зарядов и преобразования физической формы энергии в химическую, скорость передачи энергии возбуждения должна быть больше, чем испускание квантов флуоресценции. Поэтому время передачи энергии в реакционных центрах фотосистем должно составлять несколько пикосекунд. Главная особенность первичных процессов фотосинтеза как раз и заключается в том, что отрыв электрона от хлорофилла (первичное разделение зарядов) и восстановление первичного акцептора (феофетина) происходит очень быстро — за 3 пикосекунды. Именно поэтому эффективность передачи энергии возбужденного электрона в реакционных центрах фотосистем близка к 100%. Образующаяся при этом окисленная форма хлорофилла П680 приобретает способность "отнимать" электроны у белков кислород-выделяющего комплекса, а те, в свою очередь, — у воды. Разделение зарядов в реакционном центре фотосистемы II условно можно разделить на три этапа. На первом этапе под действием света происходит возбуждение молекулы хлорофилла. На втором этапе электрон передается первичному акцептору феофитину. При этом хлорофилл переходит в окисленную форму (П680), а феофитин восстанавливается. Появление неспаренного электрона в молекуле хлорофилла инициирует переход на нее электрона от кислород-выделяющего центра. Посредником между Mn-кластером кислород-выделяющего центра и П680 служит редокс-активный остаток тирозина белка D1. На заключительном этапе электрон от восстановленной формы феофетина поступает на первичный хинон QA, а затем на вторичный хинон QB. После этого электроны уже выходят за пределы реакционного центра фотосистемы II и идут на восстановление липидорастворимого пула пластохинонов. Процесс первичного разделения зарядов в фотосистеме I происходит аналогичным путем. От возбужденного под действием света П700 электроны вначале переносятся на первичный акцептор хлорофилл A0, затем на вторичный акцептор филлохинон (A1) и на белок FX. Дефицит электронов у окисленного П700 восполняется за счет их поступления из фотосистемы II через медь-содержащий белок — пластоцианин. Затем электроны от белков, содержащих железосерные кластеры FA/FB фотосистемы I, переносятся на ферредоксин . Перенос электрона по фотосинтетической цепи приводит к восстановлению переносчиков и к появлению конечных продуктов — АТФ и НАДФН, которые вступают в ферментативные реакции. Под вторичным разделением зарядов понимают процесс генерации на мембране тилакоида градиента протонов. Следует подчеркнуть, что электрохимический градиент ионов водорода, формируемый в процессе разделения зарядов на тилакоидной мембране, представляет собой уже электрическую форму энергии, которая c помощью АТФ-синтазы может быть трансформирована в химическую энергию макроэргической связи АТФ. Одним из важнейших эволюционных "приобретений" живой природы является способность фотосинтезирующих организмов окислять воду с выделением молекулярного кислорода за счет энергии солнечного света. Именно оксигенный фотосинтез привел к появлению в атмосфере значительных количеств молекулярного кислорода, что привело к переходу биоэнергетики с анаэробного на качественно новый и более эффективный аэробный тип метаболизма. В результате разделения зарядов в реакционном центре фотосистемы II образуется самый сильный биологический окислитель — хлорофилл П680 , окислительно-восстановительный потенциал которого достаточен для окисления воды. Для объяснения механизма фотоокисления (фотолиза) воды наиболее часто используют "гипотезу Кока". В основе этой гипотезы лежит представление об"S-системе", которая осуществляет одновременное 4-электронное окисление двух молекул воды без образования каких-либо промежуточных продуктов: 2H2O— 4e—> 4H++ O2 В кислород-выделяющий центр входят Mn-содержащий кластер белка D1 и, как кофакторы — кальций и хлор. Согласно модели Кока "S-система" окисления воды, в зависимости от уровня окисления ионов марганца, может находиться в пяти функционально различных состояниях — S0 , S1, S2 , S3 и S4. В ходе "S-цикла" происходит последовательное изменение валентности составляющих кластер атомов марганца. Переход из одного состояния в последующее происходит при попадании одного кванта света и удалении одного из электронов из системы через остаток аминокислоты тирозина белка D1. Выделение молекулярного кислорода из двух молекул воды происходит лишь при переходе из состояния S3 в состояние S4 , причем, поскольку состояние S4нестабильно, оно сразу же переходит в S0 . При окислении двух молекул воды в 4-тактном процессе окисления также совершается последовательное выделение 4-х протонов в люмен тилакоида.
Z-схема фотосинтеза и транспорт электронов в фотосистемах I и II Z-схема фотосинтеза. Последовательность расположения отдельных элементов ЭТЦ в тилакоидных мембранах хорошо иллюстрирует Z-схема фотосинтеза. Вертикальными длинными стрелками показан процесс поглощения света в реакционном центре и переход молекул хлорофиллов П680 и П700 в возбужденное состояние. Сплошными стрелками отмечен нециклический перенос электронов по цепи. Стрелками с точками и пунктиром показан циклический путь электронов в фотосистеме I и реакция Мелера.(Об этом читайте ниже). При нециклическом транспорте электрона в фотосистемах I и II синтез АТФ сопряжен с образованием НАДФН и выделением O2 . В случае циклического переноса электрона по замкнутому участку цепи в фотосистеме I в качестве единственного продукта образуется АТФ. Следует отметить также, что отдельные элементы электронтранспортной цепи расположены в соответствии с величиной их окислительно-восстановительного (редокс) потенциала. При фотосинтезе окислительно-восстановительные потенциалы реакций переноса электронов обычно лежат в диапазоне от +0,82 В ( H2O/O2 ) до -0,42 В (ферредоксин). Транспорт электронов в фотосистеме II.При поглощении энергии фотосистемой II хлорофилл П680 переходит в возбужденное состояние и передает электроны феофитину. Окисленная форма хлорофилла ( П680 ) восстанавливается электронами, поступающими от тирозинового остатка ( YZ ) белка D1 реакционного центра фотосистемы II. Восстановление окисленной формы YZ осуществляется электронами, выделяющимися при фотоокислении воды. От феофитина электроны идут на пластохиноны. Вначале происходит восстановление молекулы "первичного" хинона QA , а затем — терминального акцептора электронов "вторичного" хинона QB . Далее через пул липидорастворимых пластохинонов(Q) и комплекс цитохромов b6 /f электроны передаются на водорастворимый белок пластоцианин, который восстанавливает окисленную форму хлорофилла П700 . Транспорт электронов в фотосистеме I.При поглощении энергии света фотосистемой I хлорофилл П700 переходит в возбужденное состояние и передает электрон первичному акцептору — хлорофиллу а, а затем филлохинону ( A1 ). Далее следует серия мембранно-связанных железосерных белков ( FX , FA , FB ), через которые электроны поступают на ферредоксин. От ферредоксина через флавопротеин — ферредоксин-НАДФ-редуктазу электроны идут на восстановление НАДФ до НАДФН. Механизм транспорта электронов и протонов в комплексе цитохромов b6/f В процессе транспорта электронов в комплексе цитохромов b6 /f происходит формирование пластосемихинона (Q) и последующее его восстановление до пластохинола. Липидорастворимые пластохиноны работают как "двухэлектронные ворота", поскольку в ходе окисления пластохинола один из двух электронов по линейной цепи направляется в фотосистему I, а второй электрон поступает в цикл цитохромов b6 /f Таким путем достигается увеличение количества протонов, перекачиваемых через мембрану внутрь тилакоида. В цитохроме b6 имеются два отдельных сайта для связывания восстановленной и окисленной форм пластохинона. На первом этапе после окисления пластохинола один из электронов передается на белок Риске ( FeSR ) и далее на цитохром f, пластоцианин (Пц) и хлорофилл П700. Второй электрон идет на низкопотенциальный (L) гем цитохрома b6 . От восстановленного гема L электроны поступают на высокопотенциальный гемм (H) цитохрома b6 и далее на пластохинон, который восстанавливается в пластосемихинон. В итоге два протона выкачиваются внутрь тилакоида. На втором этапе происходит окисление еще одной молекулы пластохинола. Один из электронов идет по линейной цепи от белка Риске через цитохром f, на пластоцианин и фотосистему I. Второй же электрон через низкопотенциальный (L) и высокопотенциальный (H) гемы цитохрома b6 поступает на пластосемихинон и восстанавливает его до пластохинола . при этом происходит связывание двух протонов из стромы. В результате еще два протона попадают в полость тилакоида. Таким образом, в процессе транспорта электронов через комплекс цитотохромов b6 /f на каждые 2 электрона, поставляемые в фотосистему I, через тилакоидную мембрану переносится 4 протона. Формируемый градиент ионов H далее используется на синтез АТФ.
|
Источник: mykonspekts.ru