Включения цитоплазмы и их значение
Как по составу, так и по своей физической роли все микроскопически видимые и гистохимически определяемые непостоянные включения можно разделить на несколько хорошо характеризующиеся группы.
Наиболее простая классификация их такова:
I. Трофические включения (от греч. trophe — пища)
1. Включения неопределенного химического состава;
2. Включения, хорошо характеризующиеся химически, представляющие по большей части запасные вещества в клетке:
а) белковые вещества,
б) жировые вещества,
в) гликоген (углеводные вещества).
II. Пигментные включения.
III. Витамины.
IY. Продукты, обособившиеся в цитоплазме и подлежащие выведению из клеток: 1. экскреторные включения. 2. секреторные продукты.
I. Трофические включения.
1. Включения неопределенного химического состава.
Это в большинстве случаев очень мелкие образования, стоящие на границе видимости современным световым микроскопов. Во время жизненного цикла клетки они то появляются в цитоплазме, то исчезают. Данные включения состоят из разных солевых растворов, или включения разной степени плотности с белковым, углеводным, жировым, липоидным или смешанным содержимым. При определенных условиях такие включения могут скапливаться в клетках в значительных количествах, что указывает в большинстве случаев на изменения в самом обмене веществ.
2. Включения, хорошо характеризующиеся химически.
Белковые вещества.
В нормальном состоянии у животных и человека в цитоплазме клеток белковых веществ как-запасного материала обычно не откладывается. Но в цитоплазме яйцеклеток, а так же в клетках после дробления всегда присутствуют белковые включения. Они имеют чаще всею форму округлых, иногда очень мелких, иногда довольно крупных гранул.
Жировые вещества.
Капли видимого микроскопического жира в небольшом количестве можно обнаружить решительно во всех клетках организма. По. как правило, в цитоплазме клеток, специально не приспособленных к накоплению жировых веществ, при нормальном клеточном обмене запасного жира откладывается очень мало. При понижении окислительных процессов или при усилении функции жирообразования в цитоплазме клеток может появиться значительное количество жира. Это явление называется простым ожирением клетки. Жировые включения обычно имеют форму округлых капель различной величины. Это указывает на то, что жировые вещества находятся в жидком состоянии.
Углеводные вещества (гликогены).
Постоянной составной частью цитоплазмы являются углеводы (сахара). Однако можно обнаружить в клетках животных и человека лишь только полисахарид гликоген. Образуясь из глюкозы, как уже упоминалось ранее, он откладывается как запасной энергетический материал. Расщепляясь на глюкозу, гликоген тем самым снабжает организм глюкозой по мере потребления ее тканями являющуюся основным энергетическим источником нашего организма. Следует отметить, чго в норме гликоген может откладываться только в цитоплазме клеток.
II. Пигментные включения.
Пигментами называются окрашенные вещества, образующиеся в клетках растений и животных. Своим присутствием в клетках пигменты обусловливают окраску организмов. Все пигменты можно разделить на две большие группы:
пигменты крови и продукты их превращений,
пигменты не принимающие участия в процессах дыхания.
| 1 Термин «экскрет», как и термин «секрет» происходит от латинского слова сегпо — отделять. Экскрет обычно переводится как то, что подлежит удалению, секрет (se самый, таковой) как отделяемое. |
Пигменты крови.
К этой группе относятся прежде всего гемоглобин, являющийся основным составным веществом эритроцита (красной клетки крови), и продукты его распада.
Гемоглобин — сложное соединение, образованное белком глобином с окрашенным сложным соединением белкового характера, содержащим в своем составе железо. Поскольку в нем содержится железо, гемоглобин присоединяет к себе кислород, являясь главным переносчиком кислорода по организму ко всем тканям. К продуктам распада гемоглобина относятся гематоидин, гематосидерин, малярийный пигмент, образующиеся в результате распада гемоглобина в клетках крови при проникновении в них малярийного плазмодия.
Пигменты, не принимающие участия в процессах дыхания.
В эту группу объединяются вещества довольно разнородного физиологического значения. В цитоплазме клеток они в большинстве случаев обособляются в виде гранул. Различают следующие пигменты:
каротиноиды;
хромолипоиды;
меланины.
Каротиноиды.
По химическому составу каротиноиды представляют ненасыщенные углеводы, не содержащие в своем составе азота. Желтая или красная окраска каротиноидов позволяет легко заметить их под микроскопом. Каротиноиды не вырабатываются в самой цитоплазме клеток, а поступают в организм человека из растительной пищи. Откладываясь в цитоплазме клеток, каротиноиды редко обособляются в ней в виде чистых веществ, обычно вследствие своей хорошей растворимости в жирах, они всегда входят в состав жировых капель, образуя таким образом смеси.
Хромолипоиды.
Хромолипоиды в цитоплазме клеток встречаются в виде капель желтого или коричневого цвета, принадлежащих к жировым веществам и образуясь в клетках в результате окисления жиров цитоплазмы. В цитоплазме образуют смеси с жирами.
Меланины.
Важная группа пигментов, дающих большую гамму цветов, от желтого до черного. Меланины обусловливают цвет кожи человека и животных. Поэтому их можно назвать пигментами окраски. Меланины образуются в цитоплазме клеток из продуктов распада протеинов. При различных заболеваниях количество меланинов может значительно увеличиваться.
III. Витамины
В цитоплазме клеток удается обнаружить на сегодняшний день лишь два витамина: витамин А и витамин С.
IV. Продукты, подлежащие выведению из клетки
Экскреторные включения.
Вещества, образовавшиеся при распаде основных составных частей цитоплазмы и в дальнейшем выводящиеся из клетки, а в последствии и из организма во внешнюю среду. Экскреты могут быть самого разнообразного химического состава, например мочевина, мочекислые соли, продукты распада кровяных пигментов, желчные пигменты и т.д.
Секреторные включения.
Они состоят из веществ, выделяемых клеткой во внешнюю среду организма. Сюда относят: жир, выделяемый сальными железами и служащий для смазки кожи, слизь, выделяемая слюнными и другими железами, пищеварительные ферменты и т.д.
Ядро клетки.
Ядро было впервые открыто у растений в 1831 г. ботаником Р. Брауном. Он описал его как пузыревидное тельце, расположенное в центре клетки (рис 1, 2). В настоящее время можно считать доказанным, что клетки всех растительных и животных организмов, за исключением некоторых, имеют ядро. Если отрезать участок цитоплазмы от тела клетки, то он, в конце концов, распадется. Одна цитоплазма без ядра к длительному существованию неспособна. Вместе с тем участок с ядром вновь может восстановить утраченную часть цитоплазмы. При нарушении структуры ядра, путем его прокалывания, клетки погибают.
Форма ядра менее разнообразна, чем форма клетки. Большинство ядер имеют простую шаровидную или эллипсоидальную форму.
Размер ядра колеблется от 3 до 25 мкм. Большинство клеток человека — одноядерные. Однако имеются двуядерные (гепатоциты, кардиомиоциты), многоядерные (мышечные волокна — миосимпласты). Ядро включает ядерную оболочку, нуклеоплазму, хроматин, ядрышко.
Ядерная оболочка состоит из внутренней и наружной ядерных мембран толщиной 8 нм каждая. Ядерная оболочка пронизана множеством ядерных пор округлой формы диаметром 50-70 нм. Через ядерные поры происходит обмен веществ между ядром и цитоплазмой.
Нуклеоплазма — неокрашивающаяся часть ядра, представляет собой коллоидный раствор белков, окружающий хроматин и ядрышко.
Хроматин (от греческого chroma — краска). хорошо окрашивается при фиксации в красителе. Хроматин — хромосомный материал. В его состав входят ДНК, белки, небольшое количество РНК.
Ядрышко (одно или несколько выявляется во всех клетках в виде интенсивно окрашивающегося округлого тельца. В состав ядрышка входят рибонуклеопротеиды (РНИ) и большое количество нитей РНК.
Основная функция ядра — участие в процессе размножения, деление клетки.
Особенности строения и функции жировых клеток.
Жировые клетки, как и все другие клетки нашего организма, имеют вполне определенную клеточную форму, состоящую из ядра и цитоплазмы и имеющие цитоплазматическую мембрану, отделяющую данные клетки от других клеточных структур.
В функциональном отношении жировые клетки являются элементами, служащими для накопления резервного жира и имеют весьма значительные размеры (до 120 мкм) и вид шарообразных пузырьков, наполненных жиром. Жировая капля занимает всю центральную часть клетки и окружена тонким цитоплазматическим ободком, образующим вокруг этой капли как бы оболочку. Рядом с жировым накоплением в клетке располагается ядро (рис. 5, 6). В некоторых случаях жировые клетки расположены по отдельности или небольшими группами, в других случаях они образуют скопления в соединительной ткани большими массами, имеющими дольчатое строение. В таких случаях говорят о жировой ткани. Жировые вещества, входящие в состав жировых клеток в основном состоят из нейтральных жиров. Изучение физического состояния привело к заключению, что капли жира представляют собой эмульсию, образованную в результате растворения сильно обводненной фазы в смеси жировых веществ. Подобные эмульсии характеризуются тем, что они находятся на границе между твердым и жидким состоянием, образуя пастозные массы .
Как количество жира, так и число самих жировых клеток подвержено значительным
2 Примером пастозного состояния могут служить самые разнообразные мази или помады

колебаниям. При голодании содержание жира в них уменьшается. При усиленном питании — увеличивается. Жировые клетки в стадии их полного развития, по-видимому, не способны к делению. Несмотря на все поиски никому до сих пор не удалось найти митотического состояния их ядра, т.е. деления клетки. Образование же жировых клеток происходит из недифференцированных элементов, в частности из ретикулярных клеток соединительной ткани, а так же камбиальных клеток и гистиоцитов, в большом количестве сопровождающих кровеносные сосуды, около которых обычно и располагается главная масса жировых клеток. В организме жировая ткань играет не только резервную, но и механическую роль, образуя мягкие подстилки в некоторых органах, например в коже.
Глава III. «Ткань — совокупность клеток одной структуры.»
Кожа и её производные.
Кожа является очень важным и весьма многосторонним в функциональном отношении органом. Кожа выполняет ряд жизненно важных функций, о которых нельзя не сказать.
1. Кожа образует плотный и прочный покров, который защищает подлежащие части от механических повреждений и от потери воды, а так же препятствует проникновению во внутреннюю среду различных болезнетворных начал. Кожа в нормальном состоянии непроницаема не только для микроорганизмов, но для растворенных ядовитых и вредных веществ .
2. Кожа защищает подлежащие ткани от сильных световых раздражений (ультрафиолетовых лучей).
3. Кожа является органом, регулирующим теплоотдачу. В этой функции основную роль играет выделение пота, усиливающее в свою очередь отдачу тепла, и волосяной покров, защищающий от избыточного охлаждения.
4. Кожа принимает участие в обмене веществ, удаляя с потом некоторые продукты распада.
5. Кожа участвует в газообмене, осуществляя кожное дыхание.
6. Наконец, кожа является весьма важным органом чувств, в котором сосредоточены
Все сказанное относится к самому эпидермису. Выводные протоки потовых желез этим свойством не обладают, чем и пользуются врачи, назначая втирания различных наружных лекарственных средств (мазей и т.п.).
осязательные, температурные и болевые нервные окончания.
Строение кожи.
Эпителиальная наружная часть кожи носит название эпидермиса, а соединительнотканная — собственно кожи (derma) (рис. 7). С подлежащими частями кожа соединяется при помощи более рыхлой соединительной тканной прослойки, носящей название подкожного жирового слоя или подкожной клетчатки. Главную роль в защитной функции кожи играет эпителиальный слой, или эпидермис, прочность же кожи обуславливается соединительной тканью собственно кожи (дермы).
Эпидермис.
Кожный эпидермис человека представлен многослойным эпителием. На поверхности эпидермиса обнаруживается рисунок.
Источник: poznayka.org
Трофические включения
– запас питательных веществ клетки. Различают углеводные, жировые и белковые включения. Например, глыбки гликогена и капли жира в клетках печени – запас углеводов и липидов, который образуется в организме после еды и исчезает при голодании. Желточные включения (липопротеидные гранулы) в яйцеклетке – запас питательных веществ, необходимый для развития зародыша в первые дни его возникновения.
Секреторные включения
– гранулы и капли веществ, синтезированных в клетке для нужд организма (например, пищеварительные ферменты для желудочного и кишечного сока), которые накапливаются в вакуолях комплекса Гольджи апикальной части клетки и выводятся из клетки путём экзоцитоза.
Экскреторные включения
– гранулы и капли веществ, вредных для организма, которые выводятся клетками во внешнюю среду с мочой и калом. Например, экскреторные включения в клетках канальцев почек.
Пигментные включения
– гранулы или капли веществ, придающих клетке цвет. Например, глыбки белка меланина, имеющего коричневый цвет в меланоцитах кожи, или гемоглобин в эритроцитах.
Помимо структур цитоплазмы, которые можно четко отнести к органеллам или включениям, в ней постоянно имеется огромное количество разнообразных транспортных пузырьков, обеспечивающих перенос веществ между различными компонентами клетки.
Гиалоплазма – истинный раствор биополимеров заполняющий клетку, в котором во взвешенном состоянии (как в суспензии) находятся органеллы и включения, а также ядро клетки. К биополимерам гиалоплазмы относятся белки, жиры, углеводы, нуклеиновые кислоты, а также их сложные комплексы, которые растворены в воде, богатой минеральными солями и простыми органическими соединениями. Кроме того, в гиалоплазме находится цитоматрикс – сеть белковых волокон толщиной 2-3 нм. Через гиалоплазму различные структурные компоненты клетки взаимодействуют между собой, происходит обмен веществ и энергии. Гиалоплазма может переходить из жидкого (золь) в желеобразное (гель) состояние. При этом снижается скорость движения в гиалоплазме потоков веществ и энергии, движение органоидов, включений и ядра, а значит угнетается и функциональная активность клетки.
Реакция клеток на внешнее воздействие.
Описанная морфология клеток не является стабильной (постоянной). При воздействии на организм различных неблагоприятных факторов в строении различных структур проявляются различные изменения. В зависимости от факторов воздействия изменения клеточных структур проявляются неодинаково в клетках разных органов и тканей. При этом изменения клеточных структур могут быть адаптивными (приспособительными) и обратимыми, или жедезадаптивными, необратимыми (патологическими). Однако определить четкую грань между адаптивными и дезадаптивными изменениями не всегда возможно, так как приспособительные изменения могут перейти в патологические. Поскольку объектом изучения гистологии являются клетки, ткани и органы здорового организма человека, то здесь будут рассмотрены прежде всего адаптивные изменения клеточных структур. Изменения отмечаются как в строении ядра, так и цитоплазмы.
Изменения в ядре— набухание ядра и сдвиг его на периферию клетки, расширение перинуклеарного пространства, образование инвагинаций кариолеммы (впячивание внутрь ядра его оболочки), конденсация хроматина. Кпатологическим изменениям ядра относят:
-
пикноз — сморщивание ядра и коагуляция (уплотнение) хроматина;
-
кариорексис — распад ядра на фрагменты;
-
кариолизис — растворение ядра.
Изменения в цитоплазме— уплотнение, а затем набухание митохондрий, дегрануляция зернистой эндоплазматической сети (слущивание рибосом), а затем и фрагментация канальцев на отдельные вакуоли, расширение цистерн, а затем распад на вакуоли пластинчатого комплекса Гольджи, набухание лизосом и активация их гидролаз, увеличение числа аутофагосом, в процессе митоза — распад веретена деления и развитие патологических митозов.
Изменения цитоплазмымогут быть обусловлены структурными изменениями плазмолеммы, что приводит к усилению ее проницаемости и гидратации гиалоплазмы, нарушением обмена веществ, что сопровождается снижением содержания АТФ, снижением расщепления или увеличением синтеза включений (гликогена, липидов) и их избыточном накоплении.
После устранения неблагоприятных воздействий на организм реактивные(адаптивные) изменения структур исчезают и морфология клетки восстанавливается. При развитиипатологических(дезадаптивных) изменений даже после устранения неблагоприятных воздействий структурные изменения нарастают и клетка погибает.
Регенерация.
Регенера́ция (восстановление) — способность живых организмов со временем восстанавливать повреждённые ткани, а иногда и целые потерянные органы.
Виды смерти клеток.
Различают два вида клеточной гибели: насильственная смерть от повреждения – некроз и запрограммированная клеточная смерть – апоптоз.
Некроз
– это посмертные изменения клетки необратимого характера, заключающиеся в постепенном ферментативном разрушении и денатурации ее белков. Он развивается при чрезмерной альтерации клетки, не требует затрат энергии и не зависит от управляющих сигналов местного и центрального происхождения («анархических путь гибели»). Вследствие синтеза поврежденной клеткой БАВ (простогландины) и нарушения целостности ее мембран (выход различных ферментов), некроз представляет определенную угрозу окружающим структурам – это часто способствует развитию воспалительного процесса.
Насильственная гибель клетки обусловлена:
-
лишением ее питания и кислорода;
-
необратимыми изменениями структуры и функции с угнетением важнейших метаболических процессов различными патогенными агентами.
Некрозу предшествует глубокая, частично необратимая стадия повреждения клетки – некробиоз (рис. 1). Несмотря на многообразие этиологических факторов, провоцирующих в конечном счете развитие некробиоза и некроза, молекулярно-клеточные изменения, выявляемые при гибели клетки в большинстве случаев одинаковы (Зайчик А.Ш., Чурилов Л.П., 1999). Согласно их мнению, важно различать гипоксический и свободно-радикальный некробиоз. Механизмы свободно-радикального повреждения клетки (см. выше) могут запускаться без первичной гипоксии, а иногда даже в условиях его избытка. Гипоксический некробиоз (см. раздел «Гипоксия») инициируется различными патогенными факторами, вызывающих продолжительную гипоксию. Оба вида некробиоза могут комбинироваться и взаимно дополнять друг друга. Исходом обоих видов некробиоза являются такие повреждения клетки, при которых она уже неспособна к самостоятельному энергообеспечению (т. необратимости, рис. 1) и подвергается некрозу.
Некоторые исследователи иногда рассматривают некробиоз, как процесс собственной гибели клетки. По Давыдовскому И.В., некробиоз – это процесс отмирания клеток. Некроз же, в большей степени характеристика морфологическая, наблюдающаяся после гибели клетки, а не механизм самой гибели.
Различают две основные разновидности некроза:
-
коагуляционный (сухой) некроз. При нем в клетке развивается значительный ацидоз, идет коагуляция белков и отмечается повышенное накопление кальция с агрегацией элементов цитоскелета. Очень часто наблюдается при тяжелой гипоксии, например, в кардиомиоцитах при инфаркте миокарда. Данный некроз преимущественно развивается в тканях богатых белком и кальцием и характеризуется ранними и глубокими поражениями митохондрий;
-
колликвационный некроз. Для него типично преобладание гидролитических процессов лизосомального аутолиза или гетеролизиса при участии фагоцитов. Очаг некроза размягчен, наблюдается накопление активных гидроксильных радикалов и эндогенное омыление клеток, что приводит к разрушению ее структур, например различных мембран.
Между коагуляционным и колликвационным некрозоми четких границ нет. Возможно, это объясняется тем, что механизмы их развития во многом общие. Ряд исследователей выделяют и так называемый казеозный (творожистый) некроз (при туберкулезе), пологая при этом, что он представляет собой комбинацию двух предыдущих типов.
Апоптоз.
Апоптоз – это программированная клеточная смерть (инициирующаяся под действием вне- или внутриклеточных факторов) в развитии которой активную роль принимают специальные и генетически запрограммированные внутриклеточные механизмы. Он, в отличие от некроза активный процесс, требующий определенных энергозатрат. Первоначально пытались разграничить понятия «программированная клеточная гибель» и «апоптоз»: к первому термину относили устранение клеток в эмбриогенезе, а ко второму – программированную смерть только зрелых дифференцированных клеток. В настоящее время выяснилось, что никакой целесообразности в этом нет (механизмы развития клеточной гибели одинаковы) и два понятия превратились в синонимы, хотя это объединение и не бесспорно.
Прежде чем приступить к изложению материала о роли апоптоза для жизнедеятельности клетки (и организма) в норме и патологии, мы рассмотрим механизм апоптоза. Их реализацию можно представить в виде поэтапного развития следующих стадий:
1 стадия – стадия инициации (индукции).
В зависимости от происхождения сигнала, стимулирующего апоптоз, различают:
-
внутриклеточные стимулы апоптоза. Среди них к наиболее известным относят – разные виды облучения, избыток Н+, оксид азота, свободные радикалы кислорода и липидов, гипертермия и др. Все они могут вызывать различные повреждения хромосом (разрывы ДНК, нарушения ее конформации др.) и внутриклеточных мембран (особенно митохондрий). То есть в данном случае поводом для апоптоза служит «неудовлетворительное состояние самой клетки» (Мушкамбиров Н.П., Кузнецов С.Л., 2003). Причем, повреждение структур клеток должно быть достаточно сильным, но не разрушительным. У клетки должны сохраниться энергетические и материальные ресурсы для активации генов апоптоза и его эффекторных механизмов. Внутриклеточный путь стимуляции программированной смерти клетки можно обозначить как «апоптоз изнутри»;
-
трансмембранные стимулы апоптоза, т.е., в этом случае он активируется внешней «сигнализацией», которая передается через мембранные или (реже) внутриклеточные рецепторы. Клетка может быть вполне жизнеспособной, но, с позиции целостного организма или «ошибочной» стимуляции апоптоза, она должна погибнуть. Этот вариант апоптоза получил название «апоптоз по команде».
Трансмембранные стимулы подразделяются на:
-
«отрицательные» сигналы. Для нормальной жизнедеятельности клетки, регуляции ее деления и размножения необходимо воздействие на нее через рецепторы различных БАВ: факторов роста, цитокинов, гормонов. Среди прочих эффектов, они подавляют механизмы клеточной гибели. И естественно, дефицит или отсутствие данных БАВ активирует механизмы программированной смерти клетки;
-
«положительные» сигналы. Сигнальные молекулы, такие как ФНОα, глюкокортикоиды, некоторые антигены, адгезивные белки и др., после взаимодействия с клеточными рецепторами могут запускать программу апоптоза.
На клеточных мембранах находится группа рецепторов, в задачу которых передача сигнала к развитию апоптоза является основной, возможно даже единственной функцией. Это, например, белки группы DR (death receptos – «рецепторы смерти»): DR3, DR4, DR5. Наиболее хорошо изучен Fas-рецептор, появляющийся на поверхности клеток (гепатоцитах) спонтанно или под влиянием активации (зрелые лимфоциты). Fas-рецептор при взаимодействии с Fas-рецептором (лигандом) Т-киллера запускает программу смерти клетки мишени. Однако, взаимодействие Fas-рецептора с Fas-лигандом в областях, изолированных от иммунной системы, заканчивается гибелью самого Т-киллера (см. нижеигандом в областях, изолированных от иммунной системы, заканчивается гибелью самого Т-киллера ()ожно000000000000000000000000000).
Следует помнить, что некоторые сигнальные молекулы апоптоза, в зависимости от ситуации могут наоборот, блокировать развитие программированной смерти клеток. Амбивалентность (двойственное проявление противоположных качеств) характерна для ФНО, ИЛ-2, интерферона γ и др.
На мембранах эритроцитов, тромбоцитов, лейкоцитов, а так же клеток легкого и кожи обнаружены особые антигены-маркеры. На них синтезируются физиологические аутоантитела, и они, выполняя роль опсонинов, способствуют фагоцитозу этих клеток, т.е. гибель клеток происходит путемаутофагоцитоза. Выяснилось, что антигены-маркеры появляются на поверхности «старых» (прошедших свой путь онтогенетического развития) и поврежденных клетках, молодые и неповрежденные клетки их не имеют. Данные антигены получили название «антигены-маркеры стареющих и поврежденных клеток» или «белок третьей полосы». Появление белка третьей полосы контролируется геномом клетки. Следовательно, аутофагоцитоз можно рассматривать, как вариант запрограммированной гибели клеток.
-
Смешанные сигналы. Это сочетанное воздействие сигналов первой и второй группы. Например, апоптоз происходит с лимфоцитами, активированных митогоном (положительный сигнал), но не вступивших в контакт с АГ (отрицательный сигнал).
2 стадия – стадия программирования (контроля и интеграции механизмов апоптоза).
Для этой стадии характерно два, диаметрально противоположных процесса, наблюдающихся после инициации. Происходит либо:
-
реализация пускового сигнала к апоптозу через активацию его программы (эффекторами являются каспазы и эндонуклеазы);
-
блокируется эффект пускового сигнала апоптоза.
Различают два основных, но не исключающих друг друга, варианта исполнения стадии программирования (рис. 14):

Рис. 14. Каспазный каскад и его мишени
R– мембранный рецептор; К – каспазы;AIF– митохондриальная протеаза; Цит. С – цитохром с;Apaf-1 – цитоплазматический белок;IAPs– ингибиторы каспаз
1. Прямая передача сигнала (прямой путь активации эффекторных механизмов апоптоза минуя геном клетки) реализуется через:
-
адапторные белки. Например, так осуществляется запуск апоптоза Т-киллером. Он активирует каспазу-8 (адапторный белок). Аналогично может действовать и ФНО;
-
цитохром С и протеазу ΑIF (митохондриальная протеаза). Они выходят из поврежденной митохондрии и активируют каспазу-9;
-
гранзимы. Т-киллеры синтезируют белок перфорин, который образует каналы в плазмолемме клетки-мишени. Через эти каналы в клетку проникают протеолитические ферменты гранзимы, выделяемые все тем же Т-киллером и они запускают каскад каспазной сети.
2. Опосредованная передача сигнала. Она реализуется с помощью генома клетки путем:
-
репрессии генов, контролирующих синтез белков-ингибиторов апоптоза (гены Bcl-2, Bcl-XL и др). Белки Bcl-2 в нормальных клетках входят в состав мембраны митохондрий и закрывают каналы по которым из этих органоидов выходят цитохром С и протеаза AIF;
-
экспрессии, активации генов, контролирующих синтез белков-активаторов апоптоза (гены Bax, Bad, Bak, Rb, P53 и др.). Они, в свою очередь активируют каспазы (к-8, к-9).
На рис. 14 представлена примерная схема каспазного принципа активации каспаз. Видно, что откуда бы не запускался каскад, его узловым моментом является каспаза 3. Она активируется и каспазой 8 и 9. Всего в семействе каспаз – более 10 ферментов. Локализуются в цитоплазме клетки в неактивном состоянии (прокаспазы). Положение всех каспаз в данном каскаде до конца не выяснено, поэтому на схеме ряд из них отсутствует. Как только активируются каспазы 3,7,6 (возможно и их другие типы) наступает 3 стадия апоптоза.
3 стадия – стадия реализация программы (исполнительная, эффекторная).
Непосредственными исполнителями («палачами» клетки) являются выше указанные каспазы и эндонуклеазы. Местом приложения их действия (протеолиза) служат (рис. 14):
-
цитоплазматические белки – белки цитоскелета (фодрин и актин). Гидролизом фодрина объясняют изменение поверхности клетки – «гофрирование» плазмолеммы (появление на ней впячиваний и выступов);
-
белки некоторых цитоплазматических регуляторных ферментов: фосфолипазы А2, протеинкиназы С и др.;
-
ядерные белки. Протеолиз ядерных белков занимает основное место в развитии апоптоза. Разрушаются структурные белки, белки ферментов репликации и репарации (ДНК-протеинкиназы и др.), регуляторные белки (рRb и др.), белки-ингибиторов эндонуклеаз.
Иннактивация последней группы – белков ингибиторов эндонуклеаз приводит к активации эндонуклеаз, второму «орудию» апоптоза. В настоящее время эндонуклеазы и в частности, Са2+, Мg2+ -зависимая эндонуклеаза, рассматривается как центральный фермент программируемой смерти клетки. Она расщепляет ДНК не в случайных местах, а только в линкерных участках (соединительные участки между нуклеосомами). Поэтому хроматин не лизируется, а только фрагментируется, что определяет отличительную, структурную черту апоптоза.
Вследствие разрушения белка и хроматина в клетке формируются и от нее отпочковываются различные фрагменты – апоптозные тельца. В них находятся остатки цитоплазмы, органелл, хроматина и др.
4 стадия – стадия удаления апоптозных телец (фрагментов клетки).
На поверхности апоптозных телец экспрессируются лиганды, они распознаются рецепторами фагоцитов. Процесс обнаружения, поглощения и метаболизирования фрагментов погибшей клетки происходит сравнительно быстро. Это способствует избежать попадания содержания погибшей клетки в окружающую среду и тем самым, как отмечено выше, воспалительный процесс не развивается. Клетка уходит из жизни «спокойно», не беспокоя «соседей» («тихий суицид»).
Программированная клеточная гибель имеет важное значение для многих физиологических процессов. С апоптозом связаны:
-
поддержание нормальных процессов морфогенеза – запрограммированная смерть клеток в процессе эмбриогенеза (имплантации, органогенеза) и метаморфоза;
-
поддержание клеточного гомеостаза (в том числе ликвидация клеток с генетическими нарушениями и инфицированных вирусами). Апоптозом объясняется физиологическая инволюция и уравновешивание митозов в зрелых тканях и органах. Например, гибель клеток в активно пролиферирующих и самообновляющихся популяциях – эпителиоцитов кишечника, зрелых лейкоцитов, эритроцитов. Гормонально-зависимая инволюция – гибель эндометрия в конце менструального цикла;
-
селекция разновидностей клеток внутри популяции. Например, формирование антигенспецифической составляющей иммунной системы и управление реализацией ее эффекторных механизмов. С помощью апоптоза происходит выбраковка ненужных и опасных для организма клонов лимфоцитов (аутоагрессивных). Сравнительно недавно (Griffith T.S., 1997) показали значение программированной гибели клеток в защите «иммунологически привилегированных» зон (внутренние среды глаза и семенников). При прохождении гисто-гематических барьеров данных зон (что случается редко), эффекторные Т-лимфоциты гибнут (см. выше). Включение механизмов их смерти обеспечивается при взаимодействии Fas-лиганда барьерных клеток с Fas-рецепторами Т-лимфоцита, тем самым предотвращается развитие аутоагрессии.
Роль апоптоза в патологии и виды различных заболеваний связанных с нарушением апоптоза представлены в виде схемы (рис. 15) и таблицы 1.
Конечно, значение апоптоза в патологии меньше чем некроза (возможно, это связано с недостаточностью таких знаний). Однако, проблема его в патологии имеет и несколько иной характер: она оценивается по степени выраженности апоптоза — усиление или ослабление при тех или иных болезнях.
Источник: alexmed.info
Что относится к клеточным включениям, какова их роль в клетке?
По сути включения — это продукты метаболизма, способные накапливаться в виде гранул, зерен или капель с разной химической структурой. Редко могут встречаться в ядре.
Формируются они в основном в пластинчатом комплексе и в эндоплазматическом ретикулуме. Часть — результат неполного переваривания (гемосидерин).
Процесс расщепления и удаления зависит от происхождения. Секреторные включения выводятся через протоки, углеводные и липидные — расщепляются под действием ферментов, меланин разрушается клетками Лангерганса.
Классификация клеточных включений:
- Трофические (крахмал, гликоген, липиды);
- секреторные (включения поджелудочной железы, эндокринных органов);
- экскреторные (гранулы мочевой кислоты);
- пигментные (меланин, билирубин);
- случайные (медикаменты, кремний);
- минеральные (соли кальция).
Строение и функции
Жировые включения часто накапливаются в цитоплазме, как небольшие капли. Они характерны для одноклеточных, к примеру, инфузорий. У высших животных липидные капли находятся в жировой ткани. Чрезмерное накопление жировых включений приводит к патологическим изменениям в органах, к примеру, вызывает жировую дистрофию печени.
Полисахаридные имеют гранулярное строение различной формы и размеров. Наибольшие их скопления располагаются в клетках поперечнополосатой мускулатуры и печеночной ткани.

Включения белка встречаются не часто, главным образом являются питательным веществом в яйцеклетках (при микроскопическом исследовании можно увидеть разного рода пластинки, палочки).
Пигмент липофусцин — это включения желтого или коричневого цвета, которые скапливаются в клетках в процессе жизнедеятельности. Пигмент гемоглобин входит в состав эритроцитов крови. Родопсин — делает палочки сетчатки глаза чувствительными к свету.
| Строение и функции клеточных включений | |
|---|---|
| Трофические | Сюда относят белки, жиры и углеводы. В клетках животных, особенно в печени и мышечных волокнах, находится гликоген. При нагрузках и потреблении большого количества энергии он используется в первую очередь. У растений накапливается крахмал, как основной источник питания. |
| Экскреторные | Это продукты метаболизма клетки, которые не были из нее удалены. Сюда также относят чужеродных агентов, проникших во внутриклеточное пространство. Такие включения поглощаются и перерабатываются лизосомами. |
| Секреторные | Их синтез идет в специальных клетках, а после они выводятся наружу через протоки или с током лимфы и крови. К секреторной группе относятся гормоны. |
| Пигментные | Иногда представлены продуктами обмена: гранулы липофусцина или скопления гемосидерина. Находятся в меланоцитах, клетках имеющих окрас. Выполняют защитную функцию, предотвращая действие солнечных лучей. У простейших видов меланоциты находятся во многих органах, что придает животным различную окраску. У человека основная масса пигментных клеток находится в эпидермисе, часть в радужке глаза. |
| Случайные | Встречаются в клетках, способных к фагоцитозу. Захваченные бактерии, которые плохо перевариваются, остаются в цитоплазме в виде гранул. |
| Минеральные | Сюда относятся соли Ca, которые откладываются при снижении активной деятельности органа. Нарушение метаболизма иона приводит также к накоплению солей в матриксе митохондрий. |
Биологическое и медицинское значение клеточных включений
Избыточное скопление включений может привести к развитию серьезных патологий, которые принято называть болезнями накопления. Формирование заболевания связано со снижением активности лизосомальных ферментов и чрезмерным поступлением каких-либо веществ (жировое перерождение печени, гликогенозмышечной ткани).
Например, развитие наследственной болезни Помпе обусловлено дефицитом фермента кислая мальтаза, как следствие в клетках накаливается гликоген, что ведет к дистрофии нервной и мышечной ткани.
Скапливаться в цитоплазме могут свойственные для клетки вещества, а также чужеродные, которые в норме не встречаются (амилоидоз почек). Во время старения организма во всех клетках накапливается липофусцин, который служит маркером функциональной неполноценности клеток.
Чем отличаются органоиды от клеточных включений?
Органоиды — это постоянные структурные элементы клетки, необходимые для стабильной работы и жизнедеятельности.
Включения — это компоненты клетки, которые могут появляться и исчезать на протяжении ее жизни.
Источник: animals-world.ru
Клеточные включения
Помимо мембранных и немембранных органелл в клетках могут быть клеточные включения, представляющие собой непостоянные образования, то возникающие, то исчезающие в процессе жизнедеятельности клетки. Основное место локализации включений — цитоплазма, но иногда они встречаются и в ядре.
По характеру все включения — это продукты клеточного метаболизма. Они накапливаются главным образом в форме гранул, капель и кристаллов. Химический состав включений очень разнообразен.
Липоиды обычно откладываются в клетке в виде мелких капель. Большое количество жировых капель встречается в цитоплазме ряда простейших, например инфузорий. У млекопитающих жировые капли находятся в специализированных жировых клетках, в соединительной ткани. Часто значительное количество жировых включений откладывается в результате патологических процессов, например при жировом перерождении печени. Капли жира встречаются в клетках практически всех растительных тканей, очень много жира содержится в семенах некоторых растений.
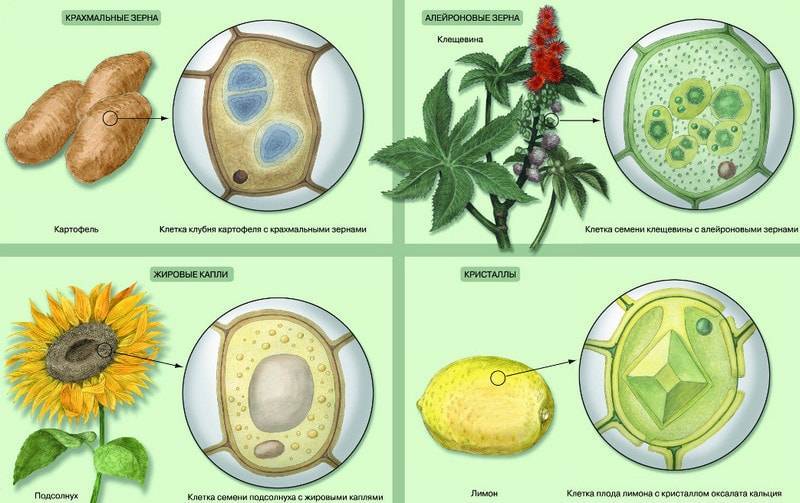
Включения полисахаридов имеют чаще всего формулу гранул разнообразных размеров. У многоклеточных животных и простейших в цитоплазме клеток встречаются отложения гликогена . Гранулы гликогена хорошо видны в световом микроскопе. Особенно велики скопления гликогена в цитоплазме поперечнополосатых мышечных волокон и в клетках печени, в нейронах. В клетках растений из полисахаридов наиболее часто откладывается крахмал. Он имеет вид гранул различной формы и размеров, причем форма крахмальных гранул специфична для каждого вида растений и для определенных тканей. Отложениями крахмала богата цитоплазма клубней картофеля, зерен злаков; каждая крахмальная гранула состоит их отдельных слоев, а каждый слой, в свою очередь, включает радиально расположенные кристаллы, почти невидимые в световой микроскоп.
Белковые включения встречаются реже, чем жировые и углеводные. Белковыми гранулами богата цитоплазма яйцеклеток, где они имеют форму пластинок, шариков, дисков, палочек. Белковые включения встречаются в цитоплазме клеток печени, клеток простейших и многих других животных.
К клеточным включениям относятся некоторые пигменты, например распространенный в тканях желтый и коричневый пигмент липофусцин , круглые гранулы которого накапливаются в процессе жизнедеятельности клеток, особенно по мере их старения. Сюда же относятся пигменты желтого и красного цвета — липохромы . Они накапливаются в виде мелких капель в клетках коркового вещества надпочечников и в некоторых клетках яичников. Пигмент ретинин входит в состав зрительного пурпура сетчатки глаза. Присутствие некоторых пигментов связано с выполнением этими клетками особых функций. Примерами могут служить красный дыхательный пигмент гемоглобин в эритроцитах крови или пигмент меланин в клетках меланофорах покровных тканей животных.
В качестве включений во многих животных клетках присутствуют гранулы секрета, вырабатываемого в клетках разных типов, в первую очередь в железистых. Секреторные включения могут быть белками, сахаридами, липопротеидами и т. д. См. Включения растительной клетки
Источник: medbiol.ru