Строение фагоцитоза
§ 3.1.4. Строение клетки
Размеры клетки широко варьируют от 0,1 мкм (некоторые бактерии) до 155 мм (яйцо страуса). У всех клеток, независимо от их формы, размеров, функциональной нагрузки обнаруживается сходное строение (рис. 3.13).

Рис. 3.13. Схема строения живой клетки: 1 – оболочка; 2 – мембрана; 3 – цитоплазма; 4 – ядро; 4а – ядрышко; 5 – рибосомы; 6 – эндоплазматическая сеть (ЭПС); 7 – митохондрии; 8 – комплекс гольджи; 9 – лизосомы; 10 – пластиды; 11 – клеточные включения
Снаружи клетка одета мембраной. Внутренняя часть клетки содержит многочисленные органоиды – структурные образования клетки, выполняющие определенные функции жизнедеятельности клетки.
1. Оболочка. Присутствует только у растительных клеток. Состоит из волокон целлюлозы. Функции оболочки: защита клетки от внешних повреждений, придает стабильную форму клетки, эластичность растительным тканям.
Повреждение наружной оболочки приводит к гибели клетки (цитолиз).
2. Мембрана. Тончайшая структура (75 Ǻ), состоит из двойного слоя молекул липидов и одного слоя белков. Такая структура обеспечивает уникальную эластичность и прочность мембране
Функции мембраны:
 участие в обмене веществ. Эта функция связана с избирательной проницаемостью в клетку определенных веществ и выведение из нее продуктов обмена. В процессе питания в клетку могут проникать определенные растворы веществ (пиноцитоз) и твердые частицы (фагоцитоз).
участие в обмене веществ. Эта функция связана с избирательной проницаемостью в клетку определенных веществ и выведение из нее продуктов обмена. В процессе питания в клетку могут проникать определенные растворы веществ (пиноцитоз) и твердые частицы (фагоцитоз).
Явление фагоцитоза – поглощение клеткой твердых частиц – впервые было описано русским врачом Мечниковым. Фагоцитарная особенность лежит в основе процесса иммунитета. Особенно развита у лейкоцитов, клеток костного мозга, лимфатических узлов, селезенки, надпочечников и гипофиза.
Пиноцитоз – поглощение клеткой растворов – состоит в том, что мельчайшие пузырьки жидкости втягиваются через образующуюся воронку, проникают через мембрану и усваиваются клеткой.
3. Цитоплазма – внутренняя среда клетки. Представляет собой гелеобразную жидкость (коллоидная система), состоит на 80 % из воды, в которой растворены белки, липиды, углеводы, неорганические вещества. Цитоплазма живой клетки находится в постоянном движении (циклоз).
Функции цитоплазмы:
 транспортировка питательных веществ и утилизация продуктов обмена клетки;
транспортировка питательных веществ и утилизация продуктов обмена клетки;
 буферность цитоплазмы (постоянство физико-химических свойств) обеспечивает гомеостаз клетки, поддерживает постоянные нужные параметры жизнедеятельности;
буферность цитоплазмы (постоянство физико-химических свойств) обеспечивает гомеостаз клетки, поддерживает постоянные нужные параметры жизнедеятельности;
 поддержание тургора (упругость) клетки;
поддержание тургора (упругость) клетки;
 все биохимические реакции происходят только в водных растворах, что обеспечивается в среде цитоплазмы.
все биохимические реакции происходят только в водных растворах, что обеспечивается в среде цитоплазмы.
4. Ядро – обязательный органоид эукариотических клеток. Впервые было исследовано и описано Р. Броуном в 1831 г. В молодых клетках расположено в центре клетки, в старых – смещается в сторону. Снаружи ядро окружено мембраной с крупными порами, способными пропускать крупные макромолекулы. Внутри ядро заполнено клеточным соком – кариоплазмой, основная часть ядра заполнена хроматином – ядерным веществом, содержащим ДНК и белок. Перед делением хроматин образует палочковидные хромосомы. Причём, хромосомы одинакового строения (но содержащие разные ДНК!) образуют пары, зрительно воспринимаемые как одно целое (рис. 3.14).

Рис. 3.14. Хромосомный набор человеческой клетки перед началом деления
Структурирование всех хромосом в пары свидетельствует о том, что число хромосом – чётное. Поэтому, его часто обозначают 2n, где n – количество хромосомных пар, а соответствующий набор хромосом называют диплоидным. Например, у голубей n = 40 (80 хромосом), у мухи n = 6 (12 хромосом), у собаки n = 39 (78 хромосом), у аскариды n = 1 (2 хромосомы). У человека n = 23 (46 хромосом). Однако, в половых клетках число хромосом в два раза меньше. Поэтому набор хромосом в половых клетках называется гаплоидным. Клетки, не являющиеся половыми называются соматическими. Иногда клетки с гаплоидным набором хромосом называют гаплоидными клетками, а с диплоидным набором хромосом – диплоидными клетками.
При слиянии двух родительских гаплоидных половых клеток образуется диплоидная клетка, дающая начало новому организму с набором генов отца и матери
Совокупность всех хромосом ядра (а значит и генов) клетки называется генотип. Именно генотип определяет все внешние и внутренние признаки конкретного организма.
В соматических клетках 44 Х-образные хромосомы (22 пары) у женщин и мужчин идентичны (сходны по строению), их называют аутосомами. А 23-я пара имеет конфигурацию ХХ – у женщин и ХY – у мужчин. Эти пары хромосом именуются половыми хромосомами.
В половых клетках 22 хромосомы также одинаковые у яйцеклеток и у сперматозоидов, а 23-я хромосома конфигурации Х – у яйцеклетки и Х или Y – у сперматозоидов. Поэтому при слиянии половых клеток и образовании пар хромосом, 23-я пара будет ({ХY} или {ХХ}) определять пол будущего ребенка.
Необходимо помнить, что хотя в соматических клетках набор хромосом диплоидный (2n), однако, перед началом деления клеток происходит репликация ДНК, то есть, удвоение их количества, а, значит, и удвоение
количества хромосом. Поэтому перед началом деления соматической клетки в ней насчитывается 4n хромосом (рис. 16). Она становится тетраплоидной.
Функции ядра:
– хранение генетической информации;
– контроль за всеми процессами, происходящими в клетке: делением, дыханием, питанием и др.
4а. Ядрышко – структура, содержащаяся в ядре. Ядро может содержат 1, 2 или более ядрышек. Функция ядрышка – формирование рибосом.
Следует отметить, что не все клетки имеют оформленное ядро. Клетки, имеющие ядро называются эукариотическими или эукариотами. Клетки, не имеющие ядра, называются прокариотическими или прокариотами. Функции ядра у прокариот несёт одна нить ДНК (именуется хромосома), в которой хранится вся генетическая информация. К прокариотам относятся бактерии и сине-зеленые водоросли. Как правило, у прокариотов отсутствуют и некоторые другие органоиды. Размеры прокариотических клеток меньше, чем размеры эукариот.
5. Рибосомы – самые мелкие органоиды клетки. Были обнаружены в 1954 г. Французским ученым Паладом. Рибосомы были обнаружены в цитоплазме, а также на гранулярной ЭПС и в ядре.
Функция рибосом: обеспечение биосинтеза белка.
6. Эндоплазматическая сеть. Представляет собой каналы и полости, ограниченные мембраной. Различают две разновидности ЭПС: гранулярная ЭПС и агранулярная ЭПС. Гранулярная ЭПС морфологически отличается от агранулярной наличием на ее поверхности многочисленных рибосом (на агранулярной ЭПС рибосомы отсутствуют).
Функции эндоплазматической сети:
– участие в синтезе органических веществ: на гранулярной ЭПС синтезируются белки, на агранулярной – липиды и углеводы;
– транспортировка продуктов синтеза ко всем частям клетки.
Несложно уяснить, что гранулярная ЭПС характерна для клеток, синтезирующих белки (например клетки желез внутренней секреции), агранулярная ЭПС характерна для клеток-производителей углеводов и липидов (например клетки жировой ткани).
7. Митохондрии – крупные органоиды, состоящие из двойного слоя мембран: наружная – гладкая, внутренняя образует многочисленные гребнеобразные складки – кристы. Внутри митохондрии заполнены жидкостью (матрикс).
Функции митохондрий: основная функция митохондрий – обеспечение клетки энергией. Этот процесс происходит за счет синтеза аденозинтрифосфорной кислоты (АТФ) (рис. 3.15), в которой фрагмент


Рис. 3.15. Структурная формула аденозинфосфорных кислот. Для аденозинтрифосфорной кислоты n = 3, для аденозиндифосфорной кислоты n = 2, для аденозинмонофосфорной кислоты n = 1
При взаимодействии молекулы аденозинтрифосфорной кислоты с водой отщепляется один остаток фосфорной кислоты, в результате чего образуется аденозиндифосфорная кислота – АДФ и выделяется огромное количество энергии:
АТФ + Н2О = АДФ + Н3РО4 + 10 000 калорий.
Впоследствии от АДФ может отщепляться еще один остаток фосфорной кислоты, образуя АМФ – аденозинмонофосфорную кислоту.
АДФ + Н2О = АМФ + Н3РО4 + 10 000 калорий[37].
Освободившаяся энергия используется для жизнедеятельности клетки (КПД процесса превышает 80 %!).
Наряду с распадом АТФ и выделением энергии в клетке постоянно происходит синтез АТФ и накопление энергии (обратные реакции).
Количество митохондрий в клетке зависит от потребности последней в энергии. Так, в клетках кожи человека находится в среднем 5–6 митохондрий, в клетках мышц – до 1000, в клетках печени – до 2500!
8. Комплекс Гольджи. Итальянский ученый Гольджи обнаружил и описал структуру клетки, напоминающую стопки мембран, цистерны, пузырьки и трубочки. Расположена эта система чаще всего возле ядра.
Функции комплекса Гольджи: в полостях комплекса накапливаются всевозможные продукты обмена клетки, которые по каким-либо причинам не вывелись наружу. В последствии эти продукты могут быть использованы клеткой для процессов жизнедеятельности. Из пузырьков и цистерночек комплекса Гольджи в растительных клетках образуются вакуоли, заполненные клеточным соком.
9. Лизосомы – мелкие органоиды. Представляют собой пузырьки, окруженные мембраной. Внутри лизосомы заполнены пищеварительными ферментами (обнаружено 12 ферментов), которые расщепляют и переваривают крупные макромолекулы (белки, полисахариды, нуклеиновые кислоты).
Функции лизосом: растворение и переваривание макромолекул. Лизосомы участвуют в фагоцитозе. Понятно, что основная функция по перевариванию поступающих в клетку частиц принадлежит лизосомам.
10. Пластиды. Эти органоиды характерны только для растительных клеток. Форма напоминает двояковыпуклую линзу. Структура пластид напоминает таковую у митохондрий: двойной слой мембраны. Наружная – гладкая, внутренняя образует складки, называемые тилакоидами. На тилакоидах происходит основной жизненно важный для всех зеленых растений процесс – фотосинтез:

Пластиды бывают трех типов:
1) Хлоропласты – зеленые пластиды. Их цвет обусловлен наличием хлорофилла. Хлорофилл – основное вещество хлоропластов (имеет зеленый цвет). Только благодаря хлорофиллу возможен процесс фотосинтеза (см. раздел 4.2). Хлоропласты придают зеленый цвет растительным организмам.
2) Хромопласты – пластиды, имеющие различные окраски: от ярко-желтого до пурпурно-багряного. Наличие различных пигментов окрашивают плоды, цветки и осенние листья растений в соответствующие цвета. Этот факт особенно важен для привлечения насекомых к цветкам, как природный индикатор созревания плодов и др.
3) Лейкопласты – бесцветные пластиды, в которых происходит накопление запасных питательных веществ (например, крахмала).
Некоторые виды пластид могут переходить друг в друга: например, переход хлоропластов в хромопласты: созревание томатов, яблок, вишни, и т. д.; изменение окраски листьев в осенний период времени. Лейкопласты могут переходить в хлоропласты: позеленение картофеля на свету. Это доказывает общность происхождения пластид.
11. Клеточные включения. Вакуоли. Это непостоянные и необязательные составляющие клетки. Они могут появляться и исчезать в течение всей жизни клетки. К ним относятся капли жира, зерна крахмала и гликогена, кристаллы щавелево-кислого кальция и др. Жидкие продукты обмена называются клеточным соком и накапливаются они в вакуолях. В клеточном соке растворены сахара, минеральные соли, пигменты и т. д. Чем старше клетка, тем больше клеточного сока накапливает клетка. Молодые клетки практически не содержат вакуолей.
Помимо перечисленного некоторые специализированные клетки обладают специальными органоидами. К ним относятся:
– реснички и жгутики, представляющие собой выросты мембраны клетки, осуществляющие движения клетки. Они имеются у одноклеточных организмов и многоклеточных (кишечный эпителий, сперматозоиды, эпителий дыхательных путей);
– миофибриллы – тонкие нити мышечных клеток, участвующие в сокращении мышц;
– нейрофибриллы – органоиды, характерные для нервных клеток и участвующие в проведении нервных импульсов. Кроме того, в состав клеток входят центриоли – две (иногда более) цилиндрические структуры диаметром около 0,1 мкм и длиной 0,3 мкм. Место расположения центриолей в период между делениями клетки считается серединой клеточного центра. При делении клетки центриоли расходятся в противоположные стороны – к полюсам, определяя ориентацию веретена деления (рис. 16).
Следует иметь в виду, что, хотя животные и растительные клетки имеют много общего, но между ними существуют и серьёзные различия (табл. 3.1).
Более общая классификация клеток представлена на рис. 3.16.
Одно из основных отличий бактерий от архей, состоит в химическом составе мембраны. Бактерии отделены от внешней среды двойным слоем липидов (жиров и жироподобных веществ). Мембраны архей состоят из терпеновых спиртов.
Таблица 3.1
Отличия растительной клетки от животной
|
Признаки |
Растительная клетка |
Животная клетка |
|
|
1 |
Оболочка |
Есть |
Нет (Мембрана есть) |
|
2 |
Пластиды |
Есть |
Нет |
|
3 |
Клеточные включения |
Вакуоли, кристаллы щавелево-кислого кальция, зёрна крахмала |
Капли жира, зёрна гликогена |
|
4 |
Питание |
Пиноцитоз (фагоцитоз невозможен из-за наличия плотной оболочки) |
Фагоцитоз, пиноцитоз |
|
5 |
Органоиды движения |
Нет |
Реснички, жгутики, ложноножки, миофибриллы, нейрофибриллы |

Рис. 3.16. Классификация клеток
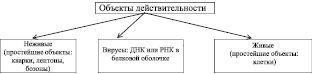
При попытке разделить все объекты действительности на живые и неживые выяснилось, что существуют объекты, которые невозможно однозначно отнести ни к живым, ни к неживым. Такие объекты назвали вирусами. Вне клетки они представляют собой неживой химический комплекс ДНК или РНК с молекулами белка. Внутри клетки существование вирусов приобретает форму жизни, то есть они вступают в вещественно-энергетический обмен с содержимым клетки и размножаются.
Таким образом, с учётом живых организмов, классификация всех объектов действительности может выглядеть так, как это представлено на рис. 3.17.

Рис. 3.17. Классификация объектов действительности
1. Обоснуйте утверждение, что ядро – это основная составляющая клетки. Раскройте значение и функции ядра.
2. К какому типу клеток (гаплоидные или диплоидные) относятся следующие примеры: клетка кожи, спора, клетка кожицы лука, клетка печени, сперматозоид, лейкоцит, пыльца, куриное яйцо?
3. В чем состоят основные функции мембранных органоидов: ЭПС, аппарата Гольджи, рибосом и лизосом.
4. Какие существуют виды пластид? Каково их значение для растительной клетки?
5. Что такое митохондрии? Какие процессы в них происходят? Каково их значение?
6. В чем состоят различия между животной и растительной клеткой? Проанализируйте – почему они возникли?
Источник: monographies.ru
История
Фагоцитоз был впервые отмечен канадским врачом Уильямом Ослером (1876)[1], а затем изучен и назван Ильей Ильичом Мечниковым в 1882 году, когда им же была установлена роль фагоцитов в защите от бактерий[2]. Он предположил, что клетки, захватывающие и переваривающие органические тела, помимо их участия в пищеварении, выполняют в организме защитную функцию. Мечников подтверждал свое предположение, проделывая опыты с морскими звёздами и дафниями, вводя в их организмы инородные тела. Например, когда Мечников поместил в тело дафнии спору грибка, то он заметил, что на неё нападают особые подвижные клетки. Когда же он ввёл слишком много спор, клетки не успели их все переварить, и животное погибло. Клетки, защищающие организм от бактерий, вирусов, спор грибов и пр., Мечников назвал фагоцитами, а само явление — фагоцитозом. Летом 1883 года на съезде естествоиспытателей и врачей Мечников сообщил об открытии явления фагоцитоза. За труды по иммунитету Мечников получил Нобелевскую премию по физиологии и медицине (1908).
Фагоциты
У человека различают два типа профессиональных фагоцитов:
- нейтрофилы
- моноциты
У некоторых других животных фагоцитировать могут ооциты, плацентные клетки, клетки, выстилающие полость тела, пигментный эпителий сетчатки глаза[3].
Этапы фагоцитоза
Основные этапы фагоцитарной реакции сходны для клеток обоих типов. Реакция фагоцитоза может быть подразделена на несколько этапов:
1. Хемотаксис. В реакции фагоцитоза более важная роль принадлежит положительному хемотаксису. В качестве хемоаттрактантов выступают продукты выделяемые микроорганизмами и активированными клетками в очаге воспаления (цитокины, лейкотриен В4, гистамин), а также продукты расщепления компонентов комплемента (С3а, С5а), протеолитические фрагменты факторов свертывания крови и фибринолиза (тромбин, фибрин), нейропептиды, фрагменты иммуноглобулинов и др. Однако, «профессиональными» хемотаксинами служат цитокины группы хемокинов.
Ранее других клеток в очаг воспаления мигрируют нейтрофилы, существенно позже поступают макрофаги. Скорость хемотаксического перемещения для нейтрофилов и макрофагов сопоставима, различия во времени поступления, вероятно, связаны с разной скоростью их активации.
2. Адгезия фагоцитов к объекту. Обусловлена наличием на поверхности фагоцитов рецепторов для молекул, представленных на поверхности объекта (собственных или связавшихся с ним). При фагоцитозе бактерий или старых клеток организма хозяина происходит распознавание концевых сахаридных групп — глюкозы, галактозы, фукозы, маннозы и др., которые представлены на поверхности фагоцитируемых клеток. Распознавание осуществляется лектиноподобными рецепторами соответствующей специфичности, в первую очередь маннозосвязывающим белком и селектинами, присутствующими на поверхности фагоцитов.
В тех случаях, когда объектами фагоцитоза являются не живые клетки, а кусочки угля, асбеста, стекла, металла и др., фагоциты предварительно делают объект поглощения приемлемым для осуществления реакции, окутывая его собственными продуктами, в том числе компонентами межклеточного матрикса, который они продуцируют.
Хотя фагоциты способны поглощать и разного рода «неподготовленные» объекты, наибольшей интенсивности фагоцитарный процесс достигает при опсонизации, то есть фиксации на поверхности объектов опсонинов к которым у фагоцитов есть специфические рецепторы — к Fc-фрагменту антител, компонентам системы комплемента, фибронектину и т. д.
3. Активация мембраны. На этой стадии осуществляется подготовка объекта к погружению. Происходит активация протеинкиназы С, выход ионов кальция из внутриклеточных депо. Большое значение играют переходы золь-гель в системе клеточных коллоидов и актино-миозиновые перестройки.
4. Погружение. Происходит обволакивание объекта.
5. Образование фагосомы. Замыкание мембраны, погружение объекта с частью мембраны фагоцита внутрь клетки.
6. Образование фаголизосомы. Слияние фагосомы с лизосомами, в результате чего образуются оптимальные условия для бактериолиза и расщепления убитой клетки. Механизмы сближения фагосомы и лизосом неясны; вероятно, происходит активное перемещение лизосом к фагосомам.
7. Киллинг и расщепление. Велика роль клеточной стенки перевариваемой клетки. Основные вещества, участвующие в бактериолизе: пероксид водорода, продукты азотного метаболизма, лизоцим и др. Процесс разрушения бактериальных клеток завершается благодаря активности протеаз, нуклеаз, липаз и других ферментов, активность которых оптимальна при низких значениях pH.
8. Выброс продуктов деградации.
Фагоцитоз может быть:
- завершённым (киллинг и переваривание прошло успешно);
- незавершённым (для ряда патогенов фагоцитоз является необходимой ступенью их жизненного цикла, например, у микобактерий и гонококков).
См. также
- Микроглия
- Трансцитоз
Источник: wiki2.org
Объекты фагоцитоза
Объектами фагоцитоза для микрофагов являются микроорганизмы и инородные неживые частицы, а для макрофагов — повреждённые, погибшие и разрушенные клетки (чужеродные и собственного организма), а также инородные неживые частицы.
Стадии фагоцитоза. Механизмы фагоцитоза.
Применительно к процессу фагоцитоза применяют следующие уточняющие определения:
-
Собственно фагоцитоз: поглощение клеток, их фрагментов и их внутриклеточное переваривание.
-
Незавершённый фагоцитоз.
-
Иммунный (специфический) фагоцитоз и опсонизация.
-
Неспецифический фагоцитоз характерен, например, для альвеолярных макрофагов, захватывающих пылевые частицы различной природы, сажу и т.п.
-
Ультрафагоцитоз — захватывание фагоцитом мелких корпускулярных частиц (пыли, попадающей с воздухом в лёгкие, или инородных частиц в тканях).
Стадии фагоцитоза. В процессе фагоцитоза условно выделяют несколько основных стадий:
-
Сближение фагоцита с объектом фагоцитоза.
-
Распознавание фагоцитом объекта поглощения и адгезия к нему.
-
Поглощение объекта фагоцитом с образованием фаголизосомы.
-
Разрушение объекта фагоцитоза.
Сближение фагоцита с объектом фагоцитоза. Первая стадия фагоцитоза — сближение фагоцита с объектом фагоцитоза — рассмотрена выше в разделе главы 5 «Направленная миграция лейкоцитов».
Распознавание объекта фагоцитоза. К наиболее существенным этапам относятся: распознавание поверхностных детерминант объекта фагоцитоза, опсонизация, адгезия фагоцита к объекту фагоцитоза, экспрессия на поверхности фагоцита гликопротеинов HLA I и II.
-
Распознавание поверхностных детерминант объекта фагоцитоза. Большинство объектов идентифицируется с помощью рецепторов на поверхности лейкоцитов. К таким объектам относятся микроорганизмы, грибы, паразиты, собственные повреждённые или опухолевые, или ви-руссодержащие клетки, а также фрагменты клеток.
-
Опсонизация (иммунный фагоцитоз) — связывание AT с клеточной стенкой микроорганизма с последующим эффективным поглощением образовавшегося комплекса фагоцитом при взаимодействии Fc-фрагмента AT с соответствующим Fc-рецептором (FcR) на мембране фагоцита. Наиболее активные опсонины: Fc-фрагмент IgG, IgM, факторы комплемента C3bi, лектины.
IgG. Бактерия, покрытая молекулами IgG, эффективно фагоцитируется макрофагом или нейтрофилом. Fab-фрагменты IgG связываются с антигенными детерминантами на поверхности бактерии, после чего те же молекулы IgG своими Fc-фрагментами взаимодействуют с рецепторами Fc-фрагментов, расположенными в плазматической мембране фагоцита, и активируют фагоцитоз.
IgM. Большая молекула IgM легко активирует комплемент и служит опсонином при фагоцитозе. Многие AT к грамотрицательным бактериям являются IgM.
Адгезия фагоцита к объекту фагоцитоза реализуется с участием рецепторов лейкоцита FcyR (при наличии у объекта соответствующего лиганда) и молекул адгезии (при отсутствии лиганда, например, у неклеточных частиц). При фагоцитозе в зернистых лейкоцитах происходит активация реакций метаболизма («метаболический взрыв»), что обеспечивает ряд важных событий: экспрессию гликопротеинов HLA I и II и молекул адгезии, респираторный взрыв, а также дегрануляцию лейкоцитов.
Метаболический взрыв. К наиболее значимым метаболическим изменениям относятся активация реакций пентозофосфатного шунта, усиление гликолиза, потенцирование глико-генолиза, накопление восстановленного НАДФ.
Дегрануляция лейкоцитов. Дегрануляция нейтрофилов, эозинофилов и базофилов сопровождается высвобождением в интерстициальную жидкость медиаторов воспаления (например, ИЛ-1 и ИЛ-6, ФНО, лейкотриенов) и активных форм кислорода, образовавшихся при респираторном взрыве.
Поглощение объекта и образование фаголизосомы. Фагоцитируемый материал погружается в клетку в составе фагосомы — пузырька, образованного плазматической мембраной. К фагосоме устремляются лизосомы и выстраиваются по её периметру. Затем мембраны фагосомы и ли-зосом сливаются и образуется фаголизосома. В образовании фаголизосомы принимают участие и специфические гранулы нейтрофильного лейкоцита — видоизменённые лизосомы, а для самого процесса слияния необходимы мик-рофиламенты цитоскелета, Са2+, протеинкиназа С.
Погружение объекта фагоцитоза в лейкоцит сопровождается секрецией медиаторов воспаления и других компонентов специфических гранул лейкоцита. При дегрануляции все эти факторы поступают в воспалительный экссудат, где оказывают бактериолитическое и цитолитическое действие.
Внутриклеточное «переваривание». Разрушение объекта фагоцитоза — внутриклеточное «переваривание» — реализуется в результате активации двух сложных механизмов: кислородзависимой (респираторный взрыв) и кислороднезависимой цитотоксичности фагоцитов.
Кислороднезависимые механизмы активируются в результате контакта опсонизированного объекта с мембраной фагоцита. В процессе фагосомо-лизосомального слияния первыми с мембраной фагосомы сливаются гранулы, содержащие лактоферрин и лизоцим, затем к ним присоединяются азурофильные гранулы, содержащие катионные белки (например, САР57, САР37), протеиназы (например, эластаза и коллагеназа), катепсин G, дефен-зины и др. Эти химические соединения вызывают повреждение клеточной стенки и нарушение некоторых метаболических процессов; в большей степени их активность направлена против грамположительных бактерий.
Кислородзависимая цитотоксичность фагоцитов играет ведущую роль в деструкции объекта фагоцитоза. Цитотоксичность сопряжена со значительным повышением интенсивности метаболизма с участием кислорода. Этот процесс получил название метаболического (дыхательного, респираторного, кислородного) взрыва. При этом потребление кислорода фагоцитом может увеличиться в течение нескольких секунд во много раз.
В результате дыхательного взрыва образуются цитотоксичные метаболиты кислорода (так называемые активные формы кислорода), свободные радикалы и перекисные продукты органических и неорганических соединений.
К этому времени в цитоплазме фагоцита накапливается большое количество восстановленного НАДФ. НАДФ-оксидаза (флавопротеин цитох-ромредуктаза) плазматической мембраны и цитохром b в присутствии хинонов трансформируют О2 в анион супероксида (О2~), проявляющий выраженное повреждающее действие.
В последующих реакциях О2~ может трансформироваться в другие активные формы: синглетный кислород, гидроксильный радикал (ОН—), пероксид водорода. Последний процесс катализирует СОД.
Пероксид водорода (Н2О2) проявляет меньший, чем О2~~ повреждающий эффект, но в присутствии миелопероксидазы конвертирует ионы С1~ в ионы НСlO-, обладающие бактерицидным свойством, во многом аналогичным эффекту хлорной извести (NaCIO).
Образующиеся активные радикалы обусловливают повреждение и деструкцию белков и липидов мембран, нуклеиновых кислот и других химических соединений объекта фагоцитоза. При этом сам фагоцит защищен от действия указанных выше агентов, поскольку в его цитоплазме имеются комплексы защитных неферментных факторов (глутатион, витамины Е, С, жирные кислоты) и ферментов (СОД, устраняющая супероксидный анион, глутатионпероксидаза и каталаза, инактивирую-щие Н2О2).
Повреждённый кислородзависимыми и независимыми механизмами объект фагоцитоза подвергается деструкции с участием лизосомальных ферментов. Образовавшиеся продукты какое-то время хранятся в остаточных тельцах и могут утилизироваться клеткой или выводиться из неё путём экзоцитоза.
-
Восстановительные процессы в очаге воспаления. Пролиферация и регенерация.
Пролиферация является завершающей фазой развития воспаления, обеспечивающей репаративную регенерацию тканей на месте очага альтерации. Пролиферация развивается с самого начала воспаления наряду с явлениями альтерации и экссудации.
При репаративных процессах в очаге воспаления регенерация клеток и фиброплазия достигаются как активацией процессов пролиферации, так и ограничением апоптоза клеток. Размножение клеточных элементов начинается по периферии зоны воспаления, в то время как в центре очага могут еще прогрессировать явления альтерации и некроза. Полного развития пролиферация соединительнотканных и органоспецифических клеточных элементов достигает после «очистки» зоны повреждения от клеточного детрита и инфекционных возбудителей воспаления тканевыми макрофагами и нейтрофилами. В связи с этим следует отметить, что процессу пролиферации предшествует формирование нейтрофильного и моноцитарного барьеров, которые формируются по периферии зоны альтерации.
Восстановление и замещение поврежденных тканей начинается с выхода из сосудов молекул фибриногена и образования фибрина, который формирует своеобразную сетку, каркас для последующего клеточного размножения. Уже по этому каркасу распределяются в очаге репарации быстро образующиеся фибробласты. Деление, рост и перемещение фибробластов возможны только после их связывания с фибрином или коллагеновыми волокнами. Эта связь обеспечивается особым белком — фибронектином. Размножение фибробластов начинается по периферии зоны воспаления, обеспечивая формирование фибробластического барьера. Хемотаксис, активация и пролиферация фибробластов осуществляются под воздействием:
-
Факторов роста фибробластов.
-
Тромбоцитарного фактора роста.
-
Цитокинов — ФНО, ИЛ-1.
-
Кининов.
-
Тромбина.
-
Трансформирующего фактора роста b.
Сначала фибробласты незрелые и не обладают достаточной синтетической активностью. Созреванию предшествует внутренняя структурно-функциональная перестройка фибробластов: гипертрофия ядра и ядрышка, гиперплазия ЭПС, повышение содержания ферментов, особенно щелочной фосфатазы, неспецифической эстеразы, b-глюкуронидазы. Только после перестройки фибробласты начинают синтезировать коллаген, эластин, коллагенассоциированные белки и протеогликаны. Коллагеногенез стимулируется следующими биологически активными веществами — ФНО, ИЛ-1, ИЛ-4, фактором роста фибробластов, тромбоцитарным фактором роста.
Интенсивно размножающиеся фибробласты продуцируют кислые мукополисахариды — основной компонент межклеточного вещества соединительной ткани (гиалуроновую кислоту, хондроитинсерную кислоту, глюкозамин, галактозамин). При этом зона воспаления не только инкапсулируется, но и начинаются постепенная миграция клеточных и бесклеточных компонентов соединительной ткани от периферии к центру, формирование соединительнотканного остова на месте первичной и вторичной альтерации.
Наряду с фибробластами размножаются и другие тканевые и гематогенные клетки. При разрушении базальных мембран сосудов в зоне альтерации происходит миграция клеток эндотелия по градиенту ангиогенных факторов. Просвет новообразующегося капилляра формируется путем слияния внеклеточных пространств соседних эндотелиоцитов. Вокруг новообразующихся капилляров концентрируются тучные клетки, макрофаги, нейтрофилы, которые освобождают биологически активные вещества, способствующие пролиферации капилляров.
Важнейшими факторами, стимулирующими ангиогенез, являются:
1. Факторы роста фибробластов (основной и кислый).
2. Сосудистый эндотелиальный фактор роста.
3. Трансформирующие факторы роста b.
4. Эпидермальный фактор роста.
Фибробласты вместе с вновь образованными сосудами создают грануляционную ткань. Это, по существу, молодая соединительная ткань, богатая клетками и тонкостенными капиллярами, петли которых выступают над поверхностью ткани в виде гранул.
Основными функциями грануляционной ткани являются: защитная — предотвращение влияния факторов окружающей среды на очаг воспаления и репаративная — заполнение дефекта и восстановление анатомической и функциональной полноценности поврежденных тканей.
Формирование грануляционной ткани не строго обязательно. Это зависит от величины и глубины повреждения. Грануляционная ткань обычно не развивается при заживлении ушибленных кожных ранок или мелких повреждений слизистой оболочки. Грануляционная ткань постепенно превращается в волокнистую ткань, называемую рубцом. В рубцовой ткани уменьшается количество сосудов, они запустевают, уменьшается количество макрофагов, тучных клеток, снижается активность фибробластов. Небольшая часть клеточных элементов, располагающаяся среди коллагеновых нитей, сохраняет активность. Предполагают, что сохранившие активность тканевые макрофаги принимают участие в рассасывании рубцовой ткани и обеспечивают формирование более мягких рубцов.
Параллельно с созреванием грануляций происходит эпителизация раны. Она начинается в первые часы после повреждения, и уже в течение первых суток образуются 2-4 слоя клеток базального эпителия. Скорость эпителизации обеспечивается следующими процессами: миграцией, делением и дифференцировкой клеток. Эпителизация небольших ран осуществляется, в основном, за счет миграции клеток из базального слоя. Раны более крупные эпителизируются за счет миграции и митотического деления клеток базального слоя, а также дифференцировки регенерирующего эпидермиса. Новый эпителий образует границу между поврежденным и подлежащим слоем, он препятствует обезвоживанию тканей раны, уменьшению в ней электролитов и белков, а также предупреждает инвазию микроорганизмов.
В процессе пролиферации участвуют и органспецифические клеточные элементы органов и тканей. С точки зрения возможностей пролиферации органспецифических клеточных элементов все органы и ткани могут быть расклассифицированы на три группы:
К первой группе могут быть отнесены органы и ткани, клеточные элементы которых обладают активной или практически неограниченной пролиферацией, достаточной для полного восполнения дефекта структуры в зоне воспаления (эпителий кожи, слизистых оболочек дыхательных путей, слизистой желудочно-кишечного тракта, мочеполовой системы; гемопоэтическая ткань и др.).
Ко второй группе относятся ткани с ограниченными регенерационными способностями (сухожилия, хрящи, связки, костная ткань, периферические нервные волокна).
К третьей группе относятся те органы и ткани, где органоспецифические клеточные элементы не способны к пролиферации (сердечная мышца, клетки ЦНС). Основными факторами, регулирующими процессы пролиферации и дифференцировки клеток в очаге воспаления, являются:
-
Факторы роста, продуцируемые макрофагами, лимфоцитами, тромбоцитами, фибробластами и другими клетками, стимулированными в зоне воспаления. К ним относятся:
-
факторы роста эпидермиса (стимулятор пролиферации и созревания эпителия, стимулятор ангиогенеза);
-
трансформирующий фактор роста-a (стимулятор ангиогенеза);
-
трансформирующий фактор роста-b (хемоаттрактант фибробластов, стимулятор синтеза коллагена, фибронектина, ангиогенеза, ингибитор протеолиза);
-
тромбоцитарный фактор роста (стимулятор миграции, пролиферации и синтеза белка в клетках-мишенях, обладает провоспалительным эффектом);
-
фактор роста эндотелиоцитов;
-
фактор роста фибробластов кислый и основной (стимуляторы пролиферации всех клеток сосудистой стенки);
-
колониестимулирующие факторы (гранулоцитарный и макрофагальный стимуляторы дифференцировки, пролиферации и функциональной активности клеток гранулоцитарного и моноцитарного рядов) — цитокины (ФНО, ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-7), продуцируемые Т- и В-лимфоцитами, мононуклеарами, тучными клетками, фибробластами, эндотелиоцитами, обеспечивают хемотаксис, фиброгенез, ингибируют апоптоз, стимулируют процессы пролиферации в очаге воспаления. Ингибиторами роста для некоторых клеток служат те же цитокины, которые стимулируют пролиферацию других — это ФНО, трансформирующий фактор роста a и b- интерферон [16];
-
фактор роста нервов (стимулятор пролиферации, роста, морфогенеза симпатических нейронов, эпителиальных клеток). Ростовые факторы, взаимодействуя с рецепторами на клетках- мишенях, могут непосредственно стимулировать синтез ДНК в клетках или подготавливать внутриклеточные рецепторы и ферменты к митотической деятельности.
-
Пептид гена, родственного кальцитонину, стимулирует пролиферацию эндотелиальных клеток, а субстанция Р индуцирует выработку ФНО в макрофагах.
-
Простагландины группы Е потенцируют регенерацию путем усиления кровоснабжения.
-
Кейлоны и антикейлоны, продуцируемые различными клетками, действуя по принципу обратной связи, могут активировать и угнетать митотические процессы в очаге воспаления [2].
-
Полиамины (путресцин, спермидин, спермин), обнаруживаемые во всех клетках млекопитающих, жизненно необходимы для роста и деления клеток. Они обеспечивают стабилизацию плазматических мембран и суперспиральной структуры ДНК, защиту ДНК от действия нуклеаз, стимуляцию транскрипции, метилирование РНК и связывание ее с рибосомами, активацию ДНК-лигаз, эндонуклеаз, протеинкиназ и многие другие клеточные процессы. Усиленный синтез полиаминов, способствующих пролиферативным процессам, отмечается в очаге альтерации .
-
Циклические нуклеотиды: цАМФ ингибирует, а цГМФ активирует процессы пролиферации.
-
Роль медиаторов в развитии воспаления. Классификация и характеристика.
Медиаторы воспаления. Медиаторами воспаления называются биологически активные вещества, которые синтезируются в клетках или в жидкостях организма и оказывают непосредственное влияние на воспалительный процесс. Клеточные медиаторы были рассмотрены выше (см. табл. 2). Гуморальные медиаторы воспаления синтезируются в плазме и в тканевой жидкости в результате действия соответствующих ферментов. Первоначальной причиной появления (или увеличения количества) этих веществ является альтерация. Именно в результате повреждения клеток освобождаются и активируются лизосомальные ферменты, которые активируют другие ферменты, в том числе содержащиеся в плазме, в результате чего возникает целый ряд биохимических реакций. Поначалу они носят хаотический характер («пожар обмена»), а продукты расщепления не имеют физиологического значения, нередко токсичны. Постепенно, однако, в этом процессе появляется определенный биологический смысл. Протеолитические ферменты расщепляют белки не до конца, а только до определенного этапа (ограниченный протеолиз), в результате чего образуются специфические вещества, действующие целенаправленно и ызывающие специфический патофизиологический эффект. Оказалось, что одни из них действуют преимущественно на сосуды, повышая их проницаемость, другие — на эмиграцию лейкоцитов, третьи — на размножение клеток. Первым обнаружил определенный «порядок» и закономерность в процессе воспаления В. Менкин. В воспалительном экссудате он выявил и индивидуализировал химические вещества и сопоставил с ними определенные слагаемые воспаления: гиперемию, лейкоцитоз, хемотаксис.
Одним из клеточных медиаторов воспаления является гистамин. Он содержится в гранулах тканевых базофилов (тучные клетки или лаброциты) в комплексе с гепарином и химазой в неактивной форме. В. свободном состоянии он оказывает расширяющее действие на мелкие сосуды (капилляры, венулы), увеличивая проницаемость их стенки. В малых дозах гистамин расширяет артериолы, в больших — суживает венулы. Выброс гистамина осуществляется вместе с выбросом в окружающую среду всех или части гранул тканевых базофилов при их дегрануляции. Этому может способствовать воздействие тепла, ионизирующего или ультрафиолетового излучения, растворов солей, кислот, белков, синтетических полимеров и мономеров, поверхностно-активных веществ. Дегрануляция всегда наблюдается при иммунных реакциях, т.е. при взаимодействии антигена с антителом на поверхности тканевых базофилов.
Другим клеточным медиатором воспаления является серотонин. У человека он содержится в тромбоцитах, хромаффинных клетках слизистой оболочки кишок, а также в некоторых нервных структурах. При разрушении клеток серотонин поступает в среду, вызывая повышение проницаемости сосудов.
Тканевые базофилы вырабатывают также гепарин, роль которого при воспалении заключается в том, что он препятствует образованию фибрина на внутренней оболочке капилляров, способствуя также увеличению проницаемости их стенки.
Лимфокины — вещества белковой природы, образующиеся в лимфоцитах, также относятся к медиаторам воспаления. Описано более десяти различных лимфокинов. При воспалении наибольшее значение имеют три из них: фактор, угнетающий эмиграцию макрофагоцитов, фактор, активирующий макрофагоциты, фактор хемотаксиса.
В клетках крови (лейкоцитах, тромбоцитах и др.) образуется еще одна группа веществ, играющих важную роль в динамике воспаления. Это простагландины. Источником их образования являются фосфолипиды клеточных мембран. Нарушение строго упорядоченной структуры фосфолипидов в мембране делает их доступными действию фосфолипазы А2, в результате чего отщепляется арахидоновая кислота. С нее начинается каскад химических реакции, идущих в двух направлениях. Сели на арахидоновую кислоту действует фермент циклоксигеназа, то в итоге образуются простагландины (ПГЕ2, ПГФ2, ПГИ2) или простациклины (ПГИ2), если же свою активность проявляет прежде всего липоксигеназа, то получаются лейкотриены. Дальнейшее превращение простагландинов происходит под влиянием тромбоксансинтетазы, в результате чего образуется тромбоксан А. Последний вызывает сужение сосудов, агрегацию тромбоцитов, тромбоз, отек, боль.
Другой путь биосинтеза простагландинов заключается в том, что под влиянием простациклинсинтетазы образуется простациклин (ПГИ2). Этот процесс совершается в эндотелиоцитах, где и находится указанный фермент. Он оказывает действие, противоположное тромбоксану: расширяет сосуды и подавляет агрегацию тромбоцитов. Таким образом, арахидоновая кислота дает начало двум веществам с противоположным действием, причем выбор одного из путей биосинтеза, по-видимому, связан с состоянием эндотелия. В неповрежденных эндотелиальных клетках содержится достаточно простациклинсинтетазы и весь ПГГ2 превращается в простациклин. Если же эндотелий поврежден, то этого фермента будет недоставать и потому часть ПГГ превращается в тромбоксан 2. Арахидоновый каскад представляет интерес еще и потому, что в ходе его образуются свободные радикалы, которые могут повреждать клеточные мембраны, в том числе и лизосом.
Лейкотриены оказывают хемотаксическое и хемокинетическое (нецеленаправленное движение) действие, повышают проницаемость, вызывают сокращение гладких мышц, индуцируют образование тромбоксанов.
К медиаторам воспаления относятся также циклические нуклеотиды, которые правильнее было бы назвать не медиаторами, а модуляторами, так как они не создают полной картины воспаления, а могут лишь в той или иной степени преобразовывать ее. Циклические нуклеотиды обусловливают эффект действия других медиаторов, выделение клетками лизосомальных ферментов и др. Отмечено противоположно направленное действие цАМФ и цГМФ. Так, первый подавляет выделение гистамина и лизосомальных ферментов, а второй, наоборот, способствует ему.
Из гуморальных медиаторов воспаления наибольшее значение имеют кинины — группа вазоактивных полипептидов, образующихся в результате каскада биохимических реакций, начинающихся с активации фактора Хагемана (рис. 12.4). Соприкосновение с поврежденной поверхностью или изменение внутренней среды (температура, рН) приводит к тому, что этот фактор становится активным и действует на находящийся в плазме прекалликреин, превращая его в калликреин. Последний в свою очередь влияет на α2-глобулины, отщепляя от них полипептидную цепочку, состоящую из 9 (брадикинин) или 10 аминокислотных остатков (каллидин). Плазменные кинины оказывают непосредственное влияние на тонус и проницаемость сосудистой стенки, вызывая расширение прекапиллярных артериол и увеличивая проницаемость стенки капилляров. Кроме того, они обусловливают типичные для воспаления зуд и боль. Медиаторы калликреин-кининовой системы при воспалении влияют на реологические свойства крови, т.е. на ее способность находиться в жидком и текучем состоянии. Из рис. 12.4 видно, что активный фактор Хагемана может инициировать процессы кининообразования, гемокоагуляции и фибринолиза. Выпадение нитей фибрина и образование тромбов в зоне воспаления определенным образом связаны с состоянием калликреин-кининовой системы.
К гуморальным медиаторам воспаления относятся компоненты комплемента. Известно, что последний является важным защитным фактором организма, но вместе с этим он может способствовать повреждению собственных тканей, что бывает при воспалении, особенно иммунном. Объясняется это тем, что из 9 компонентов комплемента 3 имеют ближайшее отношение к рассматриваемому процессу. Так, комплемент С5 обладает способностью фиксироваться на сенсибилизированных и несенсибилизированных антителами клетках и разрушать их мембраны. Фрагменты СЗа и С5а, а также трехмолекулярный комплекс С567 вызывают хемотаксис лейкоцитов. Наконец, клетки, нагруженные фрагментами С36, становятся объектом активного фагоцитоза.
|
Медиаторы воспаления |
||
|
Название |
Оказываемое действие |
Происхождение |
|
Клеточные медиаторы |
||
|
Гистамин |
Местное расширение сосудов, повышение их проницаемости, особенно венул |
Гранулы тучных клеток |
|
Серотонин |
Спазм посткапиллярных венул, повышение проницаемости стенки сосудов |
Тромбоциты, хромаффинные клетки слизистой оболочки пищеварительного канала |
|
Лизосомальные ферменты |
Вторичная альтерация, хемотаксис |
Гранулоциты, тканевые базофилы, макрофаги |
|
Катионные белки |
Повышение проницаемости стенки сосудов |
Нейтрофильные гранулоциты |
|
Продукты расщепления арахидоновой кислоты (кислые арахидониды) |
||
|
Простагландины (ПГЕ1) |
Проницаемость сосудов, отек, хемотаксис |
Арахидоновая кислота |
|
Тромбоксан (ТХА2) |
Агрегация тромбоцитов, вазоконстрикция, свертывание крови |
Тромбоциты |
|
Простациклин (ПГИ2) |
Дезагрегация тромбоцитов, расширение сосудов |
Эндотелиоциты |
|
Лейкотриены |
Хемотаксис, сокращение гладких мышц, отек |
Лейкоциты |
|
Гуморальные медиаторы |
||
|
Кинины (брадикинин, каллидин) |
Расширение капилляров, увеличение проницаемости, боль, зуд |
α2-глобулины крови |
|
Система комплемента (фрагменты СЗа, С5а) |
Хемотаксис, цитолиз |
Плазма крови |
-
Местные признаки и общие реакции при воспалениях. Механизмы развития.
Признаки острого воспаления и их основные причины подразделяют на местные и общие (системные).
Источник: studfile.net