Бактериофаги относят к
Фаголизис – процесс разрушения фагами микробов, обычно происходит в пораженном органе при спонтанном выздоровлении. В случае, если самовыздоровление не пришло, организму можно посодействовать введением соответственного бактериофага, приобретенного в критериях лекарственного предприятия. Бактериофагами именуют вирусы микробов, которые при встрече с чувствительными к ним микробными клеточками попадают вовнутрь и вызывают их растворение (лизис).
В переводе с греческого бактериофаг значит «пожиратель микробов». В природе эти мельчайшие организмы очень многообразны и составляют самую крупную из узнаваемых на сегодня групп вирусов. Фаги имеют хорошее от вирусов растений, животных и человека строение, более сложное. Они встречаются в атмосферных осадках, в воздухе, в почве, в еде, на предметах, коже, шерсти животных, словом, всюду, где встречаются бактерии.
В последние годы растет энтузиазм к бактериофагам, используемым в качестве кандидатуры лекарствам. И это логично, и те и другие препараты конкретно оказывают влияние на возбудителей зараз. Но лекарства, как понятно, гибельно действуют не только лишь на патогенную флору, да и на полезную. Бактериофаги, виды которых различны, действуют избирательно, лишь на «свою» бактерию, оставляя от нее осколки. Фактически, потому ученые и не стали выдумывать им наименования, ведь проще именовать их соответственно микробам, на которые они действуют.
Бактериофаги: виды
Выпускают стрептококковый, коли-протейный, клебсиеллезный, стафилококковый, синегнойный, сальмонеллезный, дизентерийный, брюшнотифозный бактериофаги, также «Интестифаг» и «Пиобактериофаг».
Активность препаратов определяется степенью их разведения, при которой происходит лизис чувствительной культуры. Так, титр 10 в 6-ой степени значит, что данный бактериофаг проявляет литические характеристики при разведении в 1 000 000 раз. При температуре 4-6 С препараты сохраняют свои характеристики до 12 лет.
Зависимо от формы выпуска различаются и активностью бактериофаги. Виды препаратов позволяют повлиять как на отдельных возбудителей, так и на несколько сходу. Монофаги действуют на несколько штаммов одной бактерии. К всеохватывающим продуктам (поливалентным) относят бактериофаг «Секстафаг», который сразу способен подавлять активность стафилококков, стрептококков, включая энтерококки, синегнойной и пищеварительной палочки, протея, клебсиеллы. Не считая того, существует «Интестифаг», созданный для исцеления пищеварительных зараз, он включает сальмонеллезный, брюшнотифозный, дизентерийный, протейный, если и стрептококковый (подавляющий энтерококки) фаги.
Употребляют препараты при дисбактериозах, пищеварительных инфекциях, воспалительных процессах мочеполовой системы и бронхо-легочного аппарата, для исцеления гнойно-септических процессов, также при заболеваниях полости рта и пазух носа. Их используют как вовнутрь, в том числе и в виде клизм, так и местно – для полосканий, промываний ран, спринцеваний. Например, «Бактериофаг клебсиелл поливалентный очищенный», созданный для исцеления озены, риносклеромы, зараз, вызванных бактерией клебсиелла пневмония, используют ингаляционно при поражениях трахеи, горла и глотки, вводят турунду, смоченную в воды, при отитах, употребляют для промываний при синуситах. При циститах, энтероколитах, уретритах, пневмониях продукт принимают вовнутрь.
Бактериофаги владеют массой преимуществ перед антибиотиками. Они не имеют побочных действий, их назначают даже новорожденным и беременным дамам, они не вызывают привыкания. Их можно соединять с хоть какими фармацевтическими средствами, также использовать для профилактики заразных заболеваний. Эти препараты оказывают благотворное воздействие на становление иммунитета, не подавляют естественную флору, их действие проявляется в течение 2-4 часов после приема. К ним не развивается резистентность патогенных микробов.
Один недочет имеют бактериофаги. Виды их, применяемые сейчас в медицине, пока малочисленны, что ограничивает их применение при многих инфекциях.
Перспективы внедрения
Для того чтоб удачно использовать биопрепараты, нужно определять чувствительность к ним микробов. Но ученые увидели увлекательную закономерность: чувствительность микробов к фагам не понижается, а напротив, увеличивается, что разъясняют обогащением препаратов новыми культурами. На сегодня бактериофаг стафилококковый удачно лизирует до 90% всех штаммов этих микробов, выделяемых при гнойно-септических поражениях.
Многие инфекционисты считают, что фаготерапия скоро совершит революцию в борьбе с болезнями. Иммунологи лицезреют перспективу использования этих средств там, где бессильны иммунопрепараты. Согласно данным аналитических исследовательских работ, в наиблежайшие пару лет одним из самых многообещающих направлений фармакологии станет создание фагов.
Источник: live-note.ru
Впервые, предположение, что бактериофаги являются вирусами сделал. Д.Эррель. В дальнейшем открыты вирусы грибков и тд, называть стали фаги.
Морфология фага.
Размеры – 20 – 200нм. Большинство фагов имеют форму головастиков. Наиболее сложно устроенные фаги состоят из многогранной головки, в которой располагается нуклеиновая кислота, шейка и отростки. На конце отростка располагается базальная пластинка, с отходящими от нее нитями и зубцами. Эти нити и зубцы служат для прикрепления фага к оболочке бактерии. У наиболее сложноорганизованных фагов в дистальной части отростка, содержится фермент – лизоцим. Этот фермент способствует растворению оболочки бактерий при проникновении фаговой НК в цитоплазму. У многих фагов отросток окружен чехлом, который у некоторых фагов может сокращаться.
Различают 5 морфологических групп
- Бактериофаги с длинным отростком и сокращающимся чехлом
- Фаги с длинным отростком, но не сокращающимся чехлом
- Фаги с коротким отростком
- Фаги с аналогом отростка
- Нитевидные фаги
Химический состав.
Фаги состоят из нуклеиновой кислоты и белков. Большинство из них содержит 2хнитевую ДНК, замкнутую в кольцо. Некоторые фаги содержат одну нить ДНК или РНК.
Оболочка фагов – капсид, состоит из упорядоченных белковых субъединиц – капсомеров.
У наиболее сложноорганизованных фагов в дистальной части отростка, содержится фермент – лизоцим. Этот фермент способствует растворению оболочки бактерий при проникновении фаговой НК в цитоплазму.
Фаги хорошо переносят замораживание, нагревание до 70, высушивание. Чувствительны к кислотам, УФ и кипячению. Фаги инфицируют строго определенные бактерии, взаимодействую со специфическими рецепторами клеток.
По специфичности взаимодействия –
Полифаги – взаимодействующие с несколькими родственными видами бактерий
Монофаги – видовые фаги – взаимодействуют с одним видом бактерий
Типовые фаги – взаимодействуют с отдельными вариантами бактерий внутри вида.
По действию типовых фагов вид можно разделить на фаговый ряд. Взаимодействие фагов с бактериями может протекать по продуктивному, апродуктивному и интегративному типу.
Продуктивный тип – образуется фаговое потомство, а клетка лизируется
При апродуктивном – клетка продолжает существовать, процесс взаимодействия обрывается на начальной стадии
Вирулентные взаимодействуют с бактериями по продуктивному типу. В начале происходит абсорбция фага на оболочке бактерий, за счет взаимодействия специфических рецепторов. Имеет место проникновение или пенетрация вирусной нуклеиновой кислоты в цитоплазму бактерий. Под действием Лизоцима в оболочке бактерии образуется небольшое отверстие, чехол у фага сокращается и НК впрыскивается. Оболочка фага за пределами бактерии. Далее осуществляется синтез ранних белков. Они обеспечивают синтез фаговых структурных белков, репликацию фаговой нуклеиновой кислоты и репрессию деятельности бактериальной хромосом.
После этого происходит синтез структурных компонентов фагов и репликация нуклеиновой кислоты. Из этих элементов происходит сборка нового поколения фаговых частиц. Сборка носит название морфогенез, новых частиц, которых в одной бактерии может образовываться 10-100. Далее лизис бактерии и выход нового поколения фагов во внешнюю среду.
Умеренные бактериофаги взаимодействуют либо по продуктивному, либо по интегративному типу. Продуктивный цикл идет аналогично. При интегративном взаимодействии – ДНК умеренного фага после попадания в цитоплазму встраивается в хромосому в определенном участке, причем при делении клетки реплицируется синхронно с бактериальной ДНК и вот эти структуры передаются дочерним клеткам. Такая встроенная ДНК фага – профаг, а бактерия, содержащая профаг, называется лизогенной, а явление – лизогения.
Спонтанно, или под влиянием ряда внешних факторов профаг может вырезаться из хромосомы, т.е. переходить в свободное состояние, проявлять свойства вирулентного фага, что будет приводить к образованию нового поколения бактериальных тел – индукция профага.
Лизогенезация бактерий лежит в основе фаговой(лизогенной) конверсии. Под этим понимают изменение признаков или свойств у лизогенных бактерий, по сравнению с нелизогенными того же вида. Изменяться могут разные свойства – морфологические, антигенные и тд.
- Применение в диагностике. В отношение ряда вида бактерий монофаги, используются в реакция фаголизабельности, как один из критериев идентификации культуры бактерии, типовые фаги применяют для фаготипирования, для внутривидовой дифференциации бактерий. Проводятся с эпидимиологоическими целями, для установления источника инфекции и путей устранения
- Для лечения и профилактики ряда бактериальных инфекций – брюшной тип, стафилококковы и стрептококковые инфекции(таблетки с кислотоустойчивым покрытием)
- Умеренные бактериофаги применяют в генной инженерии в качестве вектора, способных вносить генетический материал в живую клетку.
Генетика бактерий
Бактериальный геном состоит из генетических элементов, способных к самовоспроизведению – репликонов. Репликонами является бактериальные хромосомы и плазмиды. Бактериальная хромосома формирует нуклеоид, замкнутым кольцом не связанным с белками и несет гаплоидный набор генов.
Плазмиды представляет собой также замкнутое кольцо молекулы ДНК, но гораздо меньших размеров чем хромосома. Наличии плазмид в цитоплазме бактерий не обязательно, но они придают преимущество в окружающей среде. Крупные плазмиды редуцируются с хромосомой и количество их в клетке небольшое. А число мелких плазмид может достигать нескольких десятков. Некоторые плазмиды способны обратимо встраиваться в бактериальную хромосому в определенном ее участке и функционировать в виде единого репликона. Такие плазмиды называются интегративными. Некоторые плазмиды способны передаваться от одной бактерии к другой при непосредственном контакте – коньюгативные плазмиды. Они содержат гены, ответственные за образование F-пилей, формирующих коньюгативный мостик, для передачи генетического материалы.
Основные типы плазмидов-
F – интегративная коньгативная плазмида. Половой фактор, определяет способность бактерий быть донорами при коньюгации
R – плазмиды. Резистентная. Содержит гены, детерминирующие синтез факторов, разрушающих антибактериальные препараты. Бактерии, обладающие такими плазмидами не чувствительны ко многим препаратам. Поэтому формируются устойчивые к препаратам фактор.
Токс плазмиды – детерминирующие факторы патогенности –
Ent – плазмиды – содержит ген за выработку энтеротоксинов.
Hly – разрушают эритроцит.
Подвижные генетические элементы. К ним относятся вставочные – инсерционные элементы. Общепринятое обозначение – Is. Это участки ДНК, способные перемещаться как внутри репликона, так и между ними. Они содержат только гены, необходимые для их собственного перемещения.
Транспозоны – более крупные структуры, обладающие темиже свойствами, что и Is, го помимо они содержат структурные гены, определяющие синтез биологических веществ, например токсинов. Подвижные генетические элементы могут вызывать инактивацию гена, повреждение генетического материала, слияние репликонов и распространение генов в популяции бактерий.
Изменчивость у бактерий.
Все виды изменчивости подразделяют на 2 группы – ненаследственная(фенотипическая, модификационная) и наследственная(генотипическая).
Модификации – фенотипчиеские не наследуемые изменения признаков или свойств. Модификации не затрагивают генотипа, а поэтому не передаются по наследству. Они являются адаптивными реакциями, на изменение каких то конкретных условий внешней среды. Как правило утрачиваются в первом поколении, после прекращения действия фактора.
Генотипическая изменчивость затрагивает генотип организма, а поэтому способна передаваться потомкам. Генотипическая изменчивость подразделяется на мутации и рекомбинации.
Мутации – стойкие, наследуемые изменения признаков или свойств организма. Основа мутаций – качественное или количественное изменение последовательности нуклеотидов в молекуле ДНК. Мутации могут изменять практически любые свойства.
По происхождению мутации – спонтанные и индуцируемые.
Спонтанные мутации происходит в естественных условиях существования организма, а индцированные возникают в результате направленного действия мутагенного фактора. ПО характеру изменений в первичной структуре ДНК у бактерий различают генные или точковые мутации и хромосомные аберрации.
Генные мутации происходят внутри одного гена и минимально захватывают один нуклеотид. Этот тип мутаций может быть следствием замены одно нуклеотида на другой, выпадения нуклеотида или вставления лишнего.
Хромосомные – могут затрагивать несколько хромосом.
Может быть делеция – потеря участка хромосомы, дупликация — удвоения участка хромосомы. Поворот участка хромосомы на 180 градусов – инверсия.
Любая мутация возникает под действием определенного мутагенного фактора. По своей природе мутагены – физические, химические и биологические. Ионизирующая радиация, рентгеновские лучи, УФ лучи. К химическим мутагенам – аналоги азотистых оснований, саму азотистую кислоту, и даже некоторые лекарственные средства, цитостатики. К биологическим – некоторые вирусы и трансфазоны
Рекомбинация – обмен участками хромосом
Трансдукция – перенос генетического материала с помощью бактериофага
Репарация генетического материала – восстановление возникших в результате мутаций повреждений.
Существует несколько видов репарации
- Фотореактивация – этот процесс обеспечивается специальным ферментом, который активируется в присутствии видимого света. Этот фермент перемещается по цепочке ДНК и восстанавливает повреждения. Объединяет тимеры, которые образуются при действии УФ. Более значимы результаты темновой репарации. Она не зависит от света и обеспечивается несколькими ферментами – вначале нуклеазы вырезают поврежденный участок цепи ДНК, затем ДНК полимераза, на матрице сохранившейся комплементарно цепи синтезирует заплату, а лигазы вшивают заплатку на поврежденное место.
Репарации подвергаются генные мутации, а хромосомные как правило нет
- Генетические рекомбинации у бактерий. Характеризуются проникновением генетического материала от бактерии донора в бактерию реципиента с формированием дочернего генома, содержащим генов обеих исходных особей.
Включение фрагмента ДНК донора в рецепиента происходит кроссинговером
Три типа передачи –
- Трансформация – процесс, при котором происходит передача фрагмента изолированной ДНК донора. Зависит от компетентности рецепиента и состояния донорской ДНК. Компетентность – способность поглощать ДНК. Она зависит от присутствия в клеточной мембране реципиента особых белков и формируется в определенные периоды роста бактерии. Донорская ДНК обязательно должна быть двухцепочечной и не очень большой по размеру. Донорская ДНК проникает через оболочку бактерий, причем одна из цепочек разрушается, другая встраивается в ДНК реципиента.
- Трансдукция – осуществляется с помощью бактериофагов. Общая трансдукция и специфическая трансдукция.
Общая – происходит при участии вирулентных факторов. В процессе сборки фагов частиц в головку фага по ошибке может включаться не фаговая ДНК, а кусочек хромосомы бактерий. Такие фаги – дефектные фаги.
Специфическая – она осуществляется умеренными фагами. При вырезании, вырезание его строго осуществляется по границе.Встраиваются между определёнными генами и переносят их.
- Коньюгация – передача генетического материала от бактерии донора рецепиенту, при их непосредственном контакте. Необходимым условием – наличие в клетке донора коньгативного плазмида. При коньюгации за счет пилей образуется коньюгационный мостик, по которому генетический материал передается от донора к пациенту.
Генодиагностика
-Комплекс методов, позволяющих выявить геном микроорганизма или его фрагмента в исследуемом материале. Первым был предложен метод гибридизации НК. Основан на использовании принципа комплиментарности. Этот метод позволяет выявить в генетическом материале наличие маркерных фрагментов ДНК возбудителя с помощью молекулярных зондов. Молекулярные зонды представляют собой короткие цепочки ДНК, комплементарные маркерному участку. В состав зонда вводится метка – флюорозром, радиоактивный изотоп, фермент. Исследуемый материал подвергается специальнйо обработке, позволяющей разрушить микрооргнаизмы, высвободить ДНК и разделить ее на одноцепочечные фрагменты. После этого материал фиксируется. Затем выявляется активность метки. Этот метод не отличается высокой чувствительностью. Можно выявить возбудителя лишь при достаточно большом его количестве. 10 в 4 микроорганизмов. Он достаточно сложен технически и требует большого количества зондов. Широкого распространения в практике он не нашел. Был разработан новый метод – полимеразная цепная реакция – ПЦР.
Этот метод основан на способности ДНК и вирусных РНК к репликации, т.е. к саморепродукции. Суть у пациента – является многократное копирование – амплификация in vitro фрагмента ДНК, являющего маркерного для данного микроорганищма. Так как процесс проходит при достаточно высоких температурах 70-90, то метод стал возможен после выделения из термофильных бактерий термостабильной ДНК-полимеразы. Механизм амплификации таков, что копирование цепочек ДНК начинается не в любой точке, а только в определенных стартовых блоках для создания которых используют так называемые праймеры. Праймеры представляют собой полинуклеотидные последовательности, комплиментарные концевым последовательностям копируемого фрагмента искомой ДНК, причем праймеры не только инициируют амплификацию, но и ограничивают. Сейчас существует несколько вариантов ПЦР характерны 3 этапа –
- Денатурация ДНК(разделение на 1 цепочечные фрагменты)
- Присоединение праймера.
- Комплиментарное достраивание цепей ДНК до 2хцепочечных
Этот цикл длится 1,5-2 минуты. В результате количество молекул ДНК удваивает 20-40 раз. В результате 10 в 8 степени копий. После амплификации производят электрофорез и выделяются в виде полосок. Она проводится в специальном приборе, который называется амплификатор.
Достоинства ПЦР
- Дает прямые указания на присутствие возбудителя в исследуемом материале, без выделения чистой культуры.
- Очень высокая чувствительность. Теоретически можно обнаружить 1го.
- Материал для исследования может быть сразу дизенфицировать после забора.
- 100% специфичность
- Быстрота получения результатов. Полный анализ – 4-5 часов. Экспресс метод.
Достаточно широко используется для диагностики инфекционных заболеваний, возбудителями которых являются не культивируемые или трудно культивируемые организмы. Хламидии, микоплазмы, многие вирусы – гепатита, герпеса. Разработаны тест системы для определения сибирской язвы, туберкулеза.
Рестрикционный анализ — с помощью ферментов молекула ДНК разделяется по определенным последовательностям нуклеоидов и фрагменты анализируются поп составу. Таким образом можно найти уникальные участки.
Биотехнология и генная инженерия
Биотехнология это наука, которая на основе изучения процессов жизнедеятельности живых организмов использует эти биопроцессы, а также сами биологические объекты для промышленно производства продуктов необходимых для человека, для воспроизведения биоэффектов, не проявляющихся в неестественных условиях. В качестве биологических объектов чаще всего используются одноклеточные микроорганизмы, а также клетки, животных и растений. Клетки очень быстро воспроизводятся, что позволяет за короткое время нарастить биомассу продуцента. В настоящее время биосинтез сложных веществ, таких как белки, антибиотики, экономичнее и технологически доступнее чем другие виды сырья.
Биотехнология использует сами клетки как источник целевого продукта а также крупные молекулы, синтезируемые клеткой, ферменты токсины, антитела и первичные и вторичные метаболиты – аминокислоты, витамины ,гормоны. Технология получения продуктов микробного и клеточного синтеза сводится к нескольким типовым стадиям – выбор или создание продуктивного штаба. Подбор оптимальной питательной среды, культивирование. Выделение целевого продукта, его очистка, стандартизация, придание лекарственной формы. Генетическая инженерия сводится к созданию необходимый для человека целевой продукции. Полученный целевой ген сшивают с вектором, а вектором может быть плазмиды и встраивают его в клетку реципиента. Реципиент – бактерия – кишечная палочка, дрожжи. Синтезируемые рекомбинантами целевые продукты, выделяют очищают и используют в практике.
Первыми, были созданы инсулин и человеческий интерферон. Эритропоэтин, гормон роста, монокланальные антитела. Вакцина против гепатита Б.
Источник: dendrit.ru
Строение бактериофагов
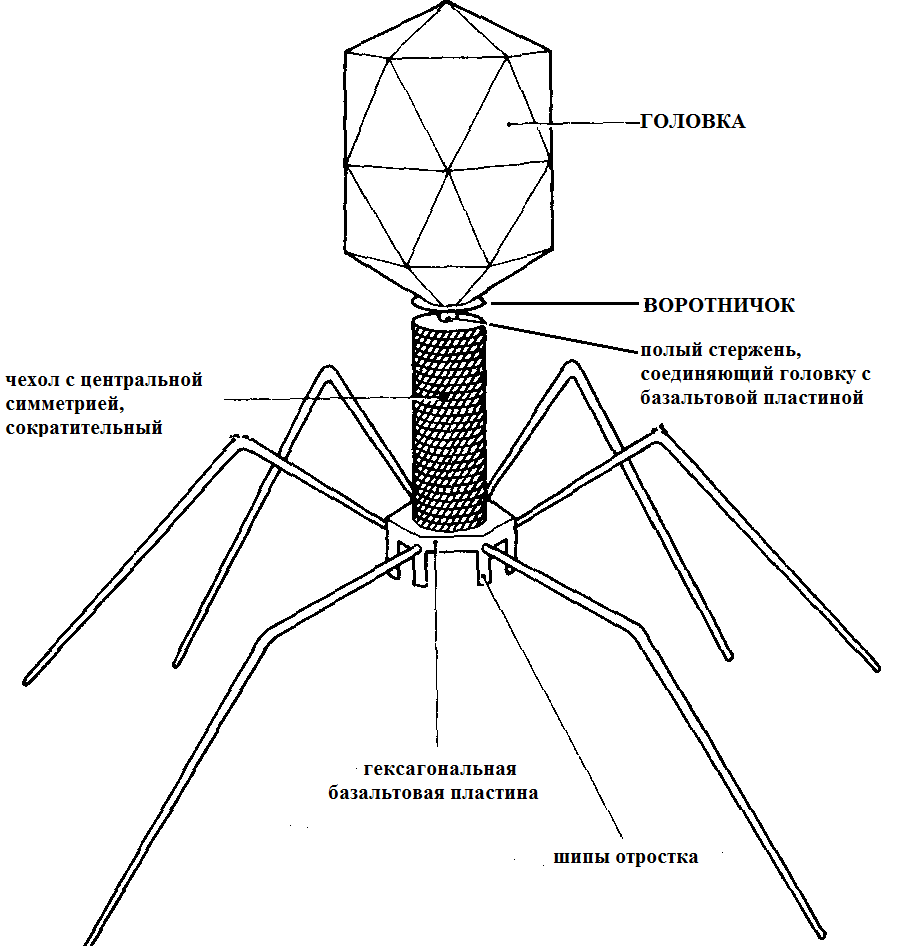
 В отличие от вирусов животных и растений бактериофаг имеет более сложное и более впечатляющее строение. Строение некоторых фагов чем-то напоминает строение космического корабля. Генетическая информация данного вируса (это ДНК или РНК) заключена в капсиде – белковой оболочке. Капсид или головка имеет разную форму (шестигранная, овальная, круглая, призматическая). Как видно из рисунка под головкой расположен воротничок. Еще ниже, под воротничком расположен полый стержень, который заключен в чехол. Чехол похож на пружину и устроен таким образом, что при надобности может сокращаться (сжиматься). Под полым стержнем и чехлом расположена базальтовая пластина шестиугольной формы с короткими выступами (шипами). Также от базальтовой пластины отходят нитевидные образования (фибриллы).
В отличие от вирусов животных и растений бактериофаг имеет более сложное и более впечатляющее строение. Строение некоторых фагов чем-то напоминает строение космического корабля. Генетическая информация данного вируса (это ДНК или РНК) заключена в капсиде – белковой оболочке. Капсид или головка имеет разную форму (шестигранная, овальная, круглая, призматическая). Как видно из рисунка под головкой расположен воротничок. Еще ниже, под воротничком расположен полый стержень, который заключен в чехол. Чехол похож на пружину и устроен таким образом, что при надобности может сокращаться (сжиматься). Под полым стержнем и чехлом расположена базальтовая пластина шестиугольной формы с короткими выступами (шипами). Также от базальтовой пластины отходят нитевидные образования (фибриллы).
Размеры бактериофагов бывают разными, хотя их относят к вирусам, которые имеют средние размеры.
Взаимодействие бактериофага с бактериальной клеткой
Большинство бактериофагов имеют сократительный чехол. У таких фагов механизм проникновения в клетку отличается от других вирусов. Они осаждаются на поверхности бактериальной клетки с помощью отростков (фибрилл) и через шипы выделяется особый фермент – лизоцим, который разрушает мембранную стенку клетки бактерии. После этого чехол сокращается и его внутренний полый стержень как игла проникает в клетку. Сразу, после проникновения стержня в клетку нуклеиновая кислота (генетическая информация) через отверстие полого стержня впрыскивается в цитоплазму бактериальной клетки. Сам бактериофаг после передачи наследственной информации в отличие от вирусов растений и животных остается вне клетки. Через 30-40 минут после проникновения нуклеиновой кислоты в цитоплазму клетки происходит синтез новых 200 фаговых единиц, которые своим присутствием увеличивают внутриклеточное давление и разрушают мембраны клетки.
Среда обитания фагов
В окружающей нас природе там, где есть бактерии, обитают и бактериофаги.
Практически все болезнетворные бактерии человека и животных содержат эти микроорганизмы. Следует также отметить, что бактериофаги присущи и у непатогенных микробах. К таким микробам относят молочнокислые бактерии, азотобактерии, бактерии лучистых грибов (на основе их готовят антибиотики), клубеньковые бактерии.
Классификация бактериофагов
В настоящее время обнаружено и исследовано большинство бактериофагов. Их различают по типу нуклеиновой кислоты, по структурной организации и форме, а также по характеру взаимодействия с клеткой бактерии. По этим признакам их разделили на 13 семейств, более чем на 140 родов.
История открытий бактериофагов
Данные вирусы впервые обнаружил в 1896 году британский бактериолог Эрнст Ханкин. После открытия вирусов, которые имеют свойство разрушать бактерии, бактериофагами заинтересовались ученные во многих странах мира. Российский ученым Николай Гамалея в 1898 предложил использовать их при лечении ран и различных инфекционных заболеваний. Вплоть до 1940 года в лабораториях всего мира велись интенсивные исследования и практическое применение этих микроорганизмов. Затем исследования по изучению свойств бактериофагов прекратились и ушли в забытье кроме Советского Союза. На территории Грузии был создан современный институт, который до настоящего времени исследует бактериофаги. Мировая медицина на какое-то время утратила интерес к этим вирусам в связи с появлением антибиотиков. Но постепенно процесс исследования и применения бактериофагов во всем мире возобновляется.
Лечение бактериофагами
Антибиотики не всегда эффективно работают, кроме болезнетворных бактерий убивают и полезные, таким образом, разрушая микрофлору кишечника. Многие болезнетворные бактерии адаптировались к действию антибиотиков, выработали устойчивость к их химическому воздействию. Другое дело бактериофаги. При правильном применении этих микроорганизмов разрушаются только вредные болезнетворные микробы, не нарушается микрофлора кишечника, выздоровление наступает быстро и без каких–либо нежелательных последствий. В медицинских учреждениях, после соответствующих анализов, теперь назначают пациентам коктейли содержащие бактериофаги.
Related posts:
Источник: muvrasil.ru
Факт 1: Бактериофаги имеют три основных типа структуры
Поскольку бактериофаги являются вирусами, они состоят из нуклеиновой кислоты (ДНК или РНК), заключенной в оболочку белка или капсид. У бактериофага также может быть хвост белка, прикрепленный к капсиду, с хвостовыми волокнами, простирающимися от хвоста.
Хвостовые волокна помогают фагу присоединяться к хозяину, а хвост обеспечивает ввод вирусных генов в хозяина. Бактериофаги могут иметь следующее строение:
- вирусные гены в капсидной головке и без хвоста;
- вирусные гены в капсидной головке с хвостом;
- нитевидный или стержневидный капсид с круглой одноцепочечной ДНК.
Факт 2: Бактериофаги упаковывают свой геном
Как вирусы укомплектовывают объемный генетический материал в свои капсиды? РНК-бактериофаги, вирусы растений и вирусы животных имеют механизм саморасширения, который позволяет вирусному геному вмещаться в контейнер капсида.
Похоже, что только у РНК вирусов этот механизм включает самосгибания. ДНК вирусы помещают свой геном в капсид с помощью специальных ферментов, известных как упаковочные ферменты.
Факт 3: Бактериофаги имеют два жизненных цикла
Бактериофаги способны воспроизводить либо лизогенные, либо литические жизненные циклы. Лизогенный цикл также известен как умеренный цикл, потому что хозяин не погибает. Вирус вводит свои гены в бактериальную хромосому. В этом цикле бактериофаг реплицируется внутри хозяина. Хозяин погибает, когда вновь реплицированные вирусы ломают или лизируют клетку-хозяина и освобождаются.
Факт 4: Бактериофаги переносят гены между бактериями
Бактериофаги помогают переносить гены между бактериями посредством генетической рекомбинации. Этот тип передачи генома известен как трансдукция. Трансдукция может быть достигнута либо литическим, либо лизогенным циклом. В литическом цикле, фаг вводит свою ДНК в бактерию, и ферменты разделяют бактериальную ДНК на кусочки. Гены фага направляют бактерии для получения большего количества вирусных генов и вирусных компонентов (капсиды, хвост и т.д.).
По мере того как новые вирусы начинают собираться, бактериальная ДНК может непреднамеренно входить в вирусный капсид. В этом случае фаг обладает бактериальной ДНК вместо вирусной. Когда этот фаг заражает другую бактерию, он вводит ДНК из предыдущей бактерии в клетку-хозяина. Затем донорская бактериальная ДНК встраивается в геном вновь инфицированной бактерии путем рекомбинации. В результате гены из одной бактерии переносятся в другую.
Факт 5: Бактериофаги могут создавать бактерии, вредные для человека
Бактериофаги играют роль в заболевании людей, превращая некоторые безвредные бактерии в возбудителей болезни. Некоторые виды бактерий, включая кишечную палочку, стрептококк пиогенес, холерный вибрион и шигеллы становятся вредными, когда гены, которые производят токсичные вещества, передаются им через бактериофаги. Эти бактерии могут заразить людей и вызвать пищевое отравление или даже смертельные заболевания.
Факт 6: Бактериофаги используются для борьбы с вредоносными бактериями
Ученые выделили бактериофагов, которые разрушают клостридиум диффициле, влияющих на пищеварительную систему, вызывая диарею и колит. Лечение этого типа инфекций бактериофагами дает возможность сохранить хорошие кишечные бактерии, уничтожая только клостридиум диффициле.
Бактериофаги рассматриваются в качестве отличной альтернативы антибиотикам. Из-за чрезмерного употребления антибиотиков устойчивые штаммы бактерий становятся все более распространенными. Бактериофаги также используются для уничтожения других вредоносных бактерий, включая лекарственно-устойчивые кишечную палочку и золотистый стафилококк.
Факт 7: Бактериофаги играют важную роль в углеродном цикле мира
Бактериофаги являются наиболее распространенным вирусами в океане. Фаги, известные как Pelagiphages, заражают и уничтожают бактерии группы SAR11. Эти бактерии превращают молекулы растворенного углерода в углекислый газ и влияют на количество углерода в атмосфере Земли. Pelagiphages играют важную роль в углеродном цикле планеты, уничтожая бактерии SAR11, размножающиеся с высокой скоростью и очень хорошо адаптирующиеся к различным инфекциям.
Источник: natworld.info